Studi Proteomik Kuantitatif Mengungkap Jalur Fibrinogen pada Penyakit Hati Polikistik Ⅱ
Nov 22, 2023
3. Hasil
3.1. Ginjal dan Hati Tidak Mengikuti Mekanisme Kistik yang Sama
Penelitian sebelumnya menunjukkan bahwa inaktivasi awal gen Pkd1 (sebelum p12) memicu perkembangan penyakit polikistik yang cepat (jendela kistik), sedangkan inaktivasi setelah p14 menyebabkan pembentukan kista yang terlambat setelah 4-5 bulan, dengan fenotip ringan (jendela non-kistik) [19]. Dengan menggunakan model ADPKD ortologis yang sama (Pkd1cond/cond; Tam-Cre) [18,19], kami menyelidiki apakah periode perkembangan ginjal ini berhubungan dengan periode perkembangan hati yang serupa. Untuk menarik perbandingan langsung dengan penelitian kami sebelumnya [37], tikus diinduksi dengan tamoxifen untuk menonaktifkan gen Pkd1 pada hari ke 14 (p14) dan 12 (p12) pascakelahiran dan dikorbankan pada usia 30 hari (p30). Menariknya, kami mengamati fenotip kistik pada kedua titik waktu dengan tingkat penyakit yang berbeda (ringan dan berat), menunjukkan bahwa ginjal dan hati memiliki jendela perkembangan kistik yang independen (Gambar 1a), dan/atau kemungkinan waktu dan perkembangan penyakit yang berbeda. . Tidak ada perbedaan yang ditemukan antara jantan dan betina pada usia penyembelihan antara kedua jendela inaktivasi (n=6 digunakan untuk setiap kelompok mutan). Hewan mutan p14 menunjukkan fenotip yang lebih ringan dibandingkan kelompok mutan p12 dengan nilai indeks kistik, jumlah kista, dan fungsi hati yang lebih rendah menurut nilai serum ALP (Gambar 1b – d). Ini adalah studi pertama yang menunjukkan jendela/mekanisme perkembangan berbeda untuk defisiensi hati dan ginjal Pkd1. Perbedaan molekuler tersebut harus ditentukan dalam penelitian selanjutnya.
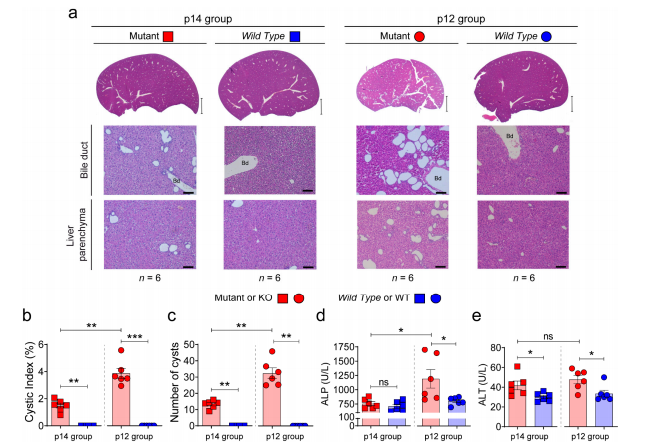
Gambar 1. Karakterisasi fenotip hati kistik pada hari ke 30 dari tahap p12 dan p14. Penghapusan Pkd1 di p12 membawa sistogenesis yang lebih parah. (a) Gambar makroskopis dan mikroskopis representatif dari hematoxylin-eosin yang diwarnai dari hati Pkd1cond/cond; Tikus Tam-Cre Tipe Liar (WT, Pkd1cond/cond; Tam-Cre−) dan Mutant (KO, Pkd1cond/cond; Tam-Cre+ ) dengan penghapusan gen Pkd1 yang diinduksi oleh tamoxifen pada hari ke 14 pascakelahiran (kelompok p14) dan 12 (kelompok p12). Semua tikus dikorbankan di p30. Bilah skala, 2 mm (panel atas) 100 µm (panel bawah). n mewakili jumlah sampel per kelompok, dan Bd berarti saluran empedu. (b,c) Indeks kistik hati dan jumlah kista dari berbagai fenotipe. (d,e) Nilai ALP dan ALT serum darah. Batangan mewakili rata-rata ± SEM dalam semua kasus. p <0,05 dengan uji-t Student (dua sisi) dianggap sebagai hasil yang signifikan. ns mewakili tidak signifikan. * p < 0,05, ** p < 0,01, *** p < 0,001.

Klik cistanche herba untuk penyakit ginjal
3.2. Analisis Proteomik Shotgun dan SWATH-MS di PLD
Sebagaimana dimaksud pada Gambar 2, kami melakukan analisis proteom diferensial pada kedua tahap kistik (p12—penyakit kistik parah- dan p14—penyakit kistik ringan-) dari Mutan (KO) dibandingkan dengan hewan Tipe Liar (WT), untuk mengidentifikasi dan mengkarakterisasi mekanisme molekuler yang relevan yang menjalani sistogenesis hati dan perkembangan penyakit.

Gambar 2. Skema alur kerja yang diilustrasikan. Kami menggunakan model murine ADPKD (Pkd1cond/cond; tikus Tam‐Cre) di mana inaktivasi genetik Pkd1 diinduksi oleh pemberian tamoxifen pada hari ke 10 pascakelahiran (p10) dan p11 (perkembangan penyakit yang cepat) atau p15 dan p16 (perkembangan penyakit tertunda ) menurut peralihan perkembangan untuk sistogenesis ginjal, mendefinisikan dua kelompok penelitian yang masing-masing diberi nama p12 dan p14 [19]. Untuk kedua kelompok, kami menggunakan n individu yang sama atau lebih besar dari enam tipe liar (WT) dan Mutan (KO) di setiap kondisi, dan semua hewan dikorbankan pada p30. Kami mempelajari perbedaan proteom hati WT dan KO pada kedua tingkat keparahan penyakit kistik hati (Gambar 1), menggunakan proteomik kuantitatif SWATH-MS dan analisis DDA-MS akuisisi yang bergantung pada data shotgun. Dari protein dengan perubahan kelimpahan yang signifikan, kami menggunakan bioinformatika. Gambar 2. Skema alur kerja yang diilustrasikan. Kami menggunakan model murine ADPKD (Pkd1cond/cond; tikus Tam-Cre) di mana inaktivasi genetik Pkd1 diinduksi dengan pemberian tamoxifen pada hari ke 10 pascakelahiran (p10) dan p11 (perkembangan penyakit yang cepat) atau p15 dan p16 (perkembangan penyakit tertunda ) menurut peralihan perkembangan untuk sistogenesis ginjal, mendefinisikan dua kelompok penelitian yang masing-masing diberi nama p12 dan p14 [19]. Untuk kedua kelompok, kami menggunakan n yang sama atau lebih besar dari enam individu Tipe Liar (WT) dan Mutan (KO) di setiap kondisi, dan semua hewan dikorbankan pada p30. Kami mempelajari perbedaan proteom hati WT dan KO pada kedua tingkat keparahan penyakit kistik hati (Gambar 1), menggunakan proteomik kuantitatif SWATH-MS dan analisis DDA-MS akuisisi yang bergantung pada data. Dari protein dengan perubahan kelimpahan yang signifikan, kami menggunakan alat bioinformatika untuk mendeteksi target terapi baru dan jalur yang terlibat dalam penyakit. Terakhir, kami memvalidasi target tersebut dengan menggunakan strategi in silico (analisis DDA vs SWATH) pertama dan terakhir in vivo, serta RT-qPCR, Western blotting, dan imunohistokimia. p berarti hari pascakelahiran

Pola Ekspresi Protein dalam Sistogenesis Hepatik Pertama, kami melakukan analisis spektrometri massa proteomik dengan akuisisi DDA-MS atau DDA yang bergantung pada data. Analisis ini memungkinkan karakterisasi proteom dari sampel lengkap dan individual, memberikan ada/tidaknya protein dengan sensitivitas tinggi tetapi tanpa memberikan kuantifikasinya. Kami secara eksklusif mempertimbangkan semua protein yang diekspresikan secara berbeda di lebih dari lima sampel independen dari total enam sampel, masing-masing untuk tahap p14 dan p12 dari Tipe Liar dan individu mutan (Gambar S1). Pada p14, 1 protein eksklusif WT (atau regulasi turun untuk penyakit) dan 7 protein eksklusif MUT (regulasi naik) diidentifikasi, sedangkan pada p12, delapan protein eksklusif WT dan enam protein eksklusif MUT diamati (Gambar S1).
Selanjutnya, kami menggunakan metode yang memungkinkan kami mengukur protein yang diekspresikan secara berbeda. Kami melakukan analisis proteomik kuantitatif SWATH-MS pada sampel yang sama yang kami gunakan untuk DDA, memperoleh ~1500 protein per sampel dan lebih dari 2000 protein di setiap kelompok studi. Pertama, kami melakukan normalisasi jumlah area total (TAS) untuk mengevaluasi bahwa sampel kami mengikuti pola distribusi normal, seperti yang ditunjukkan pada Gambar S2 dan S3. Selanjutnya, kami mempelajari protein dengan perbedaan signifikan antara kelompok Tipe Liar dan Mutan. Tabel 1 menunjukkan protein dengan perubahan kelimpahan yang signifikan dengan peningkatan dua kali lipat (regulasi ke atas) atau penurunan (regulasi ke bawah), dan nilai p yang disesuaikan secara signifikan (menurut uji parametrik Student) pada WT vs Sampel MUT di p14 dan p12. Secara total, enam protein menunjukkan perbedaan signifikan dalam kelimpahan protein antara kelompok WT p14 dan MUT-p14 (lima protein dengan regulasi naik dan satu protein dengan regulasi turun). Antara WT-p12 dan MUT-p12, 26 protein (20 protein diatur ke atas dan 6 protein diatur ke bawah) menunjukkan perbedaan yang signifikan (Gambar 3a dan Tabel 1). Secara grafis, variasi ini dapat diamati melalui plot gunung berapi, yang dihasilkan dengan memplot perubahan lipatan log(2) untuk semua protein yang diidentifikasi terhadap nilai p-log(10) (Gambar 3b). Perbedaan yang signifikan antara tingkat kelimpahan protein dapat divisualisasikan dalam peta panas dengan nilai individual sesuai dengan area perpustakaan spektral, dan tingkat pengelompokannya dalam analisis peta panas klaster (Gambar 3c dan S4). Cluster yang terdeteksi oleh analisis SWATH-MS membantu kami mengidentifikasi sampel yang dipisahkan secara kualitatif, untuk dipertimbangkan dalam analisis kuantitatif (Gambar S5). Analisis statistik multivariat tanpa pengawasan dilakukan menggunakan analisis komponen utama (PCA) untuk membandingkan data antar sampel (Gambar S6). Data peta panas dan PCA menunjukkan reproduktifitas di antara sampel rangkap tiga karena ketiga ulangan tersebut berkerumun erat di kedua analisis. Kita dapat mengamati baik di PCA maupun dalam analisis klaster peta panas (Gambar S5 dan S6) bagaimana beberapa sampel tidak dikelompokkan dengan benar, sehingga tumpang tindih di antara kedua klaster. Meskipun demikian, kita dapat melihat kecenderungan untuk memisahkan data dalam cluster Wild Type dan Mutant. Jumlah protein yang lebih rendah dengan perbedaan p14 vs p12 yang signifikan dapat dibenarkan oleh tingkat keparahan yang berbeda (Gambar 2), menunjukkan bahwa jumlah protein dan jalur meningkat berdasarkan tingkat keparahan dan status penyakit dari fenotip kistik.
3.3. Clustering, Pengayaan Jalur dan Analisis Interaksi Protein-Protein Ekspresi Gen di PLD
Untuk menetapkan fungsi yang terkait dengan protein yang diekspresikan secara berbeda yang diidentifikasi dengan analisis SWATH-MS, kami menggunakan beberapa alat bioinformatik dan bentuk analisis. Analisis istilah dan jalur Gene Ontology (GO) dilakukan menggunakan FunRich [39,40], String [41] dan Reactome [42]. Protein diurutkan dalam analisis pengayaan gen FunRich. Mengenai proses biologis, kelompok protein yang paling diperkaya untuk kelompok p14 (kistik ringan) terkait dengan transpor asam lemak dan biosintesis prostaglandin, dan untuk kelompok p12 (kistik parah) dengan aktivitas fibrinogen/fibrin, adhesi sel-sel/matriks dan metabolisme. proses (Gambar 4a, panel atas). ANXA2 dan kompleks fibrinogen adalah dua komponen seluler yang paling kaya pada kelompok p14 dan p12. Selain itu, ruang ekstraseluler adalah komponen seluler dengan persentase protein tertinggi pada kedua kelompok (Gambar 4a, panel bawah). Demikian pula, analisis yang sama dilakukan dengan analisis string, mengidentifikasi berbagai proses metabolisme sebagai proses biologis utama, dan ruang ekstraseluler sebagai komponen sel yang paling diperkaya; konsisten dengan hasil GO (Gambar S7a). Terakhir, kami mengulangi analisis dengan platform Reactome, dan menemukan bahwa metabolisme dan sistem kekebalan adalah jalur yang paling diperkaya (Gambar S7b).

Analisis protein-protein atau cluster berdasarkan analisis string juga dilakukan untuk menyelidiki kemungkinan interaksi protein-protein (interaksi dengan bukti eksperimental). Banyak interaksi protein diidentifikasi dalam kelompok yang berbeda (Gambar S8), tetapi satu kelompok di p14 dan satu lagi di p12 adalah yang paling relevan berdasarkan jumlah interaksi antara protein dan tingkat ekspresi (Gambar 4b). Cluster p14-mengandung protein annexin A2 (ANXA2_P07356) yang terkait dengan beberapa fungsi seluler, seperti fibrinolisis, motilitas sel (dalam sel epitel), protein yang terkait dengan aktin interaksi sitoskeleton dan matriks sel [43], berinteraksi dengan dua protein lain yang terlibat dalam transpor lipid intraseluler (FABP1_P12710 dan FABP5_Q05816). Menariknya, kelompok protein lain yang relevan diidentifikasi dalam kluster p12-dengan interaksi protein-protein yang sangat kuat antara beberapa fibrinogen (FGL1_Q71KU9, FIBB_Q8K0E8, FIBA{{22 }}E9PV24 dan FIBGG_Q8VCM7). Fibrinogen terlibat dalam pertumbuhan hepatosit, dan memediasi penyebaran trombosit darah, kolagen interstisial, dan lesi fibrotik [44]. Selain itu, protein tambahan ditemukan berinteraksi dengan fibrinogen (Gambar S8), seperti komponen p amiloid serum (SAMP_P12246), hemopexin (HEMO_Q91X72) atau asam hidroksi oksidase 2 (HAOX{ {37}}Q9NYQ2). Konsisten dengan hasil string, kompleks ANXA2 dan fibrinogen juga merupakan komponen seluler yang paling diperkaya yang diidentifikasi oleh analisis FunRich (Gambar 4a). Menariknya, ketika membandingkan data yang diperoleh dengan analisis DDA dan SWATH, kami memastikan bahwa beberapa protein yang diidentifikasi oleh SWATH juga diidentifikasi dengan analisis DDA, termasuk beberapa yang terkait dengan protein kompleks fibrinogen (SAMP/Apcs dan S10A9/S100a9; Tabel S3).
3.4. Validasi Analisis SWATH-MS Mengungkap Kompleks Fibrinogen sebagai Mekanisme Molekuler Baru Terkait PLD
Berdasarkan data ini, kami memilih dari analisis SWATH-MS (Gambar S9) protein yang diubah terkait dengan kompleks fibrinogen pada tahap p12 dan p14 untuk validasi in vivo dengan RT-qPCR, Western blotting dan imunohistokimia, untuk menetapkan konfirmasi mereka mungkin. sasaran penyakit. Delapan dari 1{24}} protein terpilih ini divalidasi pada tingkat mRNA oleh RT-qPCR (Gambar 5); satu diregulasi pada tahap 14-(ANXA2_P07356) dan pada grup p12-(SAMP_P12246, FGL1_Q71KU9, ILK{{ 17}}O55222, S10A9_P31725, FIBB_Q8K0E8, HEMO_Q91X72, FIBA_E9PV24 dan FIBG_Q8VCM7), dan satu down- diatur di grup p12 (HAOX2_Q9NYQ2). Menariknya, ekspresi gen dari dua protein dengan jarak yang lebih jauh atau interaksi yang lebih sedikit terhadap kelompok fibrinogen (ILK dan S10A9) adalah satu-satunya yang tidak divalidasi (Gambar 5c).

Peningkatan regulasi kompleks fibrinogen (protein ANXA2, SAMP, FIBB, FIBA, FIBG dan HAOX2) selanjutnya dikonfirmasi dengan analisis Western blotting (WB) (Gambar 6). Secara keseluruhan, ekspresi gen dan WB sangat konsisten dengan data proteomik SWATH-MS. Terakhir, kami juga melakukan validasi imunohistokimia kompleks fibrinogen pada sampel hati mutan dan polikistik (Gambar 7). Pewarnaan fibrinogen sangat diatur dalam sel epitel pelapis kista dan dilatasi saluran empedu (Gambar 7a). Hasil ini mengungkap, untuk pertama kalinya, kompleks fibrinogen sebagai jalur yang mungkin terkait dengan sistogenesis hati dan sebagai target terapi PLD di masa depan.

Gambar 5. Validasi kemungkinan target PLD oleh RT-qPCR. Ekspresi gen dari 8 hingga 1{26}} target terpilih dikorelasikan dengan data SWATH-MS. RT-qPCR dari target p14 terpilih yang diregulasi, lampiran A2 (Anxa2) (a); p12 yang diregulasi menargetkan komponen p amiloid, serum (Apcs, gen SAMP), fibrinogen-like 1 (Fgl1), rantai beta fibrinogen (Fgb), hemopexin (Hpx), rantai alfa fibrinogen (Fga), rantai gamma fibrinogen (Fgg) (b), integrin linked kinase (Ilk) dan S10{{30}} protein pengikat kalsium A9 (S100a9) (c); dan target p12 target hidroksi asam oksidase 2 (Hao2) (d) yang diatur ke bawah. n=6 digunakan untuk setiap kelompok protein. Gapdh digunakan sebagai gen rumah tangga. Batangan mewakili rata-rata ± SEM. Uji-t Student dengan dua sisi digunakan dan nilai p <0,05 dianggap signifikan. ns: tidak signifikan (p lebih besar atau sama dengan 0,05), * p < 0,05, ** p < 0,01, *** p < 0,001.

Gambar 7. Kompleks fibrinogen diatur ke atas dalam epitel kistik. (a,b) Gambar representatif imunohistokimia fibrinogen di saluran empedu (panel atas) dan parenkim hati (panel bawah) (a) dan kuantifikasinya (b). n=6 digunakan untuk setiap grup. Analisis imunohistokimia menunjukkan peningkatan regulasi fibrinogen melalui epitel kistik. Sampel sesuai dengan kelompok p12. Bilah skala mewakili 100 µm. Bd artinya saluran empedu. Batangan mewakili rata-rata ± SEM. Uji-t Student dengan dua sisi digunakan dan nilai p <0,05 dianggap signifikan. *** hal < 0,001.
Layanan Pendukung Wecistanche-Ekspor cistanche terbesar di Cina:
Surel:wallence.suen@wecistanche.com
Whatsapp/Telp:+86 15292862950
Belanja Untuk Detail Spesifikasi Lebih Lanjut:
https://www.xjcistanche.com/cistanche-toko






