Jalan Terapi Baru yang Menjanjikan Curcumin dalam Penyakit Otak
Jun 24, 2022
Mohon hubungi{0}}untuk informasi lebih lanjut
Abstrak:Curcumin, polifenol diet yang diisolasi dari Curcuma longa (kunyit), umumnya digunakan sebagai ramuan dan rempah-rempah di seluruh dunia. Karena efek biofarmakologinya, kurkumin juga disebut sebagai “bumbu kehidupan”, padahal diketahui bahwa kurkumin memiliki khasiat penting seperti anti-oksidan, anti-inflamasi, anti-mikroba, antiproliferatif, anti-tumor, dan anti penuaan. Penyakit neurodegeneratif seperti Penyakit Alzheimer, Penyakit Parkinson, dan Multiple Sclerosis adalah sekelompok penyakit yang ditandai dengan hilangnya struktur dan fungsi otak secara progresif akibat kematian neuron; saat ini, tidak ada pengobatan yang efektif untuk menyembuhkan penyakit ini. Efek perlindungan kurkumin terhadap beberapa penyakit neurodegeneratif telah dibuktikan oleh penelitian in vivo dan in vitro.ukuran penis cistancheTinjauan saat ini menyoroti temuan terbaru tentang efek neuroprotektif kurkumin, bioavailabilitasnya, mekanisme kerjanya, dan kemungkinan penerapannya untuk pencegahan atau pengobatan gangguan neurodegeneratif.

Silakan klik di sini untuk tahu lebih banyak
Kata kunci:kurkumin; flavonoid alami; peradangan saraf; antiinflamasi; penyakit neurodegeneratif; penyakit Alzheimer; penyakit Parkinson; sklerosis ganda; glioblastoma multiforme; epilepsi
1. Perkenalan
Bukti terbaru menunjukkan bahwa penggunaan nutraceuticals dan suplemen makanan dapat membawa perlindungan ke sistem saraf pusat (SSP) dengan melestarikan neuron terhadap kerusakan akibat stres, menekan peradangan saraf, dan meningkatkan kinerja neurokognitif.
Kurkumin adalah salah satu konstituen kurkuminoid hadir dalam kunyit (Curcuma longa Limn) dan merupakan ramuan abadi dari keluarga Zingiberaceae. Kunyit, juga disebut "bumbu emas" digunakan sebagai obat dalam pengobatan tradisional dan juga banyak digunakan dalam masakan Asia sebagai bahan tambahan makanan dan sebagai zat pewarna dalam industri minuman [1].
(1E,6E)-1,7-bis(4-hidroksi-3-metoksifenil)-1,6-heptadiena-3, 5-dion adalah nama IU-PAC dari kurkumin, rumus kimianya adalah CanHzoOg dan memiliki berat molekul 368,38g/mol. Berbagai aktivitas biologis dan sifat terapeutik kurkumin disebabkan oleh kimianya, khususnya gugus hidroksil fenolik, bis-, -diketon tak jenuh pusat, ikatan terkonjugasi ganda, dan gugus metoksi bertanggung jawab atas efek biofarmakologisnya. Kurkumin adalah molekul lipofilik, dengan kelarutan yang buruk dalam air atau larutan hidrofilik, sebaliknya, mudah larut dalam pelarut organik seperti metanol, etanol, aseton, dan dimetil sulfoksida, kloroform [2].
Kompleks kurkuminoid mengandung kurkumin, demethoxycurcumin dan bis-deme thoxycurcumin [3].

Cistanche dapat anti-penuaan
Kurkumin, seperti fitokimia lainnya, memiliki aktivitas pleiotropik pada sel, pada kenyataannya, karena kemampuannya untuk berinteraksi dengan banyak protein, kurkumin dapat memicu respons seluler terhadap rangsangan eksternal. Selain itu, kurkumin mengatur naik-turun berbagai miRNA dan dapat menyebabkan perubahan epigenetik dalam sel. Beberapa percobaan in vitro, in vivo dan klinis telah berfokus pada efek terapeutik potensial dari kurkumin termasuk antioksidan [4], imunomodulator, pelindung jantung [5], nefroprotektif [6], hepatoprotektif [7,8], anti-neoplastik [9 ,10], anti-mikroba, anti-diabetes [11]anti-rematik[12] anti-penuaan [13], anti-inflamasi terutama anti-neuroinflamasi [14]serta sifat penghambatan untuk mikroglia [15].
Meskipun banyak manfaat terapeutiknya, senyawa bioaktif ini memiliki bioavailabilitas yang buruk karena penyerapan yang tidak mencukupi, ketidakstabilan kimia, dan metabolisme yang cepat dalam tubuh.
Untuk meningkatkan bioavailabilitas kurkumin, nanocarrier telah terbukti menjadi strategi yang menjanjikan, untuk meningkatkan efek terapeutiknya.
Karena ukuran nanometrik dan sifat kimianya, nanopartikel [16], liposom [17,18]misel, vesikel fosfolipid [19], dan nanopartikel polimer [20,21] mampu meningkatkan efektivitas kurkumin.
Di antara nanocarrier alami, vesikel ekstraseluler, terutama eksosom, digunakan sebagai sistem untuk pengiriman obat.bubuk cistancheEksosom dilepaskan dari sel melalui eksositosis setelah pematangan badan multivesikular.
Eksosom mampu memediasi komunikasi seluler dengan komposisi protein, lipid, dan asam nukleatnya [22]. Membran lipid eksosom mengandung kurkumin melalui interaksi antara ekor hidrofobik dan bahan aktif hidrofobik. Penyisipan dalam lipid bilayer menjamin perlindungan kurkumin dari degradasi [23]. Faktanya, kurkumin dengan formulasi eksosomal lebih efektif dibandingkan dengan kurkumin liposomal dan kurkumin bebas [23].
Zhang dkk. telah menunjukkan bahwa ex yang mengandung kurkumin yang diberikan intranasal datang dalam model penyakit yang dimediasi peradangan, seperti model peradangan otak yang diinduksi Lipopolisakarida (LPS), ensefalitis autoimun eksperimental, dan model tumor otak GL26, menginduksi perlindungan saraf dengan mengurangi peradangan saraf atau ukuran tumor [24 ].
Pada cedera iskemia-reperfusi (I/R), eksosom yang mengandung kurkumin mampu menurunkan produksi spesies oksigen reaktif (ROS) pada lesi, mengurangi kerusakan sawar darah otak (BBB), dan menekan apoptosis neuron yang dimediasi mitokondria. ]. Liposom adalah nanovesikel yang terdiri dari satu atau beberapa lapisan ganda fosfolipid yang membungkus molekul hidrofilik, lipofilik, dan amfifilik [26], yang dapat digunakan untuk mengantarkan obat ke situs target.
Mohajeri dkk. telah menunjukkan efek anti-inflamasi dan anti-oksidan dari nano-curcumin terpolimerisasi yang memiliki efek positif pada model ensefalomielitis autoimun eksperimental multiple sclerosis, dan mekanisme perbaikan mielin yang diinduksi [27].

Nano-curcumin memiliki efek neuroprotektif pada cedera otak dini, ternyata mampu melemahkan disfungsi BBB setelah perdarahan subarachnoid dengan mencegah penghancuran protein persimpangan ketat (ZO-1, occludin, dan claudin-5) . Selain itu, nano-kurkumin up-mengatur transporter glutamat -1 yang mengurangi konsentrasi glutamat dalam cairan serebrospinal (CSF) berikut perdarahan subarachnoid dan menghambat aktivasi mikroglia [28]. Kombinasi asam lemak w-3 dan nano-kurkumin secara signifikan mengurangi frekuensi serangan migrain dengan modulasi ekspresi gen IL-6dan tingkat Protein C-Reaktif, sebagaimana dibuktikan dalam serangkaian uji klinis [29 ]. Liposom yang mengandung CUR mengurangi aktivitas enzim pengubah angiotensin di daerah target otak dan mempotensiasi pemulihan memori pada tikus dengan penyakit Alzheimer (AD) [30].
Seiring dengan meningkatnya harapan hidup di seluruh dunia, penyakit neurodegeneratif meningkat dan ini menyebabkan beban ketidaknyamanan sosial-ekonomi yang lebih besar bagi pasien, keluarga, dan masyarakat [31]. Penyakit neurodegeneratif ditandai dengan gangguan yang menyebabkan gangguan progresif struktur dan/atau fungsi neuron dan jaringan sinaptiknya yang akhirnya menyebabkan hilangnya fungsi otak.
AD, penyakit Parkinson (PD), penyakit Huntington (HD), Multiple Sclerosis (MS), dan amyotrophic lateral sclerosis (ALS) adalah penyakit neurodegeneratif yang paling umum hadir pada orang tua.
Faktor yang menyebabkan penyakit neurodegeneratif antara lain polimorfisme genetik, bertambahnya usia, jenis kelamin, pendidikan yang buruk, penyakit endokrin, stres oksidatif, peradangan, stroke, hipertensi, diabetes, merokok, trauma kepala, depresi, infeksi, tumor, kekurangan vitamin, gangguan kekebalan dan metabolisme. , dan paparan bahan kimia [32].
Respon inflamasi di dalam otak atau sumsum tulang belakang dikenal sebagai peradangan saraf. Peradangan saraf umum terjadi pada sejumlah penyakit otak, termasuk AD, PD, MS, dan banyak lainnya. Proses ini dimediasi melalui produksi sitokin, kemokin, spesies oksigen reaktif, dan utusan sekunder, yang dapat menghancurkan BBB, mengakibatkan kerusakan sel dan hilangnya fungsi saraf [33]. Glia, sel endotel, dan sel imun yang berasal dari perifer menghasilkan mediator ini. Di antara sel glial, mikroglia dan astrosit memainkan peran sentral dalam patofisiologi penyakit neurodegeneratif. Astrosit bekerja sama untuk mempertahankan homeostasis SSP dan meningkatkan kelangsungan hidup neuron dengan mengatur lalu lintas metabolit dan aliran darah. Sel mikroglia merasakan gangguan homeostasis jaringan otak dan berfungsi sebagai fagosit SSP [34,35]. Tujuan dari tinjauan ini adalah untuk menekankan pentingnya kurkumin dalam pengobatan AD, PD, MS glioblastoma, dan epilepsi yang berfokus pada mekanisme aksi potensialnya dalam meningkatkan perjalanannya.
2. Kurkumin dan AD
AD merupakan penyebab utama demensia di seluruh dunia, terhitung 60-80 persen dari kasus yang didiagnosis dengan demensia [36]. Secara klinis, AD biasanya ditandai dengan hilangnya memori, penurunan kognitif progresif, dan penurunan tingkat fungsi dan kinerja sebelumnya di tempat kerja atau aktivitas biasa. Neurodegenerasi telah dikaitkan dan didorong oleh agregat ekstraseluler dari plak amiloid (A) dan kusut neurofibrillary intraseluler (NFI) yang terbuat dari protein tau hiperfosforilasi di daerah kortikal dan limbik otak manusia [37l. Pembentukan plak A dimulai dari pemrosesan anomali protein prekursor amiloid APP) oleh -secretases BACE1) dan -secretases, yang mengarah ke produksi berbagai jenis monomer A, di antaranya A 40 dan A 42 (sangat tidak larut dan agregasi -Rentan). Akibatnya, monomer A terus mengalami oligomerisasi dan beragregasi menjadi plak. NFTs adalah ciri patologis kedua AD dan terdiri dari tau hiperfosforilasi terlokalisasi di sitoplasma neuron [38]. Tau memiliki domain pengikat mikrotubulus dan berkumpul dengan tubulin, menghasilkan pembentukan mikrotubulus yang stabil. A dapat mengaktifkan beberapa kinase, termasuk glikogen sintase kinase 3 (GSK-3), cyclin-dependent kinase 5(CDK5), dan lainnya seperti Protein Kinase C, Protein Kinase A, ekstraselular signal-regulated kinase 2 (ERK2), serin/treonin kinase, yang memfosforilasi tau, yang mengarah ke oligomerisasinya [39. Akibatnya, mikrotubulus menjadi tidak stabil, dan subunitnya berubah menjadi potongan besar filamen tau, yang selanjutnya bergabung menjadi NFI. NFI sangat tidak larut dan menyebabkan hilangnya komunikasi yang abnormal antara neuron dan sinyal untuk diproses dan akhirnya apoptosis pada neuron [40]. Menurut hipotesis amiloid, perubahan patologis tau dianggap sebagai peristiwa hilir deposisi A. Namun, juga telah dihipotesiskan bahwa A dan tau bertindak dalam jalur paralel yang menyebabkan AD dan memperkuat efek toksik satu sama lain [41]. Mengingat dampak sosial dan ekonomi, penting untuk memahami faktor risiko mana yang dapat mempengaruhi perkembangan DA dan juga menemukan obat yang dapat mencegah timbulnya atau menghentikan perjalanan penyakit. tersedia untuk pengobatan AD, seperti penghambat asetilkolinesterase (donepezil, rivastigmine, dan galantamine) dan memantine antagonis glutamat, yang tidak efektif dalam menghentikan perjalanan penyakit yang progresif 42].ekstrak cistanche salsaBaru-baru ini, FDA menyetujui penggunaan obat pertama dengan mekanisme modifikasi penyakit diduga, Aducanumab, yang merupakan antibodi monoklonal manusia yang secara selektif bereaksi dengan agregat A dan mengurangi plak A di otak, sehingga memprediksi manfaat klinis yang penting. Namun, uji klinis pasca-persetujuan diperlukan untuk memverifikasi manfaat klinis obat yang sebenarnya [43]. Beberapa senyawa alami baru-baru ini diselidiki untuk lebih memahami kemanjuran potensi mereka dalam "pengobatan" AD [44]. Penelitian saat ini difokuskan pada mekanisme aksi kurkumin dan perannya dalam modulasi perkembangan AD.
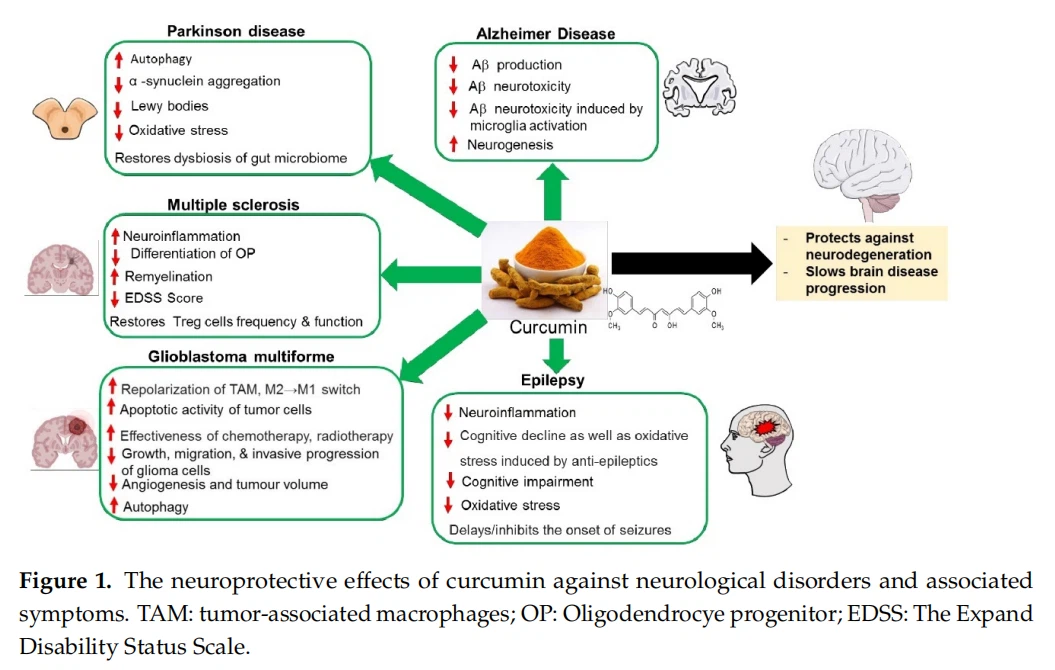
Mekanisme kerja kurkumin adalah pleiotropik (Tabel S1)[45] dan menargetkan A dan tau (lihat Gambar 1). Selain itu, ia memodulasi aspek lain dari proses penyakit: ia juga mengikat tembaga, menurunkan kadar kolesterol, memodifikasi aktivitas mikroglial, menghambat asetilkolinesterase, meningkatkan jalur pensinyalan insulin, dan bertindak sebagai antioksidan [45]. Curcumin tampaknya menargetkan A pada tingkat yang berbeda. Bahkan, telah dijelaskan bahwa itu menghambat produksi A; selain itu, kurkumin menghambat agregasi baik in vitro dan pada model tikus sehingga mencegah pembentukan plak dan mempromosikan disagregasi bentuk fibrillar [46].
Mengenai produksi A, studi in vitro menunjukkan bahwa kurkumin bertindak sebagai penghambat BACE1, yang terlibat dalam pembelahan APP[47l. Hasil ini dikonfirmasi pada model tikus AD, menunjukkan bahwa kurkumin menurunkan regulasi ekspresi BACE1, sehingga mengurangi pembentukan A [48].
Selain itu, kurkumin tampaknya menghambat aktivasi presenilin 1 (PS1) yang bergantung pada GSK-3 -dan akibatnya mengurangi produksi A. Faktanya, sel-sel neuroblastoma SHSY5Y yang diobati dengan kurkumin menunjukkan penurunan yang nyata pada kadar PS1 dan GSK-3 dan pengurangan yang nyata dari produksi A dengan cara yang bergantung pada dosis dan waktu [49]. GSK-3 diaktifkan saat didefosforilasi di situs Ser9. Aktivitasnya diatur ke hulu oleh Akt, protein kinase spesifik serin/treonin. Phosphatidylinositol (PIP) dan fosforilasi Akt yang dimediasi PDK di situs Ser473 dan Thr308 mengarah ke aktivasi Akt dan fosforilasi konsekuen dan penghambatan GSK-3 . Aktivitas Akt diatur secara negatif oleh PTEN, yang mengkatalisis fosfoinositida menjadi defosforilasi yang menonaktifkan pensinyalan PIP3. Jalur pensinyalan PI3K/Akt/GSK-3 juga dipengaruhi secara langsung oleh paparan A [50], memang, oligomer mengaktifkan GSK-3 melalui defosforilasi di situs Ser9. Selain itu, A menginduksi penurunan regulasi fosforilasi Akt dan juga ekspresi berlebih PTEN, regulator negatifnya, yang mengarah pada aktivasi hilir GSK-3 . Kurkumin menghambat overekspresi PTEN mRNA, penurunan regulasi aktivasi Akt yang dimediasi fosforilasi, dan juga aktivasi GSK-3 yang dimediasi A [51,52], sehingga mengurangi produksi A dan penumpukan plak (Gambar 2) .

Mengenai peran kurkumin dalam menghambat agregasi A , telah disarankan bahwa kurkumin mengganggu kestabilan gaya tarik yang diperlukan untuk pembentukan lembaran - dalam plak amiloid melalui hidrofobisitasnya atau interaksinya antara cincin keto atau enol dan cincin aromatik dimer A [53]. Destabilisasi -sheet juga dipengaruhi oleh interaksi antara gugus hidroksil kurkumin pada cincin aromatik dan kantong polar A [54].
Menariknya, penelitian in vitro baru-baru ini berfokus pada peran kurkumin dalam mencegah neurotoksisitas A. Thapa dkk. menunjukkan bahwa kurkumin mengurangi laju penyisipan A ke dalam membran plasma dan akibatnya bertindak sebagai faktor pelindung terhadap toksisitas membran A. Secara lebih rinci, kurkumin mengurangi gangguan membran plasma karena A , sehingga menghindari peningkatan masuknya kalsium dan kematian sel [55]. Efek neuroprotektif kurkumin, mungkin dimediasi membran, tampaknya bertindak dengan mengurangi toksisitas yang disebabkan oleh berbagai konformer A, termasuk monomer, oligomer, pra-fibrillary, dan fibrillary A [56]. Menariknya, juga telah dijelaskan bahwa kurkumin mempromosikan pembentukan oligomer larut "off-pathway" dan agregat pra-fibrilar yang tidak beracun [56]. Studi lain oleh Huang et al. menunjukkan bahwa kurkumin mampu melemahkan aktivasi yang dimediasi A dari reseptor glutamat NMDA dan dengan demikian menghambat peningkatan intraseluler Ca² plus , yang terlibat dalam toksisitas glutamat. Efek kurkumin pada depresi reseptor NMDA/Ca2 plus jalur tampaknya mencegah kerusakan sel yang disebabkan oleh A [57]. Terlepas dari hasil yang menarik ini, studi in vivo masih diperlukan untuk menerjemahkan temuan ini dan menemukan potensi penggunaan klinis. Mengenai NFI, GSK-3 mengatur fosforilasi tau dengan menambahkan gugus fosfat pada residu asam amino serin dan treonin. Kurkumin telah terbukti mencegah hiperfosforilasi tau yang bertindak sebagai inhibitor GSK-3 [45,47]. Secara lebih rinci, Huang dkk.[51] menunjukkan bahwa kurkumin menghambat hiperfosforilasi tau yang diinduksi A yang melibatkan jalur PTEN/Akt/GSK-3 dalam kultur sel manusia dan akibatnya mempengaruhi penghambatan hiperfosforilasi tau yang mencegah agregasi di NFI.
Curcumin juga dapat memainkan peran dalam pembersihan NFT dengan pengurangan konsekuen dalam toksisitas yang diinduksi tau. Memang, dalam kultur sel neuron tikus, kurkumin, pada konsentrasi rendah, meningkatkan ekspresi BCL2 terkait athanogene 2 (BAG2), pendamping molekul yang memberikan tau ke proteasome untuk degradasi [58].batang cistancheNamun, karena penelitian ini tidak dilakukan pada neuron patologis, hasil ini perlu dikonfirmasi. Studi lain oleh Miyasaka et al. menggambarkan tingkat asetilasi -tubulin, indikator stabilisasi mikrotubulus, secara signifikan lebih besar pada nematoda yang diberi kurkumin, menunjukkan bahwa kurkumin dapat mengurangi neurotoksisitas yang dimediasi tau dengan meningkatkan stabilisasi mikrotubulus [59]. Selain A dan NFT, faktor lain harus diperhitungkan dalam patogenesis AD. Mikroglia memiliki peran penting dalam respon imun bawaan dari SSP dan dapat diklasifikasikan dalam M1 (yang mengeluarkan sitokin neurotoksik, prostaglandin, ROS, dan oksida nitrat) dan fenotipe M2 (yang melepaskan mediator neuroprotektif dan anti-inflamasi dan agregat protein toksik fagosit). ). Peran mikroglia dalam AD telah dipelajari secara mendalam [60]. A menyimpang mikroglia dari neuroprotektif M2 ke neurotoksik M1 fenotipe [61]. Selain itu, akumulasi A mengaktifkan mikroglia, yang menghasilkan mediator inflamasi sehingga meningkatkan akumulasi A lebih lanjut, yang mengarah ke loop umpan balik positif ini. Kurkumin tampaknya memainkan peran dalam mengurangi neurotoksisitas karena aktivasi mikroglia yang diinduksi A [62]. Dalam hal ini, dilaporkan bahwa kurkumin memblokir pensinyalan ERK1/2 dan p38 kinase dalam mikroglia yang diaktifkan A sehingga mengurangi produksi TNF-x, IL-1 , dan IL-6 [63] dan, selain itu, melemahkan pelepasan oksida nitrat ]64]. Selain itu, kurkumin menekan fosfoinositida 2 kinase (PI3K)/fosforilasi Akt dan aktivasi faktor nuklir-kB (NF-kB), yang mendorong aktivasi mikroglia dan jalur peradangan saraf [64]. Menariknya, kurkumin menginduksi peningkatan kadar protein reseptor y (PPARy) yang diaktifkan proliferator peroksisom, sehingga meningkatkan aktivitas anti-inflamasi PPARy dalam downregulasi jalur NF-kB dan ERK. Di sisi lain, kurkumin dapat meningkatkan efek neuroprotektif mikroglia M2: pada kenyataannya, fagositosis A tampaknya meningkat pada mikroglia pada pasien AD yang diobati dengan kurkuminoid in vitro [65].
Penurunan signifikan dalam neurogenesis telah banyak dijelaskan pada AD dan penyakit neurodegeneratif lainnya [66]. Karya-karya sebelumnya menemukan bahwa kurkumin mengatur neurogenesis melalui aktivasi jalur Wnt in vitro dan di zona hippocampus dan subventrikular tikus dewasa. Wnt berinteraksi dengan 7-reseptor Frizzled transmembran dan lipoprotein densitas rendah koreseptor terfosforilasi (LRP-5/6), sehingga mengarah pada aktivasi protein acak-acakan sitoplasma (Dvl). Setelah diaktifkan, protein Dvl berinteraksi dengan kompleks penghancuran Axin/APC/GSK-3 dan menghambat GSK-3 . Penghambatan GSK-3 menyebabkan akumulasi sitoplasma -catenin dan translokasinya ke dalam inti sel. Di dalam nukleus, -catenin berinteraksi dengan kompleks promotor TCF/LEF, yang menyebabkan aktivasi gen target yang terlibat dalam proliferasi dan diferensiasi SSP. Curcumin tampaknya mempengaruhi jalur ini pada tingkat yang berbeda. Secara lebih rinci, kurkumin berinteraksi dengan Wif-1 dan Dkk-1, yang merupakan molekul penghambat Wnt, sehingga meningkatkan kadar Wnt. Selain itu, kurkumin kemungkinan dapat berinteraksi dengan GSK-3 , sehingga meningkatkan kadar -catenin sitoplasma, dan meningkatkan translokasi nuklir -catenin, yang mengarah pada peningkatan aktivitas promotor TCF/LEF dan cyclin-D1 dan peningkatan neurogenesis. Menariknya, telah ditunjukkan bahwa meskipun konsentrasi kurkumin otak yang rendah (500 nM) merangsang neurogenesis, konsentrasi otak yang tinggi 10 M) menghambat neurogenesis dan neuroplastisitas [67]. Oleh karena itu, pemilihan konsentrasi kurkumin harus hati-hati. Model praklinis sebagian besar telah menunjukkan efek positif kurkumin pada AD, namun, hanya sejumlah studi klinis yang meneliti efek kurkumin pada fungsi kognitif manusia pada AD dan hasilnya kurang konsisten. Temuan pada pengurangan A tidak jelas karena tidak ada perubahan signifikan pada kadar A atau tau dalam plasma atau CSF yang ditemukan antara kurkumin dan plasebo [68,69]. Di sisi lain, neuroimaging mendukung bahwa kurkumin mengurangi deposit A di otak pada 2-(1-{6-[(2-[F-18]fluoroethyl) (metil) amino-2-naphthyl}ethylidene) malononitrile positron emission tomography (FDDNP-PET) pada pasien non-demensia [70]. Inkonsistensi ini mungkin terkait dengan perbedaan metodologi dan populasi yang disertakan |71. Selain itu, kurkumin menunjukkan bioavailabilitas yang rendah dan efeknya pada jalur antioksidan dan neurogenesis mungkin membutuhkan lebih banyak waktu untuk menginduksi peningkatan yang signifikan dalam kapasitas kognitif dan pengurangan A. Dengan demikian, efek ringan yang dijelaskan sebelumnya juga bisa disebabkan oleh durasi pengobatan yang relatif singkat. Studi lebih lanjut diperlukan untuk meningkatkan bioavailabilitas kurkumin dan untuk lebih mengeksplorasi efek kurkumin pada A dan NFT, untuk memahami apakah kurkumin dapat menjadi kontributor potensial baru untuk pencegahan dan pengobatan DA.
3. Efek Terapi Kurkumin pada PD
PD adalah penyakit neurodegeneratif kedua yang paling umum setelah AD. Diperkirakan 10 juta orang menderita PD di seluruh dunia pada tahun 2020 (https://www.epda.eu.com/, diakses pada 27 Oktober 2021)[72]. PD terutama mempengaruhi neuron penghasil dopamin di substantia nigra otak tengah yang menyebabkan disfungsi motorik dan kognitif yang parah. Pada PD idiopatik, mekanisme patofisiologis meliputi produksi -synuclein dan kompleks yang mempengaruhi disfungsi pernapasan mitokondria, yang disebabkan oleh ROS [73]. Hal ini juga ditandai dengan akumulasi agregat protein, terutama terdiri dari -synuclein, karena kegagalan mekanisme degradasi protein seperti sistem lisosom [74,75]. Sebagian besar modalitas pengobatan yang ada hanya bersifat simptomatik. Ini termasuk suplemen dopamin yang mengontrol sementara disfungsi motorik yang disebabkan oleh degenerasi sistem nigrostriatal dopaminergik. Stimulasi otak dalam (DBS) digunakan pada PD yang resistan terhadap obat.
Untuk mencegah stres oksidatif dan mengurangi perkembangan penyakit, penggunaan antioksidan alami tetap menjadi terapi alternatif yang potensial. Mengingat efek neuroprotektif, anti-inflamasi, dan anti-oksidan terhadap neurodegenerasi kurkumin yang diinduksi stres, di sini kami membahas temuan terbaru terkait dengan efek menguntungkan kurkumin dalam mengurangi perkembangan dan pencegahan PD [12].
Meskipun patogenesis PD masih belum jelas, beberapa mekanisme telah diusulkan dan berbagai bukti mendukung peran penting disfungsi mitokondria dalam patogenesis PD [76].
Sebuah studi baru-baru ini melaporkan efek perlindungan kurkumin terhadap disfungsi mitokondria dan kematian sel dalam model knock-down PINK1 yang dimediasi siRNA [77]. Studi lain menjelaskan efek kurkumin pada disfungsi mitokondria dalam model PD toksisitas yang diinduksi paraquat, pada fibroblas yang berasal dari LRRK 2- PD mutasi-positif dan kontrol kesehatan. Faktanya, pra-perawatan model sel ini dengan kurkumin sebelum perawatan paraquat, meningkatkan respirasi maksimal dan respirasi terkait ATP tanpa mempengaruhi kapasitas pernapasan. Setelah pengobatan paraquat, pasca pengobatan fibroblas dengan kurkumin tidak meningkatkan respirasi mitokondria di tiga parameter (respirasi maksimal, respirasi terkait ATP, dan kapasitas pernapasan cadangan), sehingga menunjukkan efek pencegahan kurkumin sebelum timbulnya PD. 78].

Sebuah studi terbaru oleh Motawi et al. [79] menyelidiki efek kurkumin dan suplemen makanan pada model tikus rotenone PD menunjukkan peningkatan keseluruhan yang signifikan secara statistik. Memang, pemberian kurkumin pada tikus yang diberi rotenon meningkatkan kadar -synuclein dan mengurangi badan Lewy. Perilaku hewan juga meningkat dan tingkat mediator inflamasi berkurang secara signifikan pada tikus yang diobati dengan kurkumin bila dibandingkan dengan kelompok kontrol. Ini termasuk IL-6, CRP, dan Ang Il, yang sebelumnya ditunjukkan dengan efek pro-inflamasi dan pro-fibrotik yang berkontribusi pada kerusakan progresif fungsi organ pada PD[80]. Ketika mengevaluasi penanda PD, penurunan yang signifikan pada tingkat ekspresi gen adenosin A2AR ditemukan pada tikus yang diobati dengan kurkumin dibandingkan dengan kelompok rotenon. Peningkatan lain yang menjanjikan dalam kadar dopamin dan serotonin dicatat pada model tikus PD yang diobati dengan kurkumin. Selain itu, pengobatan dengan kurkumin menyebabkan berkurangnya stres oksidatif pada model tikus PD [79]. Bukti pendukung lainnya menunjukkan hasil yang serupa pada model tikus PD dengan respons tikus yang lebih tinggi terhadap perawatan kurkumin mengenai stres oksidatif dan indeks energik. Oleh karena itu, kurkumin melemahkan efek parah PD pada model tikus dan dapat dilihat sebagai suplemen makanan potensial [81].
Bukti dari literatur telah menunjukkan bahwa gangguan jalur autophagy-lisosom (ALP) memainkan peran penting dalam patogenesis PD. Sebuah studi baru-baru ini berfokus pada efek kurkumin pada oligomer alfa-synuclein( S) melalui metode simulasi dinamika molekuler menunjukkan bahwa kurkumin mengurangi stabilitas struktural oligomer S dengan mengganggu sifat umumnya. Selanjutnya, agregasi oligomer -synuclein dicegah dan pembentukan pembentukan fibril dihambat oleh kurkumin [82].
Karena kemampuan kurkumin dalam mengurangi -synuclein yang salah lipat dengan mempromosikan autophagy, penelitian terbaru telah menyelidiki efeknya pada regulasi autophagy. Dengan demikian, pengobatan model seluler untuk PD telah menunjukkan peningkatan ekspresi protein terkait mikrotubulus 1 rantai ringan 3(LC3-II), penentuan protein plasma inti dari faktor transkripsi nuklir EB(TFEB), dan autophagy- protein terkait protein membran lisosom 2 (ALAMP2A). Ini menghasilkan peningkatan sintesis autophagy-lisosom dan pembersihan autophagic dari -synuclein [83,84].
TFEB telah diidentifikasi sebagai salah satu regulator kunci penting dari autophagy dan biogenesis lisosom [8586]. Ini telah memperkuat hipotesis bahwa TFEBcan dianggap sebagai target terapi baru untuk PD. Faktanya, turunan kurkumin, yang disebut E4 (analog kurkumin), mampu mengaktifkan dan mempromosikan translokasi TFEB dari sitoplasma ke dalam nukleus. Translokasi ini disertai dengan stimulasi autophagy dan biogenesis lisosom. Secara mekanis, senyawa E4 mengaktifkan TFEB melalui penghambatan jalur AKT-MTORC1. Selain itu, dalam model sel PD, E4 telah terbukti mengurangi tingkat -synuclein dan melindungi terhadap sitotoksisitas MPP plus (1-metil-4-ion fenilpiridinium) dalam sel saraf. Data yang menjanjikan ini menunjukkan efek perlindungan in vitro dari E4 namun masih memerlukan uji eksperimental in vivo lebih lanjut karena bioavailabilitas otak dari E4 masih belum diketahui. Kemanjuran neuroprotektif dari E4 perlu dieksplorasi lebih lanjut pada model hewan PD [87].
Selain itu, injeksi kurkumin intraperitoneal in vivo mempromosikan ekspresi protein LC3-II dan menghambat ekspresi P62 yang mendukung autophagy. Kurkumin menghambat ekspresi a-synuclein dan apoptosis neuron dopamin dalam model tikus PD yang diinduksi MPTP (kurkumin 80mg/kg selama 14 hari) dan memperbaiki gangguan gerakan pada tikus 33]. Telah ditunjukkan bahwa anestesi sevoflurane menginduksi gangguan kognitif dengan mengaktifkan autophagy di hipokampus tikus muda [88]. Menariknya, kurkumin mampu memodulasi autophagy pada 300 mg/kg selama enam hari dan menghambat gangguan memori pada tikus yang diinduksi oleh sevofluran [89]. Efek protektif kurkumin diselidiki dalam pemberian secara oral dalam 6-hidroksi dopamin (6-OHDA) - model hewan yang diinduksi PD.manfaat dan efek samping cistanche tubulosaEfek neuroprotektif kurkumin pada (200 mg/kg) 2 minggu sebelum dan sesudah operasi dinilai dengan analisis morfologi dan perilaku. Fungsi motorik dinilai tiga minggu setelah operasi. Curcumin telah secara signifikan meningkatkan perilaku motorik abnormal dan terbukti melindungi terhadap neuron dopaminergik yang berkurang di substantia nigra dan nukleus caudate-putamen seperti yang ditunjukkan oleh imunoreaktivitas tirosin hidroksilase (TH).
Pemberian intraperitoneal metil-aconitine antagonis selektif 7-nAChR membalikkan efek neuroprotektif ini. Ini mengkonfirmasi implikasi 7-nAChRs dalam efek yang dimediasi kurkumin. Dalam penelitian ini, ditunjukkan bahwa kurkumin memiliki efek neuroprotektif dalam model tikus 6-hydroxy dopamine(6-OHDA) PD melalui mekanisme yang diperantarai 7-nAChR [90]. Zhang dkk. telah menunjukkan bahwa ekspresi G2385R-LRRK2 menginduksi neurodegenerasi pada neuroblastoma manusia SH-SY5Y dan neuron primer tikus. Neurotoksisitas yang dimediasi oleh stres oksidatif ini menghasilkan aktivasi jalur apoptosis. Kurkumin, yang menunjukkan aktivitas antioksidan, telah secara signifikan melindungi terhadap gabungan G2385R-LRRK2-yang diinduksi neurodegenerasi dengan melemahkan tingkat ROS mitokondria, aktivasi caspase-3/7, dan pembelahan PARP dan mengurangi stresor lingkungan seluler H , O, (Gambar 2). Hasil ini memberikan wawasan baru tentang mekanisme neurodegenerasi terkait G2385R-LRRK2-dan efek terapeutik potensial kurkumin pada pasien PD yang membawa G2385R [91].
Selain mekanisme kurkumin-neuroprotektif yang dibahas di atas terhadap PD, minat baru yang berkembang pada sumbu usus-otak pada PD dapat menjelaskan sifat neuroprotektif kurkumin terlepas dari bioavailabilitasnya yang terbatas. Sebenarnya, kurkumin dapat bekerja secara tidak langsung pada SSP melalui sumbu mikrobiota-usus. Sistem dua arah yang kompleks yang memainkan peran penting dalam kesehatan otak masih belum sepenuhnya dipahami.
Studi terbaru menunjukkan bahwa kurkumin mengembalikan disbiosis mikrobioma usus. Disbiosis didefinisikan sebagai kondisi komunitas mikroba yang stabil yang secara fungsional berkontribusi pada etiologi, diagnosis, atau pengobatan penyakit [92]. Namun, modifikasi kurkumin oleh bakteri tidak membentuk metabolit kurkumin yang lebih aktif [93]. Interaksi timbal balik ini dapat mempertahankan fungsi fisiologis yang seimbang dan memainkan peran kunci dalam perlindungan saraf dan pencegahan perkembangan dan perkembangan PD. Meskipun meningkat, minat penelitian pada gejala non-motorik terkait PD seperti depresi, defisit penciuman, sembelit, tidur, dan gangguan perilaku, efek kurkumin pada PD memerlukan penyelidikan lebih lanjut.
Secara bersama-sama, kurkumin menunjukkan efek yang menjanjikan dalam pengobatan PD (Tabel S1) (lihat Gambar 1). Namun, mengeksplorasi lebih banyak formulasi kurkumin dalam model in vivo dan dalam uji klinis akan memberikan kemajuan lebih lanjut dalam penggunaan kurkumin sebagai terapi pencegahan untuk memblokir atau memperlambat timbulnya PD.
4. Kurkumin sebagai Kandidat Terapi di MS
MS adalah penyakit demielinisasi kronis, neuroinflamasi, autoimun dari SSP pada orang dewasa muda yang mempengaruhi jutaan orang [94]. MS dikaitkan dengan beberapa proses patofisiologis termasuk peradangan kronis, perubahan sistem kekebalan, pelanggaran BBB sebagai episode relapsing-remitting (RR), infiltrasi sejumlah besar leukosit, stres oksidatif, demielinasi yang akibatnya menyebabkan kerusakan aksonal dan neuron, remielinasi dan aktivasi sistem perbaikan [95-98]. Meskipun penyebab MS masih belum diketahui, para ilmuwan percaya bahwa MS adalah penyakit multifaktorial yang melibatkan kombinasi faktor genetik, lingkungan, dan autoimun yang berkontribusi pada risiko pengembangan MS [99]. Fase awal peradangan ditandai dengan kontribusi IL-22, IL-17, dan sel T yang mengarah ke aktivasi kaskade inflamasi dan fitur MS patofisiologis lainnya, yang merupakan penyebab demielinasi dan kerusakan aksonal [100].
Sampai saat ini, hanya pengobatan simtomatik yang tersedia untuk MS, yang berfokus pada pengobatan kekambuhan dan remisi episode penyakit. Perawatan MS saat ini dikenal sebagai terapi pengubah penyakit (DMT) di mana berbagai senyawa telah dikembangkan. Sebagian besar terapi ini adalah senyawa imunomodulator, disetujui untuk pengobatan berbagai jenis MS dan menargetkan jalur patofisiologis yang berbeda [101,102]. Strategi pengobatan lain sedang digunakan yang melibatkan terapi sel induk yang digunakan seperti transplantasi sel induk hematopoietik autologus (HSCT) dan terapi monoklonal penipisan sel B [102]. Relaps adalah gambaran klinis yang dominan dari RRMS, tetapi juga terjadi pada fase awal dari MS progresif sekunder [103]. Pilihan strategi pengobatan untuk relaps dan remisi MS (RRMS), hadir di 85-90 persen pasien dengan MS, masih kontroversial [104] Hal ini disebabkan variabilitas gejala terkait dengan MS untuk setiap individu. Meskipun banyak terapi yang tersedia, tantangan baru telah diajukan mengenai identifikasi strategi terapi yang tepat untuk setiap kasus individu. Selain itu, profil keamanan dan kemanjuran untuk senyawa ini, serta pemahaman tentang kemungkinan efek samping tetap menjadi tantangan. Efek samping, kegagalan terapi, laporan toksisitas, dan mahalnya obat kimia saat ini merupakan faktor yang mendukung pertimbangan tanaman obat, termasuk kurkumin, untuk tujuan terapeutik. Beberapa sifat kurkumin baru-baru ini telah diidentifikasi, beberapa di antaranya mungkin efektif dalam mengobati MS, terutama sifat anti-inflamasinya dengan menghambat sekresi sitokin pro-inflamasi (Gambar 1)[103]. Di sini, kita akan meninjau berbagai sifat dan efek utama kurkumin untuk mengobati MS (Tabel S1). Mengingat peran astrosit yang sangat diperlukan dalam perbaikan dan pemulihan dari MS, garis sel astrosit manusia (U373-MG) digunakan sebagai model seluler MS dalam penelitian sebelumnya [105]. Dalam sel-sel pra-perawatan dengan LPS, kurkumin mengurangi pelepasan aktivitas IL6 dan MMP9, meskipun itu tidak mempengaruhi tingkat mRNA faktor pertumbuhan seperti insulin (IGF)-1 atau neurotropin-3. Ini mendukung efek anti-inflamasi kurkumin pada astrosit di SSP [106]. Ensefalomielitis autoimun eksperimental (EAE) yang dihasilkan dengan injeksi mielin ke tikus digunakan sebagai model eksperimental untuk mempelajari MS. Minat kurkumin sebagai calon terapi potensial untuk MS juga berkembang. Menariknya, temuan terbaru tentang efek kurkumin pada model tikus Lewis EAE telah menunjukkan bahwa nanoCUR (PNC) terpolimerisasi yang diberikan dengan dosis 12,5 mg/kg memiliki efek terapeutik yang efisien dengan efek signifikan pada skor EAE dan menunjukkan mekanisme perbaikan mielin. Faktanya, PNC meningkatkan mielinisasi melalui mekanisme perbaikan yang ditingkatkan yang menginduksi faktor neurotropik yang ditingkatkan. Selain itu, ia membalikkan peradangan saraf yang diinduksi EAE dengan menghambat ekspresi gen pro-inflamasi NF-kB, IL-1, IL-17, TNF-, MCP-1 dan meningkatkan efek anti-inflamasi. ekspresi gen IL-4, IL-10, FOXP3, dan TGF-. Selain itu, PNC memodulasi ekspresi penanda stres oksidatif. Lebih menariknya, pretreatment dengan PNChas meningkatkan penanda sel progenitor dan perkembangan EAE tertunda [27.107.108]. Mengingat pentingnya oligodendrosit dan nenek moyangnya yang belum matang, yang merupakan target penting untuk strategi terapeutik untuk pengobatan penyakit demielinasi, efek kurkumin pada oligodendrosit dipelajari. Investigasi efek kurkumin pada diferensiasi progenitor oligodendrosit (OP), terutama pada penyakit inflamasi, telah menunjukkan bahwa kurkumin meningkatkan diferensiasi OP melalui peningkatan ekspresi penanda yang terkait dengan berbagai tahap perkembangan. Kurkumin mampu mengaktifkan PPAR-y di OPs dengan menunjukkan translokasi nuklir PPAR-【109】 yang bergantung pada kurkumin. Kemampuan kurkumin untuk mempromosikan diferensiasi OP menjadi (oligodendrosit imatur) OL melibatkan beberapa mekanisme, termasuk aktivasi PPAR-y dan ERK1/2 dan pencegahan efek merusak yang diinduksi TNF- -. Sebuah studi baru-baru ini telah mengkonfirmasi efektivitas nanoformulasi kurkumin pada karakteristik inflamasi pada pasien dengan MS. Memang, kurkumin secara signifikan menurunkan ekspresi miRNA termasuk miR-145, miR-132, dan miR-16, serta mediator inflamasi seperti STAT-1, NF-kB, AP-1, IL-1, IL-6, IFN-y, CCL2, CCL5, TNF-. Di sisi lain, nanoCUR telah menginduksi peningkatan yang signifikan dalam tingkat ekspresi Sox2, Sirtuin -1, Foxp3, dan PDCD1. Selain itu, tingkat sekresi IFN-, CCL2, dan CCL5 secara drastis berkurang pada kelompok pasien yang diobati dengan kurkumin dibandingkan dengan kelompok plasebo [110]. Sel T helper 1 (Th1) dan T helper 17(Th17) terlibat dalam patogenesis MS dan diyakini sebagai target terapi [111] (lihat Gambar 2). Penelitian terbaru pada model EAE dan pasien MS menyoroti peran penting sel Th17 dalam memediasi peradangan saraf autoimun. Th17, garis keturunan pro-inflamasi dari sel Th efektor diyakini sebagai penghasil sitokin paling penting dari IL17 [112]. Oleh karena itu, sel-sel ini terlibat dalam demielinasi dan degenerasi aksonal/neuronal. Menariknya, bila dibandingkan dengan kelompok plasebo, proporsi sel Th17 dan tingkat ekspresi RORyt dan IL-17 secara signifikan menurun pada pasien MS yang menerima suntikan interferon -1a(Actovex) mingguan dan dilengkapi dengan NanoCUR selama 6 bulan [113]. Secara dominan, skor EDSS pada kelompok pasien MS yang dilengkapi dengan nanoCUR menunjukkan kualitas yang lebih baik dibandingkan dengan kelompok plasebo. Secara keseluruhan, nanoCUR dapat menghambat perkembangan penyakit pada pasien MS. Kesimpulannya, nanoCUR berpotensi dipandang sebagai agen neuroprotektif terhadap perkembangan MS, terutama menargetkan sifat inflamasi MS. Penelitian lain yang menggunakan model EAE telah menyarankan peran sentral dari CD4 plus sel T(Treg) pengatur dalam patogenesis dan eksaserbasi MS [114-117]. Penting untuk ditekankan bahwa frekuensi dan fungsi supresi sel Treg terganggu pada pasien dengan MS [118,119]. Studi terbaru lainnya oleh Dolati et al. menjelaskan efek nanoCUR pada fungsi dan frekuensi Treg pada pasien dengan MS. Sekelompok dari mereka menerima efek kapsul nanoCUR selama setidaknya enam bulan, kelompok lain menerima plasebo sebagai kelompok kontrol. Peningkatan frekuensi sirkulasi Treg dengan ekspresi FoxP3 yang lebih tinggi telah diamati pada pasien MS. Secara keseluruhan, formulasi nano kurkumin mampu menurunkan skor EDSS pada pasien MS dibandingkan dengan baseline, menunjukkan pemulihan dari kejadian kambuh daripada peningkatan nyata. Berdasarkan hasil di atas, ditemukan bahwa nanoCUR dianggap sebagai agen imunomodulator dengan mengatur fungsi fungsi sistem kekebalan tubuh dan mencegah autoreaktivitas dengan memodulasi proporsi dan fungsi sel Treg pada pasien MS [120]. Pengamatan ini menunjukkan bahwa nanoCUR mampu memulihkan frekuensi dan fungsi sel Treg pada pasien MS, menyoroti mekanisme terapeutik kurkumin yang muncul dalam pengobatan MS sebagai strategi untuk mempromosikan remielinasi.
5. Efek Terapi Kurkumin pada Glioblastoma Multiforme
Glioblastoma (GBM) adalah glioma difus paling agresif dari garis keturunan astrositik dan diklasifikasikan sebagai glioma grade IV menurut klasifikasi WHO [121]. GBM adalah tumor otak primer ganas yang paling umum dan menyumbang 54 persen dari semua glioma dan 16 persen dari semua tumor otak primer [122]. GBM tetap merupakan tumor yang tidak dapat disembuhkan dengan tingkat kelangsungan hidup 14-15bulan setelah diagnosis [123.124]. Meskipun kemajuan dalam reseksi bedah, prognosis untuk pasien dengan GBM tetap buruk dan suram [125]. Pendekatan standar untuk pengobatan GBM adalah reseksi bedah maksimal diikuti dengan radiasi pasca operasi harian dan kemoterapi. Temozolomide, agen alkilasi oral yang dapat melewati BBB, adalah pengobatan lini pertama yang paling umum untuk GBM setelah operasi. Ini digunakan dalam kombinasi dengan terapi radiasi [126].
Mengingat sifat invasif dari potensi metastasis GBM, reseksi tumor yang lengkap sulit dilakukan. Banyak faktor yang dapat mempengaruhi efektivitas terapi gabungan ini, termasuk efisiensi target otak yang buruk dan resistensi multidrug (MDR), yang menyebabkan sel GBM menunjukkan respons monoterapi yang sangat buruk bahkan ketika kambuh dari rongga marginal yang direseksi 127. Faktanya, efektivitas dari obat kemoterapi temozolomide (TMZ) sering dibatasi oleh resistensi obat dan efek samping yang semakin meningkat [128,129]. Oleh karena itu, pengobatan GBM tetap menantang ketika ada kebutuhan mendesak untuk meningkatkan hasil kemoterapi dan untuk mengidentifikasi target potensial baru untuk pengobatan GBM.
Studi terbaru menunjukkan bahwa kurkumin tidak hanya memainkan efek anti-kanker pada kanker paru-paru, dubur, dan payudara, terutama karena sifat antioksidan dan anti-inflamasinya, tetapi juga karena meningkatkan efektivitas radiasi dan kemoterapi, yang mengarah pada peningkatan kelangsungan hidup serta ekspresi protein anti-metastasis[130], dan mengurangi, pada saat yang sama, efek sampingnya[131-134]. Menariknya, kurkumin meningkatkan dan memicu aktivitas apoptosis terhadap sel tumor yang melibatkan jalur intrinsik dan ekstrinsik seperti yang dijelaskan sebelumnya [10,135]. Oleh karena itu, kombinasi kurkumin dengan kemoterapi atau radioterapi dapat meningkatkan sensitivitas sel kanker terhadap kemoterapi atau terapi radiasi dan meningkatkan efektivitas obat kemoterapi. Memang, ekspresi caspase-3 dan Bax meningkat, tetapi ekspresi Bcl-2 dan HIF1 dalam sel U251 menurun setelah pengobatan dengan 20 dan 30 M kurkumin. Ekspresi HIF-1 dan ENO1 dalam sel U251 menurun. Dalam kondisi hipoksia, HIF-1 dapat bertindak sebagai faktor transkripsi utama yang mengaktifkan enzim glikolitik yang disandikan termasuk ENO1.
Telah didokumentasikan dengan baik bahwa peningkatan glikolisis dianggap sebagai salah satu sifat metabolik GBM [136]. Enolase adalah enzim glikolitik yang penting dan ENO1 adalah isoform utamanya, yang diekspresikan dalam GBM. Dalam studi yang sama, ENO1 berkurang mengakibatkan penekanan pertumbuhan, migrasi, dan perkembangan invasif sel glioma. Kesimpulannya, ENO1 bisa menjadi gen target potensial untuk kurkumin dan mekanisme anti-kankernya dapat dikaitkan dengan jalur glikolitik dan apoptosis [137]. Temuan ini dikuatkan oleh data penelitian terbaru yang menunjukkan bahwa nanomicelle-curcumin dan curcumin dalam kombinasi dengan Erlotinib mengurangi viabilitas, migrasi, dan invasi sel glioblastoma manusia U87 in vitro. Baik invasi dan migrasi memainkan peran penting dalam metastasis kanker. Menariknya, ekspresi faktor terkait angiogenesis termasuk VEGF, HIF-1 , bFGF, dan Cox-2 sangat berkurang dalam sel glioblastoma manusia U87. Di sisi lain, kurkumin sendiri atau dalam kombinasi dengan Erlotinib meningkatkan ekspresi protein terkait autophagy (LC3-I, LC3-I, dan Beclin1) dan memodulasi ekspresi faktor pro-apoptosis Bax, Caspase 8, dan Bcl-2 dengan NF-kB pro-inflamasi (lihat Gambar 2) [138].
Selain itu, ekspresi gen yang terkait dengan jalur Wnt seperti cyclin D1, ZEB1, -catenin, dan Twist muncul secara signifikan diturunkan regulasinya oleh kurkumin [139]. Pada tingkat molekuler, kurkumin telah terbukti menekan proliferasi proliferasi sel GBM melalui jalur pensinyalan AKT/mTOR dan untuk meningkatkan ekspresi PTEN. Eksperimen in vitro dari penelitian ini secara konsisten mengkonfirmasi bahwa kurkumin menghambat migrasi dan invasi sel U251 yang berasal dari Glioblastoma multiforme ganas manusia dan merangsang apoptosis [140].
Berbagai pendekatan telah diusulkan untuk mencapai penetrasi BBB yang lebih baik dan pelepasan obat intracephalic yang efektif dan untuk menyediakan agen terapeutik yang efektif dan ditargetkan untuk GBM. Dalam pendekatan ini, kurkumin dienkapsulasi dalam dendrimer poliamidoamine (PAMAM) yang dimodifikasi permukaan dari generasi keempat. Khususnya, penggunaan kurkumin yang dienkapsulasi secara in vitro pada dosis terapeutik telah secara signifikan mengurangi viabilitas berbagai sel glioblastoma dari tiga spesies berbeda (U98, F98, dan GL261)[141]. Diketahui bahwa sel kanker membutuhkan keadaan oksidatif yang tinggi untuk mempertahankan pertumbuhan dan proliferasinya. Seperti dijelaskan di atas, kurkumin adalah senyawa nutraceutical yang dikenal dengan aktivitas anti-inflamasi dan antioksidannya dan oleh karena itu dapat menjadi kandidat potensial alternatif baru untuk pengobatan GBM yang menghancurkan. Namun, penilaian potensi kurkumin untuk GBM terkait dengan perawatan lain yang ada tetapi membutuhkan studi in vivo di masa depan dengan model hewan pengerat glioblastoma. Untuk meningkatkan penetrasi BBB dan untuk mencapai pengiriman obat yang efisien ke glioblastoma tikus, virus rabies glikoprotein polipeptida derivatif (RVG) peptida diarahkan, doxorubicin-loaded dan pengurangan sensitivitas kurkumin-dibantu nanomicelle (DOX/RVG-CSC) telah digunakan. Pengiriman kurkumin yang tepat merangsang repolarisasi keseluruhan mikroglia, yang pada gilirannya merangsang transformasi sel GBM dari keadaan imunosupresif M2 menjadi fenotipe M1 yang rentan [142]. Karena kompatibilitas lingkungan mikro yang unik dan afinitas untuk glioma intraserebral, kondroitin sulfat (CHS) digunakan sebagai segmen hidrofilik [143] dan terkonjugasi ke kurkumin melalui ikatan disulfida. Hal ini menyebabkan misel polimer cangkang inti yang dirakit sendiri secara spontan dalam air. DOX/RVG-CSC yang dimediasi RVG menembus BBB, mencapai daerah target sel tumor dan kemudian, setelah stimulasi oleh konsentrasi glutathione tinggi di GBM, melepaskan obat aktif [144]. Selain itu, temuan terbaru menunjukkan bahwa kurkumin dapat memainkan peran penting dalam menghilangkan sisa sel GMB dengan merangsang sistem kekebalan [145.146].
Peran kurkumin yang muncul dalam konteks GBM ini dieksplorasi melalui serangkaian studi mekanistik yang dilakukan pada model tikus GBM. Baru-baru ini, Baidoo et al. telah mempelajari penggunaan sistem kekebalan bawaan dalam pendekatan terapeutik untuk menghilangkan sel kanker. Mereka menemukan bahwa tumor membawa makrofag dan mikroglia di ceruknya, tetapi sebagian besar dalam keadaan M2 yang mempromosikan tumor di bawah kendali sitokin yang dilepaskan tumor. Temuan paling menonjol yang muncul dari hasil mereka adalah bahwa kurkumin menginduksi repolarisasi tumor terkait makrofag (TAM) menjadi oksida nitrat (NO) yang memproduksi fenotipe tumorisidal M1. Sakelar M2→M1 ini melibatkan penekanan STAT-3 yang dimediasi kurkumin serta induksi dan aktivasi STAT-1. Ini merekrut sel-sel pembunuh alami (NK) yang diaktifkan dan T sitotoksik (Tc) ke dalam tumor dan akibatnya menghilangkan sel-sel kanker dan sel-sel induk kanker. Dengan demikian, pendekatan ini dapat memberikan strategi umum untuk memerangi GBM, tetapi studi lebih lanjut diperlukan untuk lebih memahami implikasi dari berbagai faktor terkait jalur curcumin-antikanker [147-150]. Selain itu, ini telah membuka prospek uji klinis Fase I/II pada pasien GBM untuk menyelidiki efektivitas terapi berbasis kurkumin mereka untuk menginduksi repolarisasi TAM.
Singkatnya, kurkumin mampu memodulasi jalur terkait GBM. Misalnya, kurkumin menekan pertumbuhan tumor dengan memblokir jalur pemicu tumor NF-kB, PI3k/Akt/mamalia target rapamycin (PI3K/Akt/mTOR), Janus kinase/transduser sinyal, dan aktivator transkripsi (JAK/STAT3) dan mitogen jalur protein kinase teraktivasi, sedangkan gen penekan tumor utama (yaitu, p53 dan p21, dan caspase) diregulasi ke atas [151].
Konsisten dengan semua temuan in vitro kurkumin, efek in vivo bermanfaat lainnya dari kurkumin pada GBM telah dilaporkan (Tabel S1), termasuk penghambatan migrasi sel yang bergantung pada matriks metaloproteinase (MMP) dan proliferasi sel invasif, yang kemudian menyebabkan volume tumor berkurang dan, pada saat yang sama, waktu kelangsungan hidup lebih lama [137].
Semua efek kurkumin yang dibahas menunjukkan bahwa fungsi / aktivitas sel glioblastoma dimodulasi, dan perkembangannya tertunda (Gambar 1). Namun, profil genom tumor glioblastoma dan identifikasi target spesifik kurkumin untuk pengobatan GBM tetap penting dalam memahami mekanisme farmakologisnya dan, yang lebih penting, dapat memberikan dasar teoretis untuk penggunaan kurkumin yang rasional dalam praktik klinis. Penelitian lebih lanjut harus dipertimbangkan untuk laporan konklusif akhir tentang efek terapeutik kurkumin dalam praktik klinis sendiri atau dalam kombinasi dengan produk obat. Kemungkinan efek tidak langsung pada kesehatan otak dan pencegahan glioblastoma melalui sumbu usus-otak memerlukan penyelidikan lebih lanjut.
6. Kurkumin dan Epilepsi
Penyakit SSP saat ini merupakan masalah sosial dan individu yang utama. Secara khusus, bukti epidemiologi terbaru menunjukkan bahwa epilepsi merupakan kelompok penyakit yang semakin meluas di seluruh dunia. Untuk alasan ini, selama bertahun-tahun, semakin banyak obat dan terapi telah dikembangkan untuk melawan gejala dan frekuensi serangan epilepsi; namun, banyak dari obat ini telah terbukti efektif, tetapi mereka juga bertanggung jawab atas efek samping yang serius dan sering terjadi. Faktanya, banyak tanaman obat telah dipelajari baru-baru ini, dan kurkumin adalah salah satunya. Curcumin tampaknya memainkan peran dalam regulasi tingkat monoamine otak dan ini akan menunjukkan kemungkinan efek perlindungan pada kontrol kejang dan gangguan kognitif (terutama yang berkaitan dengan gangguan memori). Kurkumin telah terbukti memiliki efek antioksidan 10 kali lebih besar dari vitamin E dan merupakan alternatif yang valid untuk vitamin E itu sendiri [152].
Kurkumin memang mampu menghambat transkripsi yang dimediasi NF-kB, sitokin inflamasi, inducible iNOS, dan Cox-2 yang menghasilkan sifat antioksidan dan antiinflamasinya[153]. Sifat-sifat ini menunjukkan perannya dalam perlindungan saraf dan neuromodulasi dalam proses epileptogenesis yang dijelaskan (Tabel S1) (Gambar 1).
Tindakan anti-epilepsi kurkumin juga dapat dicapai melalui peningkatan regulasi gen anti-inflamasi seperti gen beta subunit reseptor Interleukin-10, dan ligan kemokin16(CXCL16), CXCL17, dan NCSTN[154]. Studi praklinis terbaru menunjukkan bahwa kurkumin mungkin memainkan peran yang berguna dalam epilepsi dan gangguan terkait tanpa efek samping atau efek samping [155,156]. Beberapa studi eksperimental berdasarkan model epilepsi yang diinduksi telah melaporkan efektivitas kurkumin dalam menunda atau sepenuhnya menghambat timbulnya kejang [157].
Curcumin juga telah disarankan untuk berperan dalam menentukan downregulasi beberapa protein saluran (CACNA1A dan GABRD), yang mengakibatkan penghambatan kejang yang diinduksi FeClg (Gambar 2). Pemberian kurkumin mereproduksi model manusia epilepsi pasca-trauma [158]. Kurkumin mikronisasi telah menunjukkan kemanjuran yang sebanding dengan obat anti-epilepsi valproat dalam menghambat kejang tonik-klonik pada model epilepsi yang diinduksi PTZ pada larva dan ikan zebra dewasa [159]. Dalam studi lain, evaluasi efek antiinflamasi dan antikonvulsan dari kurkumin setelah FeCl dosis tinggi; diberikan dengan diet dan diukur dalam bagian per juta (1500 ppm) menunjukkan kemanjuran unggul dalam menghambat kejang umum dibandingkan dengan dosis rendah (500 ppm) [160].
Dalam model uji kejut listrik tegangan tinggi pada tikus, kurkumin dengan dosis 100 mg/kg secara oral meningkatkan ambang kejang pada epilepsi akut dan kronis (selama 21 hari) [161]. Efek ini sebanding dengan pemberian fenitoin (25 mg/kg PO)[161]. Dalam penelitian ini, penurunan angka kematian ditemukan bahkan dengan pemberian kurkumin kronis, menjelaskan efek antikonvulsan dari zat ini. Studi pra-klinis lebih lanjut mengkonfirmasi efek antikonvulsan dan anti-inflamasinya. Selanjutnya, kurkumin ditemukan memainkan peran protektif dalam membalikkan berbagai perubahan stres oksidatif yang terkait dengan stimulasi pilocarpine [162]. Data ini juga dikonfirmasi oleh penelitian lain yang mengevaluasi dosis kurkumin antara 10 dan 300 mg/kg yang ditemukan berguna dalam mengurangi kejang akibat pilocarpine [163]
Curcumin juga telah menunjukkan efeknya pada keadaan epilepsi. Memang, studi oleh Gupta et al. [164], memprediksi pemberian kurkumin dalam kisaran dosis 50-200mg/kg sekitar 30 menit sebelum stimulasi dengan asam kainic. Penulis penelitian ini mengamati efek perlindungan kurkumin dalam meningkatkan latensi timbulnya kejang bila diberikan pada dosis antara 100 dan 200 mg/kg. Kelompok yang sama menunjukkan penurunan yang signifikan secara statistik dalam kejadian kejang [164]. Dosis yang lebih rendah tidak menunjukkan efektivitas klinis. Analisis otak hewan kemudian menunjukkan bagaimana kejang yang berlangsung lama meningkatkan kadar MDA dan menurunkan kadar glutathione. Efek ini hanya bisa dibalik dengan dosis 100 dan 200 mg/kg kurkumin. Dosis yang lebih rendah tidak berguna secara klinis [164].
Kurkumin juga telah terbukti efektif dalam mengurangi penurunan kognitif dan stres oksidatif yang disebabkan oleh penggunaan kronis obat antiepilepsi seperti fenobarbital dan karbamazepin yang banyak digunakan dalam praktik klinis [165].
Selain itu, kemanjuran kurkumin pada gangguan terkait epilepsi juga dikonfirmasi oleh penelitian dengan tikus Wistar jantan dalam metode yang diinduksi PTZ. Dalam penelitian ini, pemberian kurkumin 300 mg/kg menghasilkan peningkatan onset kejang yang diinduksi PTZ dan pengurangan stres oksidatif, dan penurunan penurunan kognitif [165].
Seperti diketahui, pemberian kronis beberapa obat antiepilepsi seperti carbamazepine dan fenobarbital dapat menyebabkan penurunan kognitif yang diyakini disebabkan oleh stres oksidatif. Curcumin, bila diberikan bersama dengan obat antiepilepsi ini telah terbukti membalikkan penurunan kognitif ini serta parameter stres oksidatif [165]
Studi lain, memeriksa kemanjuran kurkumin pada gangguan neurologis dan kejiwaan termasuk penurunan kognitif, menunjukkan bahwa tidak ada perkembangan penurunan kognitif yang diamati pada tikus yang mengonsumsi kurkumin dibandingkan dengan penurunan kognitif pada tikus yang mengonsumsi fenitoin [166]. Injeksi piperin bersama dengan kurkumin dapat meningkatkan bioavailabilitasnya dan membuat tindakan anti-epilepsinya menjadi lebih efektif [167].
Studi-studi ini sangat menggembirakan dan mewakili dasar untuk penelitian masa depan meskipun ada batasan baik mengenai sulitnya reproduktifitas jaringan epileptogenik manusia mulai dari model berbasis eksperimental dan kesulitan dalam mengubah dosis yang diberikan dalam model eksperimental menjadi dosis untuk manusia.
7. Kesimpulan
Senyawa alami Curcumin memiliki sifat anti-oksidan, dan anti-inflamasi, dan memiliki efek perlindungan dengan bekerja pada berbagai jalur seluler. Dalam ulasan ini, kami memfokuskan perhatian kami pada efek terapeutik kurkumin pada gangguan neurodegeneratif seperti AD, PD, MS, glioblastoma, dan epilepsi dengan memodulasi berbagai jalur molekuler dalam sel otak (lihat Tabel S1 dan Gambar 2). Vesikel ekstraseluler atau nanovesikel dapat meningkatkan kelarutan dan bioavailabilitas kurkumin di otak, tetapi sampai sekarang, penerapan cara baru pengiriman kurkumin ini belum sepenuhnya diselidiki pada penyakit neurodegeneratif. Oleh karena itu, lebih banyak penelitian yang menggunakan biomolekul terapeutik ini dapat memberikan hasil positif untuk perlindungan saraf. Studi baru ini dapat difokuskan pada (1) meningkatkan sistem penghantaran obat untuk meningkatkan bioavailabilitas dan permeabilitas BBB kurkumin; (2) studi klinis lebih lanjut untuk menetapkan dosis yang lebih efektif dari biomolekul yang mengangkut kurkumin untuk pengobatan gangguan neurodegeneratif; (3 ) menyelidiki jalur pensinyalan yang digunakan biomolekul terapeutik untuk menginduksi perlindungan saraf. Hasil yang dijelaskan dalam ulasan ini menggembirakan tetapi penelitian lebih lanjut diperlukan untuk mengoptimalkan penggunaan kurkumin dalam pencegahan dan pengobatan penyakit neurodegeneratif.
Artikel ini disarikan dari Molecules 2022, 27, 236. https://doi.org/10.3390/molecules27010236 https://www.mdpi.com/journal/molecules
