Tren Terbaru dalam Aplikasi Terapi Bahan Pemurnian Darah Yang Direkayasa Untuk Penyakit Ginjal
Jul 10, 2023
Abstrak
Pemurnian darah adalah metode yang umum digunakan untuk menghilangkan kelebihan sisa metabolisme dalam darah dalam terapi penggantian ginjal. Penghapusan racun yang cukup dari darah dapat mengurangi komplikasi dan meningkatkan kelangsungan hidup seumur hidup pada pasien dialisis. Namun, bahan pemurnian darah biologis saat ini dalam praktik klinis tidak ideal, di mana ada kebutuhan yang tidak terpenuhi untuk memproduksi bahan baru yang memiliki biokompatibilitas yang lebih baik, mengurangi toksisitas, dan, khususnya, tingkat pembersihan toksin yang lebih efisien dan biaya produksi yang lebih rendah. Mengingat hal ini, ulasan ini telah dengan hati-hati merangkum bahan biomedis struktural berbeda yang direkayasa yang baru dikembangkan untuk pemurnian darah dalam hal jenis dan karakteristik struktur bahan pemurnian darah, proses produksi, serta sifat atau mekanisme adsorpsi kimia antar muka. Studi ini dapat memberikan referensi berharga untuk membuat perangkat pemurnian yang ramah pengguna yang lebih cocok untuk aplikasi pemurnian darah klinis pada pasien dialisis.
Kata kunci
Pemurnian darah, Terapi penggantian ginjal, Rekayasa biomaterial, Adsorben, Membran komposit polimer.

Klik di sini untuk mengetahui apa itu Cistanche
Perkenalan
Racun uremik sering menumpuk pada pasien dengan fungsi ginjal yang terganggu, termasuk penyakit ginjal stadium akhir (ESKD). Hal ini menyebabkan penyakit serius, dengan terapi pengganti ginjal sebagai satu-satunya solusi untuk bertahan hidup. Banyak penelitian menemukan penurunan angka kematian dan laporan kualitas hidup yang lebih baik di antara penerima ginjal; namun, permintaan melebihi ketersediaan, di mana hanya 25 persen pasien ESKD yang menerima ginjal [1]. Di seluruh dunia, diperkirakan sekitar 280 pasien per juta menjalani perawatan hemodialisis reguler atau dialisis peritoneal, sedangkan kelangsungan hidup lima tahun orang-orang ini antara 13 persen dan 60 persen lebih rendah daripada orang pada populasi umum pada usia yang sama [1–3] . Karena penuaan populasi, serta peningkatan prevalensi diabetes dan hipertensi, kejadian ESKD diperkirakan akan meningkat selama beberapa dekade mendatang [4]. Terlebih lagi, akumulasi zat terlarut retensi uremik pada konsentrasi tinggi dikaitkan dengan hasil yang merugikan pada pasien dialisis, termasuk kematian yang tinggi dan kualitas hidup yang berhubungan dengan kesehatan secara keseluruhan rendah [5-8].

Kreatinin adalah toksin uremik utama, dan kumpulannya dalam darah menyebabkan serangkaian gejala toksik yang dapat mengurangi fungsi ginjal dan akibatnya mempercepat penurunan ginjal [9]. Toksin uremik terikat protein (PBUT) adalah molekul kecil yang terutama mengikat protein transpor, albumin serum manusia dalam darah [10], dan terlibat dalam pembentukan spesies oksigen reaktif (ROS) [11]. Sementara PBUT secara khusus diketahui terkait dengan efek samping/toksik, termasuk penyakit kardiovaskular [12-14], perkembangan gagal ginjal [15], dan kematian [5], mekanisme pembersihan ginjal dan perannya dalam patofisiologi uremik masih belum jelas [16 ]. Biasanya, p-cresyl sulfate (PCS), indoxyl sulfate (IS), 3- Carboxy-4-methyl-5-propyl-2-furanpropionic acid (CMPF), dan indole{{14 }}asam asetat (IAA) adalah biomarker uremia yang paling diskriminatif dan dianggap sebagai prototipe toksin uremik yang terikat protein yang dapat mengikat lebih dari 90 persen protein plasma. Keempat PBUT tersebut memiliki cincin aromatik dan gugus fungsi ionik serta dapat membentuk ikatan non kovalen, seperti gaya Van der Waals dan ikatan hidrogen, serta interaksi elektrostatik dan hidrofobik [16]. Dengan PBUT, ada keseimbangan antara bentuk yang terikat protein dan yang tidak terikat dalam sekresi dan sirkulasinya, dan pembersihan inheren dari racun yang tidak terikat sangat tergantung pada sekresi tubular ginjal melalui transporter anion organik basolateral (OAT) spesifik. Jalur produksi dan pembersihan protein PBUT ditunjukkan pada Gambar 1 [16]. Toksisitas uremik terkait dengan disfungsi endotel dan disfungsi imun, yang menyebabkan peradangan dan aktivasi efektor imun bawaan melalui induksi keadaan pro-inflamasi yang melibatkan reseptor Toll-like dan sitokin inflamasi [14]. Dengan demikian, penghilangan toksin yang cukup dari darah meningkatkan kemanjuran dialisis, yang pada gilirannya meningkatkan tingkat kelangsungan hidup pada pasien ESKD. Mekanisme dasar hemodialisis ditunjukkan pada Gambar. 2. Namun, eliminasi kelebihan metabolit menggunakan terapi pengganti ginjal ekstrakorporeal konvensional melalui membran polimer berpori semipermeabel saat ini belum efektif dalam penggunaan klinis. Secara khusus, PBUT sulit untuk dihilangkan melalui hemodialisis karena masing-masing molekul ini memiliki bagian aromatik dan gugus fungsi ionik yang memungkinkan untuk berikatan dengan beberapa situs adsorpsi pada albumin serum manusia [17-20]. Telah dilaporkan bahwa rasio pengurangan PCS dan IS kurang dari 35 persen dihilangkan selama hemodialisis high-flux [11].

Mengingat hemodialisis sebagai pengobatan ekstrakorporeal untuk mempertahankan hidup gagal ginjal, dimana sejumlah besar pasien ESKD memerlukan dialisis jangka panjang, maka perlu disiapkan bahan dengan metode fabrikasi yang sederhana dan murah. Meskipun sifat efisiensi dan selektivitas membran dialisis telah meningkat dalam beberapa dekade terakhir, perawatan dialisis tradisional tetap menjadi proses yang tidak nyaman, memakan waktu, dan mahal [21-23]. Baru-baru ini, beberapa bahan pemurnian darah biomedis telah dikembangkan untuk meningkatkan tingkat pembuangan toksin, beberapa di antaranya juga memiliki karakteristik seperti toksisitas yang lebih rendah dan biaya produksi yang rendah. Pada artikel ini, kami meringkas hasil ini berdasarkan kategori untuk menawarkan informasi untuk penelitian lebih lanjut tentang bahan dialisis dengan sifat yang lebih baik.
Cistanche tubulosa
Bahan biomedis untuk menghilangkan racun-Adsorben
Karbon aktif (AC) dan zeolit adalah dua adsorben yang umum digunakan dalam pemurnian untuk meningkatkan sifat ultrafiltrasi. AC memiliki rekam jejak panjang dalam sistem detoksifikasi sebagai partikel adsorptif karena dapat menyerap berbagai zat terlarut [24-26]. Ini memiliki ukuran pori yang besar tetapi tidak selektif ukuran. AC menunjukkan kapasitas adsorpsi yang tinggi untuk racun uremik, tetapi juga secara bersamaan menghilangkan molekul berguna lainnya. Mengurangi diameter partikel adalah cara yang layak untuk menaikkan luas permukaan luar dan dengan demikian meningkatkan situs aktif yang dapat diakses dan pengikatan cepat. Namun, penerapan suspensi dengan karbon aktif bubuk memerlukan filter membran untuk menjaga agar sorben tetap tersuspensi dan mencegah kontak partikel dengan darah, yang biasanya membatasi jumlah volume sorben dan pasti menghasilkan konsentrasi sorben yang lebih rendah [27]. Dibandingkan dengan AC, tabung nano karbon (CNT) memiliki luas permukaan yang lebih tinggi, rasio aspek yang lebih besar, dan kinerja adsorpsi yang lebih baik untuk racun uremik, sehingga dianggap sebagai bahan yang lebih cocok untuk desain membran pemurnian darah yang sangat efisien [28-30] . Liu dkk. manik-manik adsorben karbon berpori (NPCA) yang mengandung nitrogen buatan yang memiliki keunggulan tambahan dalam hal pembersihan PBUT yang aman dan efektif, dan memiliki hemokompatibilitas in vitro yang memuaskan. NPCA disiapkan melalui pirolisis manik-manik kopolimer akrilonitril/divinilbenzena berpori yang terhubung silang (Gbr. 3a) [31]. Manik-manik NPCA menunjukkan tingkat adsorpsi PBUT yang lebih tinggi (IS, PCS, dan IAA; 45 persen , 44 persen , dan 95 persen ) dan kinerja adsorpsi yang setara terhadap racun berat molekul menengah (PTH dan IL-6) dalam plasma manusia dibandingkan dengan HA- 130/MG-150 (penyerap komersial yang digunakan di klinik). Mekanisme penghilangan PBUT dari NPCA dianggap berasal dari persaingan antara gugus fungsi nitrogen pada NPCA dan protein untuk pengikatan PBUT melalui interaksi elektrostatik, dan tidak memiliki hubungan yang kuat dengan struktur pori (Gbr. 3b) [31].

Tidak seperti AC amorf, adsorben kristal dapat memungkinkan karakterisasi struktural langsung yang dapat membantu dalam memahami interaksi antara adsorben dan toksin, yang sangat penting untuk desain bahan adsorben yang unggul. Zeolit adalah salah satu inosilikat tawas terbaik yang diaplikasikan untuk banyak saringan molekuler dan memiliki ketahanan yang tinggi dalam proses kimia dan termal [32]. Zeolit tidak beracun, stabil dalam larutan berair, dan tidak terdegradasi dalam kondisi fisiologis. Selain itu, berbagai jenis zeolit mikro memiliki sistem saluran dalam ukuran berbeda yang dapat secara selektif menyerap beberapa racun uremik [33-36], dan dapat ditemukan secara alami atau diproduksi secara sintetis. Fitur-fitur ini menjadikan zeolit sebagai bahan potensial untuk aplikasi ginjal buatan. Ukuran dan bentuk partikel zeolit penting untuk kemampuan serapan kreatinin saat dimasukkan ke dalam membran [37, 38]. Misalnya, mikropartikel memiliki kinerja yang lebih baik pada adsorpsi kreatinin daripada nanopartikel. Sementara itu, dibandingkan dengan nanopartikel batang, nanopartikel sferis adalah pilihan yang lebih baik untuk dimasukkan ke dalam serat polimer elektrospinning untuk meningkatkan tingkat pembersihan kreatinin [37].

Suplemen cistanche
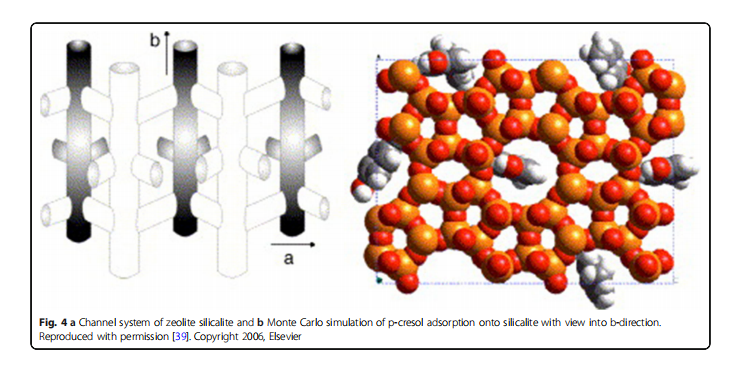
Wernet et al. menyelidiki penghapusan racun uremik menggunakan zeolit dari tipe struktural yang berbeda [33]. Mereka menyimpulkan bahwa sifat adsorpsi zeolit tidak hanya tergantung pada ukuran saluran tetapi juga interaksi antara adsorbat dan kisi zeolit. Lebih khusus lagi, zeolit silikalit (MFI) menunjukkan adsorpsi yang kuat dari p-kresol (sekitar 60 persen p-kresol dalam larutan dengan konsentrasi yang dekat dengan yang ditemukan pada pasien uremik), yang dikaitkan dengan efek pembukaan/ukuran saluran dan interaksi ikatan hidrogen. Mekanisme adsorpsi ditunjukkan pada Gambar. 4 (misalnya, adsorpsi p-kresol ke silikalit zeolit) [39]. MFI memiliki waktu kesetimbangan yang lebih singkat dan tingkat adsorpsi p-kresol yang lebih tinggi daripada membran berbasis selulosa dan membran sintetik [39]. Selain itu, dimungkinkan untuk secara selektif menghilangkan 75 persen kreatinin dalam larutan oleh mordenit asam (MOR), yang pada dasarnya disebabkan oleh interaksi elektrostatik antara gugus Ofungsional dan situs Brønstedt yang ada di pori-pori MOR [33]. Adsorpsi asam urat yang tinggi pada ion-exchanged stilbites (STIs), seperti Ca-STI, K-STI, dan Na-STI, dapat dikaitkan dengan interaksi elektrostatik antara kation dan atom negatif dari ikatan molekul polar. Namun, terdapat cara potensial untuk meningkatkan sifat adsorpsi IMS melalui pembentukan interaksi kovalen yang kuat menggunakan kation dengan afinitas terhadap toksin uremik [33]. Berge-Lefranc et al. menunjukkan lebih lanjut bahwa MFI silika murni memiliki kapasitas yang lebih baik untuk menghilangkan p-kresol daripada MFI aluminosilikat (Si/Al=30, mengkompensasi muatan dengan H plus , Na plus , K plus , dan Mg2 plus ) [34]. Mereka menemukan bahwa dibandingkan dengan dalam larutan, afinitas p-kresol untuk zeolit umumnya berkurang dalam serum manusia (diperoleh dari pasien dialisis) karena protein menyumbat sistem pori. Dengan demikian, zeolit hanya dapat digunakan dalam ultra-filtrat tanpa kontak langsung dengan albumin serum [35].
Kerangka logam-organik (MOF) adalah salah satu jenis bahan hibrid baru, yang memiliki stabilitas termal dan kimia yang tinggi dan telah terbukti lebih efektif daripada bahan AC atau silika mesopori, karena porositasnya yang sangat tinggi dan situs aktifnya [40–42] . Dan luas permukaan BET dan diameter kandang MOF sebelumnya telah dihipotesiskan sebagai parameter kunci dalam kapasitas adsorpsi MOFs [43]. MOF terbuat dari ion logam dan penghubung organik melalui batas koordinat untuk membentuk struktur 1D, 2D, atau 3D [40, 44]. MOF dengan cepat mendapatkan daya tarik dalam aplikasi untuk, namun tidak terbatas pada, pemisahan senyawa bioaktif [45], pemurnian air [46, 47], pemberian obat [48], dan pemisahan gas [49]. Namun demikian, penggunaan MOFs dalam aplikasi ginjal buatan masih dalam tahap awal. Selain itu, MOF memiliki daya tahan yang luar biasa, dan, tidak seperti kelas bahan kristal lainnya, MOF dapat dipelajari secara sistematis dan dimasukkan ke dalam sejumlah fungsi [50].

ekstrak Cistacnhe
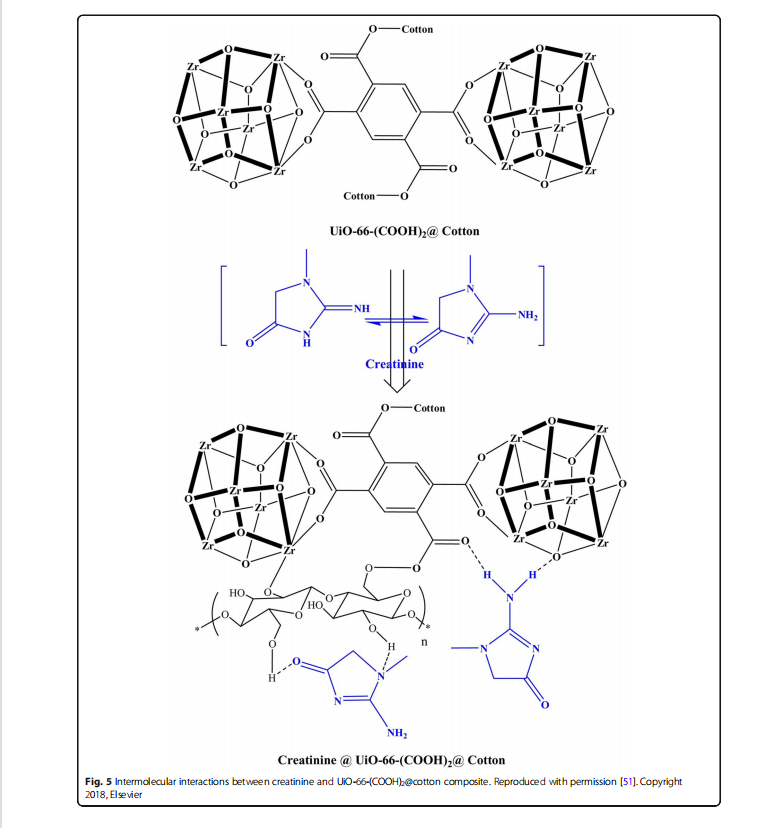
Abdelhameed dkk. melaporkan satu jenis MOF berbasis Zr yang tumbuh dalam komposit kain katun, yang dapat diregenerasi dengan sonikasi menggunakan metanol, sementara efisiensinya dalam menghilangkan kreatinin hanya berkurang sebesar 16 persen (98 persen vs. 82 persen) setelah tiga siklus generasi [ 51]. Komposit in-situ ini langsung diformat tanpa membuat UiO-66-(COOH)2 dan menggunakan 1,2,4,5- benzena tetrakarboksilat dianhidrida, zirkonium tetraklorida, dan kain katun [51]. Komposit kain UiO-66- (COOH)2@kapas menyerap kreatinin melalui interaksi lemah antara situs ikatan MOF dan gugus fungsi kreatinin. Mekanisme reaksi ditunjukkan pada Gambar. 5. Selain itu, telah dilaporkan bahwa memfungsikan UiO-66 dengan substituen isovalen seperti -NH2, -OH, dan SO2H sangat meningkatkan kapasitas adsorpsi dengan mengubah sifat elektronik MOF [52 , 53]. Klaudia dkk. mensintesis rangkaian bahan UiO-66 yang bervariasi dengan kandungan akhir gugus amino dengan mengubah rasio H2BDC/H2BDC-NH2 dan menambahkan asam klorida (HCl) selama sintesis termodulasi [52]. Mereka memastikan bahwa UiO-66-NH2(75 persen ) (dengan 75 persen mol gugus -amino) dan UiO-66-NH2(75 persen )12,5 persen HCl memiliki kapasitas adsorpsi yang lebih baik untuk asam hipurat dan {{39} }asam indoleasetat, mengungkapkan kapasitas adsorpsi analog ke NU-1000, sedangkan UiO-66-NH2 yang telah disiapkan masih belum menunjukkan efek sitotoksik.
Kato et al. mengamati perilaku adsorpsi kresil sulfat dalam serangkaian MOF berbasis Zr6-dengan berbagai topologi, konektivitas, dan struktur penaut, termasuk UiO-66, UiO-67, UiO-NDC, PCN{ {4}}OH, NU-901, NU-1000, NU-1010, NU-1200 dan MOF-808 [50]. MOF berbasis zirkonium ini memiliki luas permukaan dan ukuran pori yang sebanding. Diantaranya, NU-1000 menunjukkan efisiensi penghilangan toksin tertinggi, di mana lebih dari 70 persen p-cresyl sulfate, 98 persen indoxyl sulfate, dan asam hipurat dalam larutan, serta sekitar 93 persen p-cresyl sulfate , dapat dihilangkan dari albumin serum manusia. Hal ini dapat dikaitkan dengan situs adsorpsi yang sangat hidrofobik yang diapit oleh dua penghubung pirena, serta ikatan hidrogen antara gugus hidroksil pada nodus Zr6 dan gugus fungsi ionik dari adsorbat [50]. Dua situs p-cresyl sulfate pada NU-1000 digambarkan pada Gambar. 6. Kedua lokasi ini kira-kira memiliki hunian yang sama, di mana interaksi elektrostatik dengan gugus hidroksil pada simpul Zr6 dan interaksi π-π dengan penghubung berbasis pirena merupakan faktor penting dalam kemampuan adsorpsi. Namun, Cuchiaro et al. menunjukkan bahwa penerapan NU-1000 terbatas karena tidak tersedia secara komersial, dan besi merupakan alternatif yang diinginkan untuk zirkonium [43]. Cuchiaro et al. mensintesis MIL-100(Fe) dan MOF-808, keduanya memiliki penghubung organik yang sama dengan MOF-808 tetapi MIL-100 (Fe) kurang beracun karena zat besinya simpul logam berbasis [43]. Mereka menemukan serapan p-cresyl sulfate untuk MIL-100(Fe) tiga kali lebih besar daripada MOF-808, yang kurang berkorelasi dengan luas permukaan BET, ukuran jendela pori, diameter sangkar, dan jumlah karbon aromatik dalam penghubung organik, menunjukkan bahwa interaksi logam-besi dapat terjadi lebih baik dalam MIL-100(Fe) daripada MOF-808.

Terinspirasi oleh kemampuan pemurnian diri ginjal, Chen et al. mengusulkan adsorben baru yang disebut partikel opal polimer imprinted molekul (MIPIOPs) [54]. Di sini, lingkungan fluidik digunakan untuk menyelesaikan dilema kontak yang tidak mencukupi antara bahan penyerap dan molekul target. MIPIOP tertanam dalam chip mikrofluida dengan mixer herringbone dan skalanya dapat dengan mudah diperkuat untuk mengakomodasi sejumlah besar MIPIOP untuk pemurnian. Selain itu, saluran herringbone dapat menghasilkan adveksi cairan yang kacau, dan karenanya meningkatkan efisiensi pencampuran dan adsorpsi antara biomolekul target dan MIPIOP. MIPIOP dibuat melalui proses pencetakan kombinasi (Gbr. 7). Manik-manik kristal koloid silika (SCCB) pertama kali dibuat, dan kemudian nanopartikel silika pada permukaan SCCB mengadsorpsi lisozim melalui interaksi elektrostatik. Langkah berikut mengisi ruang kosong antara nanopartikel silika dari SCCB yang difungsikan lisozim menggunakan campuran prekuel gelatin metakrilat (GelMA), polietilen glikol diakrilat (PEGDA), urea, dan kreatinin. Kemudian, SCCB dan molekul cetakan, termasuk lisozim, urea, dan kreatinin, dikeluarkan dari polimer pra-gel. MIPIOP yang dihasilkan memiliki beberapa situs pengikatan molekuler untuk lisozim di permukaan, sedangkan urea dan kreatinin berada di bagian dalam. MIPIOPs memiliki fitur unik dan menampilkan kompatibilitas darah yang baik, dan telah dibuktikan bahwa kapasitas adsorpsinya dipertahankan secara stabil setelah digunakan kembali sebanyak lima kali [54]. Selain itu, karena struktur berpori 3D yang sangat tertata, mereka diberikan sifat celah pita fotonik yang memungkinkan untuk memantau dan melaporkan sendiri keadaan adsorpsi.

Cyclodextrins (CDs) adalah oligosakarida siklik berbentuk toroidal yang terdiri dari 6-8 unit D-glukosa ( , , ), dengan bagian luar hidrofilik dan rongga bagian dalam yang relatif hidrofobik, yang dapat membungkus tamu atau makromolekul lipofilik dengan berat molekul rendah yang berbeda [55 , 56]. -CD berbentuk cangkir terdiri dari 7 unit glukosa dan paling sering digunakan karena pengenalannya yang sensitif terhadap beragam molekul hidrofobik dengan membentuk kompleks tamu CD. Li dkk. mengusulkan untuk pertama kalinya bahwa menambahkan poli- -siklodekstrin (PCD) berikatan silang ke dalam dialisat dialisis eksterior untuk meningkatkan efisiensi transfer massa indoksil sulfat (IS) (Gbr. 8a) [56]. PCD disintesis oleh ikatan silang antara -CD dan epiklorohidrin (ECH). -CD terlebih dahulu dilarutkan dalam larutan NaOH, kemudian ECH ditambahkan ke dalam campuran, yang selanjutnya diaduk pada suhu 30 derajat selama 2 jam. Menurut penelitian awal, kapasitas pengikatan maksimum PCD untuk IS adalah sekitar 45 mg g-1 dan peningkatan tingkat pelepasan sebesar 21 persen telah dicapai dalam percobaan dialisis simulasi dengan diperkenalkannya PCD. Mekanisme pengikatan IS ke PCD mungkin karena cincin indole IS diakomodasi dalam rongga -CD melalui interaksi hidrofobik dan ikatan hidrogen [56]. Strategi baru ini tidak memberikan dampak negatif pada membran dialisis dan aman untuk aplikasi klinis karena PCD telah terbukti dengan tingkat hemolisis yang rendah dan tidak dapat melintasi membran untuk kontak dengan darah (diameter hidrodinamik polimer adalah 9nm). Li dkk. lebih jauh membandingkan kapasitas adsorpsi poli- -siklodekstrin, poli- - siklodekstrin dan poli- -siklodekstrin, dan poli- - siklodekstrin berkinerja paling baik dengan kapasitas pengikatan kresol sulfat (PCS) maksimum (263 mg g-1) [57]. Mereka menemukan bahwa pembersihan PCS dalam plasma melalui mode sekali lewat (Gbr. 8b) lebih efektif daripada mode daur ulang (96 persen vs. 43 persen ), yang dikaitkan dengan perbedaan konsentrasi PCS antara plasma dan peningkatan dialisat dengan penghilangan PCS. Dan PCS (96 persen ), asam hipurat (98 persen ), dan asam quinolinic (97 persen ) dalam plasma dihilangkan dalam sistem dialisat tambahan PCD, selanjutnya menjelaskan sifat penghilangan PBUT spektrum luas dari PCD [57].

MXena adalah keluarga karbida dua dimensi dan nitrida logam transisi dengan struktur umum Mn plus 1XnTx (M adalah logam transisi awal, seperti Ti, V, Nb, dll.; n plus 1=1-3; X adalah C dan/atau N; Tx mewakili terminasi permukaan, seperti O, OH, F, dan/atau Cl) [58, 59]. MXene memiliki kombinasi sifat yang unik, termasuk hidrofilik karena permukaan yang difungsikan dan larutan koloid yang stabil dalam air karena potensi zeta negatif yang tinggi, dan telah banyak diteliti di bidang biomedis dalam beberapa tahun terakhir [58]. Ti3C2Tx adalah anggota MXenes yang dilaporkan dan paling banyak dipelajari pertama kali dan diketahui dapat menyerap urea secara efisien. Dan Ti3C2Tx telah terbukti memiliki biokompatibilitas yang relatif tinggi dan biotoksisitas yang rendah pada penelitian in vivo sebelumnya [60]. Dalam karya Zhao et al., Ti3C2Tx (Ti3C2- F, Ti3C2-O, Ti3C2-OH, dibuat dari prekursor Ti3AlC2 menggunakan asam fluorida 10 persen berat) digunakan sebagai adsorben dalam larutan berair, dan itu melakukan tingkat adsorpsi cepat dan kapasitas adsorpsi yang lebih tinggi terhadap kreatinin dan asam urat dibandingkan dengan karbon aktif konvensional [59]. Afinitas tinggi antara Ti3C2Tx dan kreatinin dalam proses adsorpsi dianggap berasal dari terminasi permukaan hidrofilik Ti3C2Tx dan difusi intrapartikel kreatinin antara lapisan Ti3C2Tx. Namun, dalam proses adsorpsi asam urat, afinitas tinggi mungkin berasal dari ikatan hidrogen (TiOH…N) dan interaksi van der Waals. Terlebih lagi, mengingat bahwa Ti3C2Tx secara efektif menyerap urea, kreatin, dan asam urat, serta kation elektrolit (K plus , Ca2 plus , Mg2 plus , dll.) juga dapat menempati situs aktif Ti3C2Tx, Zhao et al. mengusulkan bahwa Ti3C2Tx memiliki potensi untuk digunakan sebagai sorben yang efisien untuk regenerasi dialisat. Baru-baru ini, Wang et al. menyiapkan nanosheet Ti3C2Tx dengan mengelupaskan Ti3C2Tx yang tergores dalam air terdeaerasi dengan ultrasonikasi dan menemukan untuk pertama kalinya bahwa kemampuan penyingkiran Ti3C2Tx yang sangat tinggi terhadap IL-6, yang menunjukkan 13,4 kali dibandingkan dengan karbon aktif tradisional dan laju penyisihan yang jauh lebih cepat [ 61]. Mekanisme utama adsorpsi adalah pembentukan ikatan hidrogen antara MXene dan IL-6 (TI-X … HNC=O), serta imobilisasi IL-6 pada permukaan Nanosheet MXene.

Kapsul cistanche
Kesimpulan
Sebagai kesimpulan, kami merangkum biomaterial baru untuk pemurnian darah yang telah dilaporkan dalam beberapa tahun terakhir. Biomaterial ini secara kasar dibagi menjadi 3 kategori, termasuk adsorben, membran komposit polimer, dan nanomaterial. Adsorben, seperti zeolit, karbon aktif, dan CTN, umumnya digabungkan di dalam bahan polimer untuk meningkatkan kapasitas ultrafiltrasi. Ketika partikel adsorptif tersebar di seluruh matriks polimer, efisiensi penghilangan racun uremik dapat ditingkatkan dengan menggabungkan adsorpsi dan difusi zat terlarut retensi uremik, yang telah divalidasi dalam penelitian terkait dengan membran komposit MMM dan f-CNT/PES. Karena luas permukaan dan porositas yang besar, nanomaterial dan MOF sama-sama menunjukkan kemampuan adsorpsi yang menguntungkan. Selain itu, pembuatan nanofiber polimer hemat biaya dan MOF berbasis Zr memiliki kemampuan untuk digunakan kembali dengan baik.
Permeasi adalah properti vital dari membran yang digunakan untuk hemodiafiltrasi karena tingkat pembuangan racun yang rendah membuat pasien menderita melalui dialisis jangka panjang yang menghabiskan biaya lebih tinggi. Ketika konsentrasi toksin bebas pada sisi dialisat dipertahankan pada tingkat rendah, terdapat kekuatan pendorong difusi yang terus menerus sepanjang panjang hemodialyzer, terutama untuk PBUT [130, 131]. Seperti disebutkan dalam makalah ini, bahan dengan luas permukaan dan porositas yang besar merupakan kandidat yang menjanjikan untuk memproduksi membran hemodialisis. Menanamkan partikel adsorptif dalam matriks membran polimer juga merupakan metode yang efektif untuk mencapai tingkat pembersihan racun uremik yang lebih efisien, karena pemeliharaan perbedaan konsentrasi. Ada juga beberapa adsorben yang kemampuan adsorpsinya kurang berkorelasi dengan struktur pori, seperti butiran NPCA. Oleh karena itu, sangat penting untuk menganalisis struktur molekul masing-masing adsorben dan toksin uremik, serta interaksi di dalamnya.
Dialisis adalah pengobatan jangka panjang dan mempertahankan hidup untuk pasien ESKD, dan hampir 500 L air keran diperlukan untuk mendapatkan air dialisis murni untuk satu sesi hemodialisis, yang tinggi baik dalam biaya maupun konsumsi energi [132]. Oleh karena itu, metode pembuatan bahan dialisis yang sederhana dan murah sangat penting untuk aplikasi klinisnya. Selain itu, biofilm mikrobiologi yang disebabkan oleh genangan air akan tetap terbentuk ketika sistem tubing tidak memadai atau perawatan mesin tidak tepat [133, 134]. Pertumbuhan bakteri dan lisis dalam sistem pemurnian air, dan dengan demikian pirogen dapat ditransfer ke dalam darah pasien, yang menyebabkan status mikro-inflamasi, menyebabkan efek samping kardiovaskular atau efek samping akut, seperti demam dan kram otot [133–139] . Beberapa sistem sorben untuk penghilangan endotoksin (misalnya, lipopolisakarida) telah dilaporkan, seperti fungsional partikel nano [140], karbon aktif [26, 141], penambahan kopolimer PS-poli (etilen glikol) (PS-PEG) dan pemutih. sterilisasi [133]. Selain itu, MMM menawarkan penghilangan endotoksin yang unggul dan bertindak sebagai penghalang keamanan yang menghindari respons inflamasi tanpa penurunan pembuangan racun uremik [71]. Secara umum, biomaterial dengan ultrafiltrasi jangka panjang dan tinggi, biokompatibilitas yang menguntungkan, dan metode pembuatan yang hemat biaya merupakan kandidat ideal untuk pemurnian darah. Bahkan jika biomaterial baru yang disebutkan dalam ulasan ini telah meningkatkan kapasitas adsorpsi dan biokompatibilitas, masih banyak pekerjaan yang harus dilakukan yang berfokus pada modifikasi bahan sehingga cocok untuk aplikasi klinis.
Referensi
1. Webster AC, Nagler EV, Morton RL, Masson P. Penyakit ginjal kronis. Lanset. 2017;389(10075):1238–52.
2. Tonelli M, Wiebe N, Knoll G, Bello A, Browne S, Jadhav D, dkk. Tinjauan sistematis: transplantasi ginjal dibandingkan dengan dialisis dalam hasil yang relevan secara klinis. Am J Transplantasi. 2011;11(10):2093–109.
3. Nordio M, Limido A, Maggiore U, Nichelatti M, Postorino M, Quintaliani G. Kelangsungan hidup pada pasien yang dirawat dengan dialisis jangka panjang dibandingkan dengan populasi umum. Am J Kidney Dis. 2012;59(6):819–28.
4. Liyanage T, Ninomiya T, Jha V, Neal B, Patrice HM, Okpechi I, dkk. Akses di seluruh dunia untuk pengobatan penyakit ginjal stadium akhir: tinjauan sistematis. Lanset. 2015;385(9981):1975–82.
5. Bammens B, Evenepoel P, Keuleers H, Verbeke K, Vanrenterghem Y. Konsentrasi serum bebas dari zat terlarut retensi terikat protein p-cresol memprediksi kematian pada pasien hemodialisis. Ginjal Int. 2006;69(6):1081–7.
6. Cheung AK, Rocco MV, Yan G, Leypoldt JK, Levin NW, Greene T, dkk. Kadar mikroglobulin beta-2 serum memprediksi kematian pada pasien dialisis: hasil penelitian di rumah. J Am Soc Nephrol. 2006;17(2):546–55.
7. Ito S, Osaka M, Higuchi Y, Nishijima F, Ishii H, Yoshida M. Indoxyl sulfate menginduksi interaksi leukosit-endotel melalui pengaturan seleksi. J Biol Kimia. 2010;285(50):38869–75.
8. Duranton F, Cohen G, De Smet R, Rodriguez M, Jankowski J, Vanholder R, dkk. Konsentrasi normal dan patologis toksin uremik. J Am Soc Nephrol. 2012;23(7):1258–70.
9. Panasyuk-Delaney T, Mirsky VM, Wolfbeis OS. Sensor kreatinin kapasitif berdasarkan polimer yang dicetak secara molekuler yang difoto. Elektroanalisis. 2002;14(3):221–4.
10. Vanholder R, De Smet R, Glorieux G, Argiles A, Baurmeister U, Brunet P, dkk. Ulasan tentang racun uremik: klasifikasi, konsentrasi, dan variabilitas antarindividu. Ginjal Int. 2003;63(5):1934–43.
11. Itoh Y, Ezawa A, Kikuchi K, Tsuruta Y, Niwa T. Racun uremik terikat protein pada pasien hemodialisis diukur dengan kromatografi cair/spektrometri massa tandem dan pengaruhnya terhadap produksi ros endotel. Kimia Bioanal Anal. 2012;403(7):1841–50.
12. Lin CJ, Pan CF, Liu HL, Chuang CK, Jayakumar T, Wang TJ, dkk. Peran toksin uremik yang terikat protein pada penyakit arteri perifer dan kegagalan akses vaskular pada pasien hemodialisis. Aterosklerosis. 2012;225(1):173–9.
13. Wu PH, Lin YT, Chiu YW, Baldanzi G, Huang JC, Liang SS, dkk. Hubungan indoksil sulfat dan p-kresil sulfat dengan target protein kardiovaskular pada pasien hemodialisis. Sains Rep. 2021;11(1):3786.
14. Falconi CA, Junho CVDC, Fogaça-Ruiz F, Vernier ICS, Da Cunha RS, Stinghen AEM, dkk. Racun uremik: bahaya yang mengkhawatirkan terkait sistem kardiovaskular. Fisik Depan. 2021;12:686249.
15. Wu IW, Hsu KH, Lee CC, Sun CY, Hsu HJ, Tsai CJ, dkk. P-cresyl sulfate dan indoxyl sulfate memprediksi perkembangan penyakit ginjal kronis. Transplantasi Nephrol Dial. 2011;26(3):938–47.
16. Daneshamouz S, Eduok U, Abdelrasoul A, Shoker A. Racun uremik terikat protein (PBUTS) pada pasien penyakit ginjal kronis (CKD): jalur produksi, tantangan, dan kemajuan terkini dalam pembersihan PBUTS ginjal. NanoImpact. 2021;21:100299.
17. Ghuman J, Zunszain PA, Petitpas I, Bhattacharya AA, Otagiri M, Curry S. Dasar struktural spesifisitas pengikatan obat albumin serum manusia. J Mol Biol. 2005;353(1):38–52.
18. Brettschneider F, Toelle M, von der Giet M, Passlick-Deetjen J, Steppan S, Peter M, dkk. Penghapusan toksin uremik hidrofobik yang terikat protein dengan pemisahan plasma fraksinasi gabungan dan teknik adsorpsi. Organ Artifisial. 2013;37(4):409–16.
19. Berge-Lefranc D, Chaspoul F, Cerini C, Brunet P, Gallice P. Studi termodinamika interaksi indoksil sulfat dengan albumin serum manusia dan pengikatan kompetitif dengan p-cresyl sulfate. Kalorim Anal J Term. 2014;115(3):2021–6.
20. Yu S, Schuchardt M, Toelle M, van der Giet M, Zidek W, Dzubiella J, dkk. Interaksi albumin serum manusia dengan racun uremik: studi termodinamika. RSC Adv. 2017;7(45):27913–22.
21. Baboolal K, McEwan P, Sondhi S, Spiewanowski P, Wechowski J, Wilson K. Biaya dialisis ginjal di UK setting--studi multisenter. Transplantasi Nephrol Dial. 2008;23(6):1982–9.
22. Harris A, Cooper BA, Li JJ, Bulfone L, Branley P, Collins JF, dkk. Efektivitas biaya memulai dialisis lebih awal: uji coba terkontrol secara acak. Am J Kidney Dis. 2011;57(5):707–15.
23. BA Muda, Chan C, Blagg C, Lockridge R, Golper T, Finkelstein F, dkk. Cara mengatasi hambatan dan membangun program HD rumah yang sukses. Klinik J Am Soc Nephrol. 2012;7(12):2023–32.
24. Dinh DC, Recht NS, Hostetter TH, Meyer TW. Dilapisi karbon hemoperfusion memberikan izin terbatas dari zat terlarut yang terikat protein. Organ Artifisial. 2008; 32(9):717–24.
25. Ash SR. Sorben dalam pengobatan uremia: sejarah singkat dan masa depan yang cerah. Semin Dial. 2009;22(6):615–22.
26. Gun'Ko VM, Betz WR, Patel S, Murphy MC, Mikhalovsky SV. Adsorpsi lipopolisakarida pada saringan karbon. Karbon. 2006;44(7):1258–62.
27. Ash SR, Sullivan TA, Carr DJ. Suspensi sorben vs kolom sorben untuk detoksifikasi ekstrakorporeal pada gagal hati. Ada Apher Dial. 2006;10(2):145–53.
28. Ye C, Gong Q, Lu F, Liang J. Adsorpsi racun uremik pada karbon nanotube. Sep Purif Technol. 2007;58(1):2–6.
29. Lu C, Su F. Adsorpsi bahan organik alami oleh karbon nanotube. Sep Purif Technol. 2007;58(1):113–21.
30. Spitalsky Z, Tasis D, Papagelis K, Galiotis C. Komposit karbon nanotube-polimer: kimia, pemrosesan, sifat mekanik dan listrik. Ilmu Polim Prog. 2010;35(3):357–401.
31. Liu Y, Peng X, Hu Z, Yu M, Fu J, Huang Y. Pembuatan adsorben karbon berpori yang mengandung nitrogen untuk menghilangkan racun uremik yang terikat protein. Mater Sci Eng C Mater Biol Appl. 2021;121:111879.
32. Soldatkin OO, Soy E, Errachid A, Jaffrezic-Renault N, Akata B, Soldatkin AP, dkk. Pengaruh komposisi zeolit/nanobiokomposit enzim terhadap karakteristik analitik biosensor urea berdasarkan transistor efek medan selektif ion. Sens Lett. 2011;9(6SI):2320–6.
33. Wernert V, Schäf O, Ghobarkar H, Denoyel R. Sifat adsorpsi zeolit untuk aplikasi ginjal buatan. Tikar Mesopor Mikropor. 2005;83(1): 101–13.
34. Bergé-Lefranc D, Pizzala H, Paillaud JL, Schäf O, Vagner C, Boulet P, dkk. Adsorpsi molekul toksin uremik kecil pada zeolit tipe mfi dari larutan air. Adsorpsi. 2008;14(2):377–87.
35. Bergé-Lefranc D, Vagner C, Calaf R, Pizzala H, Denoyel R, Brunet P, dkk. Eliminasi in vitro toksin uremik terikat protein p-kresol oleh zeolit tipe mfi. Tikar Mesopor Mikropor. 2012;153:288–93.
36. Namekawa K, Tokoro Schreiber M, Aoyagi T, Ebara M. Fabrikasi nanofiber komposit zeolit– polimer untuk menghilangkan racun uremik dari pasien gagal ginjal. Biomater Sci-Uk 2014;2(5):674–9.
37. Lu L, Chen C, Samarasekera C, Yeow JTW. Pengaruh bentuk dan ukuran partikel zeolit pada kapasitasnya untuk menyerap toksin uremik sebagai bubuk dan sebagai pengisi dalam membran. J Biomed Mater Res B Appl Biomater. 2017;105(6):1594–601.
38. Tantekin-Ersolmaz SB, Atalay-Oral C, Tatlier M, Erdem-Senatalar A, Schoeman B, Sterte J. Pengaruh ukuran partikel zeolit pada kinerja membran matriks campuran zeolit polimer. Ilmu Membran J. 2000;175(2):285–8.
39. Wernert V, Schäf O, Faure V, Brunet P, Dou L, Berland Y, dkk. Adsorpsi toksin uremik p-kresol ke membran hemodialisis dan adsorben zeolit silikalit mikropori. J Bioteknol. 2006;123(2):164–73.
40. Furukawa H, Cordova KE, O'Keeffe M, Yaghi OM. Kimia dan aplikasi kerangka logam-organik. Sains. 2013;341(6149):974.
41. Haque E, Jun JW, Jhung SH. Penghapusan adsorpsi jingga metil dan biru metilen dari larutan air dengan bahan kerangka logam-organik, besi tereftalat (mof-235). J Hazard Mater. 2011;185(1):507–11.
42. Fletcher AJ, Thomas KM, Rosseinsky MJ. Fleksibilitas dalam bahan kerangka logam-organik: berdampak pada sifat penyerapan. J Solid State Chem. 2005;178(8):2491–510.
43. Cuchiaro H, Thai J, Schaffner N, Tuttle RR, Reynolds M. Menjelajahi ruang parameter adsorpsi p-cresyl sulfate dalam kerangka logam-organik. Antarmuka Appl Mater ACS. 2020;12(20):22572–80.
44. Tan J, Civalleri B. Kerangka logam-organik dan bahan hibrid: dari dasar hingga aplikasi. Crystengcomm. 2015;17(2):197–8.
45. Abdelhameed RM, Abdel-Gawad H, Taha M, Hegazi B. Pemisahan chamazulene bioaktif dari ekstrak chamomile menggunakan kerangka logam-organik. Biomed Farmasi J. 2017;146:126–34.
46. Mon M, Bruno R, Ferrando-Soria J, Armentano D, Pardo E. Teknologi kerangka logam-organik untuk remediasi air: menuju ekosistem yang berkelanjutan. J Mater Chem A. 2018;6(12):4912–47.
47. Abdelhameed RM, Abdel-Gawad H, Elshahat M, Emam HE. Komposit Cu–btc@cotton: desain dan penghilangan insektisida ethion dari air. RSC Adv. 2016;6(48):42324–33.
48. Huxford RC, Della Rocca J, Lin W. Kerangka logam-organik sebagai pembawa obat potensial. Curr Opin Chem Biol. 2010;14(2):262–8.
49. Rodenas T, Luz I, Prieto G, Seoane B, Miro H, Corma A, dkk. Nanosheet kerangka logam-organik dalam bahan komposit polimer untuk pemisahan gas. Nat Mater. 2015;14(1):48–55.
50. Kato S, Otake K, Chen H, Akpinar I, Buru CT, Islamoglu T, dkk. Kerangka logam-organik berbasis zirkonium untuk menghilangkan toksin uremik yang terikat protein dari albumin serum manusia J Am Chem Soc. 2019;141(6):2568–76.
51. Abdelhameed RM, Rehan M, Emam HE. Figurasi komposit kain mof@cotton berbasis zr untuk potensi aplikasi ginjal. Polim Karbohidrat. 2018; 195:460–7.
52. Dymek K, Kurowski G, Kuterasinski L, Jedrzejczyk R, Szumera M, Sitarz M, dkk. Mencari kerangka kerja logam-organik otomatis-66 yang efektif untuk aplikasi ginjal buatan. ACS Appl Mater Inter. 2021;13(38):45149–60.
53. Zhu J, Wu L, Bu Z, Jie S, Li B. Kerangka kerja logam-organik UiO-66-nh2 (zr) yang dimodifikasi polietilenimina: persiapan dan adsorpsi selektif co2 yang ditingkatkan. ACS Omega. 2019;4(2):3188–97.
54. Chen H, Bian F, Sun L, Zhang D, Shang L, Zhao Y. Partikel berpori yang dicetak secara hierarkis untuk pembersihan ginjal biomimetik. Mater Adv. 2020; 32(52):2005394.
55. Mejia-Ariza R, Grana-Suarez L, Verboom W, Huskens J. Nanopartikel supramolekul berbasis siklodekstrin untuk aplikasi biomedis. J Mater Chem B. 2017;5(1):36–52.
56. Li J, Han L, Liu S, He S, Cao Y, Xie J, dkk. Penghapusan indoksil sulfat oleh polisiklodekstrin yang larut dalam air dalam dialisis. Permukaan Koloid B. 2018;164:406–13.
57. Li J, Han L, Xie J, Liu S, Jia L. Adsorben poli siklodekstrin multi-situs untuk menghilangkan racun uremik yang terikat protein yang digabungkan dengan hemodialisis. Polim Karbohidrat. 2020;247:116665.
58. Gogotsi Y, Anasori B. Munculnya mxenes. ACS nano. 2019;13(8):8491–4.
59. Zhao Q, Seredych M, Precetti E, Shuck CE, Harhay M, Pang R, dkk. Adsorpsi racun uremik menggunakan pria ti3c2tx untuk regenerasi dialisat. ACS nano. 2020;14(9):11787–98.
60. Dai C, Lin H, Xu G, Liu Z, Wu R, Chen Y. Biokompatibel 2d titanium carbide (mxenes) nanosheet komposit untuk hipertermia tumor yang dipandu mri responsif-ph. Materi Kimia. 2017;29(20):8637–52.
61. Wang T, Sun X, Guo X, Zhang J, Yang J, Tao S, dkk. Badai sitokin yang sangat menenangkan menggunakan ti (3) c (2) t (x) mxene. Metode Kecil. 2021;5(5): e2001108.
62. Tian H, Tang Z, Zhuang X, Chen X, Jing X. Polimer sintetis yang dapat terurai secara hayati: persiapan, fungsionalisasi, dan aplikasi biomedis. Ilmu Polim Prog. 2012;37(2):237–80.
63. Weber V, Linsberger I, Hauner M, Leistner A, Leistner A, Falkenhagen D. Kopolimer styrene-divinylbenzene netral untuk adsorpsi racun pada gagal hati. Biomakromolekul. 2008;9(4):1322–8.
64. Jiang X, Xiang T, Xie Y, Wang R, Zhao W, Sun S et al. Partikel polietersulfon fungsional untuk menghilangkan bilirubin. Journal of Material Science: Materials in Medicine 2015;27(2):28.
65. Lu L, Samarasekera C, Yeow JTW. Kapasitas adsorpsi kreatinin membran nanofiber electrospun polyacrylonitrile (PAN)-zeolite untuk potensi aplikasi ginjal buatan. J Appl Polym Sci 2015;132(34): 42418- 26.
66. Lu L, Yeow JTW. Kajian adsorpsi indoksil sulfat oleh membran komposit zeolit dan polietersulfon-zeolit. Desain Mater. 2017;120: 328–35.
67. Tijink MS, Wester M, Sun J, Saris A, Bolhuis-Versteeg LA, Saiful S, dkk. Pendekatan baru untuk pemurnian darah: membran matriks campuran menggabungkan difusi dan adsorpsi dalam satu langkah. Biomater Akta. 2012;8(6):2279–87.
68. Tijink MSL, Wester M, Glorieux G, Gerritsen KGF, Sun J, Swart PC, dkk. Membran serat berongga matriks campuran untuk menghilangkan racun yang terikat protein dari plasma manusia. Biomaterial. 2013;34(32):7819–28.
69. Pavlenko D, van Geffen E, van Steenbergen MJ, Glorieux G, Vanholder R, Gerritsen KGF dkk. Membran matriks campuran low-flux baru menawarkan penghilangan toksin terikat protein yang unggul dari plasma manusia. Sci Rep 2016;6:34429.
70. Geremia I, Pavlenko D, Maksymow K, Rueth M, Lemke HD, Stamatialis D. Ex vivo evaluasi kompatibilitas darah membran hemodialisis matriks campuran. Biomater Akta. 2020;111:118–28.
71. Geremia I, Bansal R, Stamatialis D. Penilaian in vitro membran hemodialisis matriks campuran untuk mencapai dialisat bebas endotoksin dikombinasikan dengan penghilangan racun uremik yang tinggi dari plasma manusia. Biomater Akta. 2019;90:100–11.
72. Nie C, Ma L, Xia Y, He C, Deng J, Wang L, dkk. Kuas polimer peniru heparin baru yang dicangkokkan membran karbon nanotube/pes komposit untuk pemurnian darah yang aman dan efisien. Ilmu Membran J. 2015;475:455–68.
73. Zhang Y, Lim CT, Ramakrishna S, Huang Z. Perkembangan terbaru dari nanofibers polimer untuk aplikasi biomedis dan bioteknologi. J Mater Sci Mater Med. 2005;16(10):933–46.
74. Ramakrishna S, Fujihara K, Teo W, Yong T, Ma Z, Ramaseshan R. Serat nano elektrospun: memecahkan masalah global. Mater Hari ini. 2006;9(3):40–50.
75. Huang Z, Zhang YZ, Kotaki M, Ramakrishna S. Tinjauan tentang serat nano polimer dengan elektrospinning dan aplikasinya dalam nanokomposit. Compos Sci Technol. 2003;63(15):2223–53.
76. Fu GD, Xu LQ, Yao F, Zhang K, Wang XF, Zhu MF, dkk. Serat nano cerdas dari gabungan polimerisasi radikal hidup, "kimia klik", dan elektrospinning. ACS Appl Mater Inter. 2009;1(2):239–43.
77. Kim Y, Ebara M, Aoyagi T. Jaring nanofiber pintar yang menangkap dan melepaskan sel. Angew Chem Int Ed. 2012;51(42):10537–41.
78. Wang XY, Drew C, Lee SH, Senecal KJ, Kumar J, Samuelson LA. Teknologi Electrospinning: pendekatan baru untuk aplikasi sensor. J Macromol Sci Pure Appl Chem. 2002; A39(10):1251–8.
79. Barhoum A, Pal K, Rahier H, Uludag H, Kim IS, Bechelany M. Nanofibers sebagai bahan generasi baru: dari teknik fabrikasi pemintalan dan pemintalan nano hingga aplikasi baru. Aplikasi Mater Hari Ini. 2019; 17:1–35.
80. Peh P, Lim NSJ, Blocki A, Chee SML, Park HC, Liao S, dkk. Pengiriman simultan senyawa bioaktif yang sangat beragam dari serat electrospun campuran untuk penyembuhan luka kulit. Kimia Biokonjugat. 2015;26(7):1348–58.
81. Qi R, Guo R, Shen M, Cao X, Zhang L, Xu J, dkk. Electrospun poly (lactic-co-glycolic acid)/halloysite nanotube composite nanofibers untuk enkapsulasi obat dan pelepasan berkelanjutan. J Mater Chem. 2010;20(47):10622–9.
82. Salalha W, Kuhn J, Dror Y, Zussman E. Enkapsulasi bakteri dan virus dalam serat nano elektrospun. Nanoteknologi. 2006;17(18):4675–81.
83. Luo Y, Nartker S, Miller H, Hochhalter D, Wiederoder M, Wiederoder S, dkk. Fungsionalisasi permukaan serat nano elektrospun untuk mendeteksi e. Coli o157:h7 dan sel tubuh dalam biosensor transfer muatan langsung. Biosen Bioelektron. 2010;26(4):1612–7.
84. Esmaeili A, Haseli M. Elektrospinning nanofibers karboksimetil selulosa termoplastik/poli (etilena oksida) untuk digunakan dalam sistem pelepasan obat. Mat Sci Eng C-Mater. 2017;77:1117–27.
85. Han D, Steckl AJ. Membran nanofiber elektrospun triaksial untuk pelepasan ganda molekul fungsional yang terkontrol. ACS Appl Mater Inter. 2013;5(16):8241–5.
86. Bahramimehr F, Esmaeili A. Memproduksi nanofiber hibrida berbasis /pan/fe3o4/zeolit/ekstrak tanaman jelatang/urease dan polimer alami koaksial cacat untuk mengurangi bahan toksisitas dalam darah pasien dialisis. J Biomed Mater Res A. 2019;107(8):1736–43.
87. Irfan M, Idris A, Yusof NM, Khairuddin NFM, Akhmal H. Modifikasi permukaan dan peningkatan kinerja membran hemodialisis nano-hybrid f-mwcnt/pvp90/pes. Ilmu Membran J. 2014;467:73–84.
88. Niyogi S, Hamon MA, Hu H, Zhao B, Bhowmik P, Sen R, dkk. Kimia nanotube karbon berdinding tunggal. Akun Chem Res. 2002;35(12):1105–13.
89. Raravikar NR, Schadler LS, Vijayaraghavan A, Zhao Y, Wei B, Ajayan PM. Sintesis dan karakterisasi film komposit karbon nanotube-polimer yang disejajarkan dengan ketebalan. Materi Kimia. 2005;17(5):974–83.
90. Valcárcel M, Cárdenas S, Simonet BM, Moliner-Martínez Y, Lucena R. Struktur nano karbon sebagai bahan penyerap dalam proses analitik. TraC Trends Analyt Chem. 2008;27(1):34–43.
91. Tsuge M, Takahashi K, Kurimoto R, Fulati A, Uto K, Kikuchi A, dkk. Pembuatan jaring nanofiber penyerap air menuju pembuangan kelebihan air yang efisien dari pasien gagal ginjal. Serat. 2019;7(5):39.
92. Khan I, Saeed K, Khan I. Nanopartikel: sifat, aplikasi, dan toksisitas. Arab J Chem. 2019;12(7):908–31.
93. Wang L, Zhang Y, Li Y, Chen J, Lin W. Kemajuan terbaru dalam bahan nano rekayasa untuk theranostics cedera ginjal akut. Nano Res. 2021;14(4):920–33.
94. Stamopoulos D, Bouziotis P, Benaki D, Kotsovassilis C, Zirogiannis PN. Pemanfaatan nanobioteknologi dalam hemodialisis: percobaan mock-dialisis pada homocysteine. Transplantasi Nephrol Dial. 2008;23(10):3234–9.
95. Ma Y, Cai F, Li Y, Chen J, Han F, Lin W. Tinjauan penerapan nanopartikel dalam diagnosis dan pengobatan penyakit ginjal kronis. Bioact Mater. 2020;5(3):732–43.
96. Cheah W, Ishikawa K, Othman R, Yeoh F. biomaterial nanopori untuk adsorpsi toksin uremik dalam sistem ginjal buatan: ulasan. J Biomed Mater Res B Appl Biomater. 2017;105(5):1232–40.
97. Abidin MNZ, Goh PS, Ismail AF, Said N, Othman MHD, Hasbullah H, dkk. Nanopartikel pati teroksidasi dengan daya serap tinggi untuk penghilangan urea yang efisien. Polim Karbohidrat. 2018;201:257–63.
98. Cabello-Alvarado C, Andrade-Guel M, Pérez-Alvarez M, Cadenas-Pliego G, Cortés-Hernández DA, Bartolo-Pérez P, dkk. Nanoplatelet graphene dimodifikasi dengan gugus amino oleh radiasi ultrasonik dengan frekuensi variabel untuk potensi adsorpsi racun uremik. NanomaterialsBasel. 2019;9(9):1261.
99. Andrade-Guel M, Ávila-Orta CA, Cadenas-Pliego G, Cabello-Alvarado CJ, Pérez-Alvarez M, Reyes-Rodríguez P, dkk. Sintesis nanokomposit karbon hitam nilon 6/modifikasi untuk aplikasi dalam adsorpsi asam urat. Bahan. 2020;13(22):5173.
100. Korsvik C, Patil S, Seal S, Self WT. Sifat mimetik superoksida dismutase ditunjukkan oleh nanopartikel ceria yang direkayasa kekosongan. Komun Kimia. 2007; 10:1056–8.
101. Pirmohamed T, Dowding JM, Singh S, Wasserman B, Heckert E, Karakoti AS, dkk. Nanoceria menunjukkan aktivitas mimetik katalase yang bergantung pada keadaan redoks. Komun Kimia. 2010;46(16):2736–8.
102. Xue Y, Luan Q, Yang D, Yao X, Zhou K. Bukti langsung untuk aktivitas pemulungan radikal hidroksil dari nanopartikel serium oksida. J Phys Chem C. 2011; 115(11):4433–8.
103. Ni D, Wei H, Chen W, Bao Q, Rosenkrans ZT, Barnhart TE, dkk. Nanopartikel Ceria memenuhi cedera iskemia-reperfusi hati: ketidaksempurnaan yang sempurna. Mater Adv. 2019;31(40):1902956.
104. Fleming RE, Ponka P. Iron overload pada penyakit manusia. New Engl J Med. 2012;366(4):348–59.
105. Hamilton JL, Kizhakkedathu JN. Nanocarriers polimer untuk pengobatan kelebihan zat besi sistemik. Sel Mol Ada. 2015;3:3.
106. Kang H, Han M, Xue J, Baek Y, Chang J, Hu S dkk. Khelator nano yang dapat dibersihkan ginjal untuk terapi kelebihan zat besi. Nat Commun 2019;10(1):5134.
107. Mobarra N, Shanaki M, Ehteram H, Nasiri H, Sahmani M, Saeidi M, dkk. Tinjauan tentang kelator besi dalam pengobatan sindrom kelebihan zat besi. Int J Hematol Sel Induk Oncol Res. 2016;10(4):239–47.
108. Shapiro SM. Toksisitas bilirubin pada sistem saraf yang sedang berkembang. Pediatr Neurol. 2003;29(5):410–21.
109. Peng Z, Yang Y, Luo J, Nie C, Ma L, Cheng C, dkk. Manik-manik polimer nanofibrous dari serat aramid untuk menghilangkan bilirubin secara efisien. Biomater Sci-Uk. 2016;4(9):1392–401.
110. Yang M, Cao K, Sui L, Qi Y, Zhu J, Waas A, dkk. Dispersi serat nano aramid: blok bangunan skala nano baru. ACS nano. 2011;5(9):6945–54.
111. Zhao C, Xue J, Ran F, Sun S. Modifikasi membran polietersulfon - tinjauan metode. Prog Mater Sci. 2013;58(1):76–150.
112. Goldberg AL. Degradasi protein dan perlindungan terhadap protein yang salah lipatan atau rusak. Alam. 2003;426(6968):895–9.
113. Furie B, Furie BC. Mekanisme penyakit: mekanisme pembentukan trombus. New Engl J Med. 2008;359(9):938–49.
114. Arepally GM. Trombositopenia yang diinduksi heparin. Darah. 2017;129(21):2864– 72.
115. Ratner BD. Kompatibilitas darah - perspektif. J Biomat Sci-Polym E. 2000; 11(11):1107–19.
116. Mao C, Qiu YZ, Sang HB, Mei H, Zhu AP, Shen J, dkk. Berbagai pendekatan untuk memodifikasi permukaan biomaterial untuk meningkatkan hemokompatibilitas. Antarmuka Koloid Tingkat Lanjut. 2004;110(1-2):5–17.
117. Werner C, Maitz MF, Sperling C. Strategi terkini menuju pelapis yang kompatibel dengan hemokompatibel. J Mater Chem. 2007;17(32):3376–84.
118. Huang J, Xue J, Xiang K, Zhang X, Cheng C, Sun S, dkk. Modifikasi permukaan membran polietersulfon dengan memadukan kopolimer triblock dari metoksil poli (etilena glikol)-poliuretan-metoksil poli (etilen glikol). Permukaan Koloid B. 2011;88(1):315–24.
119. Liu X, Xu Y, Wu Z, Chen H. Poly(n-vinylpyrrolidone)-permukaan yang dimodifikasi untuk aplikasi biomedis. Makromol Biosci. 2013;13(2):147–54.
120. Li X, Wang M, Wang L, Shi X, Xu Y, Song B, dkk. Blokir permukaan yang dimodifikasi kopolimer untuk konjugasi biomakromolekul dengan kontrol kuantitas dan aktivitas. Langmuir. 2013;29(4):1122–8.
121. Modi A, Verma SK, Bellare J. Hidrofilik zif-8 lembar nano yang dihias meningkatkan biokompatibilitas dan kinerja pemisahan membran serat berongga polietersulfon: bahan membran potensial untuk aplikasi hati bioartifisial. Mater Sci Eng C. 2018;91:524–40.
122. Said N, Abidin MNZ, Hasbullah H, Ismail AF, Goh PS, Othman MHD, dkk. Nanopartikel oksida besi meningkatkan biokompatibilitas dan menghilangkan toksin uremik molekul menengah dari membran serat berongga polisulfon. J Appl Polym Sci. 2019;136(48):48234.
123. Wang L, Gong T, Brown Z, Randle C, Guan Y, Ye W, dkk. Nanopartikel magnetik heparin-mimetik yang diilhami ascidian dengan potensi untuk aplikasi dalam hemodialisis sebagai antikoagulan daur ulang ACS Biomater Sci Eng. 2020;6(4): 1998–2006.
124. Cheng C, Sun S, Zhao C. Kemajuan dalam membran biomedis yang difungsikan dengan heparin dan seperti heparin / meniru polimer. J Mater Chem B. 2014;2(44): 7649–72.
125. Nie S, Xue J, Lu Y, Liu Y, Wang D, Sun S, dkk. Kompatibilitas darah yang lebih baik dari membran polietersulfon dengan permukaan hidrofilik dan anionik. Permukaan Koloid B. 2012;100:116–25.
126. Li L, Cheng C, Xiang T, Tang M, Zhao W, Sun S, dkk. Modifikasi membran hemodialisis polietersulfon dengan memadukan poliuretan cangkok asam sitrat dan aktivitas antikoagulannya. Ilmu Membran J. 2012;405:261–74.
127. Wang LR, Qin H, Nie SQ, Sun SD, Ran F, Zhao CS. Sintesis langsung polimer poli (eter sulfon) seperti heparin dan kompatibilitas darahnya. Biomater Akta. 2013;9(11):8851–63.
128. Nie S, Tang M, Cheng CS, Yin Z, Wang L, Sun S, dkk. Desain membran yang terinspirasi secara biologis dengan antarmuka seperti heparin: pembekuan darah yang berkepanjangan, penghambatan aktivasi komplemen, dan proliferasi sel yang berhubungan dengan hati bio-buatan. Biomater Sci-Uk. 2014;2(1):98–109.
129. Ma L, Qin H, Cheng C, Xia Y, He C, Nie C, dkk. Self-coating yang diilhami kerang pada antarmuka makro dengan peningkatan biokompatibilitas dan bioaktivitas melalui polimer dan heparin seperti heparin yang dicangkokkan dengan dopamin. J Mater Chem B. 2014;2(4):363–75.
130. Meyer TW, Peattie JWT, Miller JD, Dinh DC, Recht NS, Walther JL, dkk. Meningkatkan pembersihan zat terlarut yang terikat protein dengan penambahan sorben ke dialisat. J Am Soc Nephrol. 2007;18(3):868–74.
131. Patzer J. Prinsip dialisis zat terlarut terikat. Ada Apher Dial. 2006;10(2):118– 24.
132. Agar JWM. Dialisis hijau: tantangan lingkungan ke depan. Semi Dialisis. 2015;28(2):186–92.
133. Madsen B, Britt DW, Ho C, Henrie M, Ford C, Stroup E, dkk. Kimia permukaan membran hemodialisis sebagai penghalang transfer lipopolisakarida. J Appl Polym Sci. 2015;132(4155021).
134.Lonnemann GR. Kualitas dialisat: pendekatan terpadu. Ginjal Int. 2000;5876:S112–9.
135. Susantitaphong P, Riella C, Jaber BL. Efek dialisat ultra murni pada penanda peradangan, stres oksidatif, nutrisi, dan parameter anemia: meta-analisis. Nephrol Dial Transpl. 2013;28(2):438–46.
136. Gorbet MB, Sefton MV. Endotoksin: tamu tak diundang. Biomaterial. 2005; 26(34):6811–7.
137. Schepers E, Glorieux G, Eloot S, Hulko M, Boschetti-de-Fierro A, Beck W, dkk. Penilaian hubungan antara peningkatan ukuran pori membran dan permeabilitas endotoksin menggunakan pengaturan simulasi dialisis eksperimental baru. BMC Nefrol. 2018;19(1):1–0.
138. Glorieux G, Hulko M, Speidel R, Brodbeck K, Krause B, Vanholder R. Melihat melampaui endotoksin: Sebuah studi perbandingan retensi pirogen oleh ultrafilter yang digunakan untuk persiapan cairan dialisis steril. Sci Rep 2014;4:6390.
139. van Tellingen A, Grooteman M, Schoorl M, Bartels P, Schoorl M, van der Ploeg T, dkk. Peristiwa klinis yang terjadi bersamaan merupakan prediksi kadar protein c-reaktif plasma pada pasien hemodialisis. Ginjal Int. 2002;62(2):632–8.
140. Darkow R, Groth T, Albrecht W, Lutzow K, Paul D. Partikel nano yang difungsikan untuk pengikatan endotoksin dalam larutan berair. Biomaterial. 1999;20(14):1277–83.
141. Murphy MC, Patel S, Phillips GJ, Davies JG, Lloyd AW, Gun'Ko VM, dkk. Adsorpsi sitokin inflamasi dan endotoksin oleh polimer mesopori dan karbon aktif. Di dalam: Rodriguez Reinoso F, McEnaney B, Rouquerol J, Unger K, editor. Studi dalam ilmu permukaan dan katalisis; 2002. hal. 515–20.
Cui Gao1 , Qian Zhang1 , Yi Yang1,2,3, Yangyang Li4,5 and Weiqiang Lin1,3
1 Pusat Penyakit Ginjal, Rumah Sakit Afiliasi Pertama, Fakultas Kedokteran Universitas Zhejiang, Hangzhou 310003, Zhejiang, Tiongkok.
2 Departemen Nefrologi, Rumah Sakit Afiliasi Keempat, Fakultas Kedokteran Universitas Zhejiang, Yiwu 322000, Zhejiang, China.
3 Institut Kedokteran Internasional, Rumah Sakit Afiliasi Keempat, Fakultas Kedokteran Universitas Zhejiang, Yiwu 322000, Zhejiang, Cina.
4 Laboratorium Utama Penelitian Kesehatan Reproduksi Wanita Provinsi Zhejiang, Rumah Sakit Wanita, Fakultas Kedokteran Universitas Zhejiang, Hangzhou 310006, Zhejiang, China.
5 Cancer Center, Universitas Zhejiang, Hangzhou 310058, Zhejiang, Cina.






