Pasien Bedah Vaskular Dengan Peningkatan Rasio Neutrofil-limfosit Mengalami Penurunan Regulasi Ekspresi RNA Komplemen Neutrofil
Nov 24, 2023
Peningkatan rasio neutrofil terhadap limfosit (NLR) pada pasien yang menjalani bedah vaskular elektif (EVS) telah meningkatkan angka kematian terlepas dari hasil bedah perioperatif. Untuk memahami mengapa NLR tinggi dikaitkan dengan kematian yang lebih tinggi, kami menyelidiki ekspresi transkriptome neutrofil dan limfosit pada pasien yang menjalani EVS. Sampel darah dikumpulkan dari pasien yang menjalani EVS dan donor sehat untuk perhitungan NLR. Sampel RNA diisolasi dari neutrofil dan limfosit pasien dan dibagi menjadi NLR_Rendah (<3) and NLR_High (≥3) groups (n = 6 each). Paired samples with the highest RNA integrity number (mean = 9.8 ± 0.4) were sequenced and analyzed for differential expression. Normalized data were inputted for downstream analysis using iPathwayGuide (AdvaitaBio) and gene set enrichment analysis using GenePattern and MSigDB (Broad Institute). There was no clinical difference between the patient groups about clinical diagnosis, age, sex, history of hypertension, lipid abnormalities, diabetes mellitus, smoking, or statin use. The mean NLR was 4.37 ± 0.27 SEM in the NLR_High and 1.88 ± 0.16 for the NLR_Low groups. Significantly differentially expressed gene sets identified in the RNA sequence data were enriched highly (P = 1E-24) in the humoral immunity and complement systems. Neutrophils from NLR_High patients downregulated complement genes (C1QA, C1QB, C1QC, C1S, C2, CR2, C3AR1, C3, C8G, and C9 and complement regulatory genes CD59, SERPING1, C4BPA, CFH, and CFI). Downregulation of gene expressions of humoral immunity and complement within the neutrophils are associated with elevated NLR. It remains to be determined whether and how these changes contribute to increased late mortality previously observed in patients undergoing EVS.

manfaat cistanche untuk pria-memperkuat sistem kekebalan tubuh
Perkenalan
Penyakit kardiovaskular (CVD) merupakan penyebab utama kematian di seluruh dunia. Hal ini sebagian besar disebabkan oleh aterogenesis dan aterosklerosis yang, selain faktor genetik dan pola makan individu, juga dimediasi oleh mekanisme inflamasi dan imun.1-3 Baru-baru ini, perbedaan jumlah leukosit (neutrofil dan limfosit) menjadi fokus untuk memprediksi hasil kardiovaskular (CV). Rasio jumlah neutrofil-limfosit absolut (NLR) telah diakui sebagai prediktor kematian total dalam beberapa penelitian kecil mengenai intervensi koroner akut, hipertensi,7,8, dan gagal jantung.9
Tabel 1. Karakteristik klinis pasien bedah vaskular elektif yang diperiksa dengan RNA-seq

Investigasi sebelumnya juga menunjukkan bahwa NLR merupakan prediktor hasil jangka panjang pada pasien dengan penyakit pembuluh darah perifer.10-13 Studi retrospektif kami terhadap populasi pasien bedah pembuluh darah mendukung kesimpulan ini. Dalam 1 penelitian terhadap 108 pasien dengan perbaikan aneurisma aorta perut endovaskular elektif, tidak ada perbedaan dalam angka kematian 30-hari pasca operasi antara NLR sebesar<4 and an NLR of >4 (P = .507). However, the 1-year, 3-year, and 5-year mortality between the groups were 4.2% vs 28.1%, 15.1% vs 64.9%, and 24% vs 90%, respectively.14 In a second study of 290 asymptomatic patients undergoing prophylactic carotid endarterectomy, the risk for stroke was noted to be significantly higher (P < .0001) in patients with an NLR of >3 (n=116 pasien, 42,6% risiko stroke) dibandingkan mereka yang memiliki NLR sebesar<3 (n = 174 patients, 9.3% stroke risk).15 In a third study with 488 patients who underwent percutaneous interventions of femoropopliteal arteries, the 30-day mortality rates increased significantly (P = .005) with increasing NLR (1.4%, 4.3%, and 7.0% for low [<3], mid [3-4], and high [>4] kelompok NLR, masing-masing).16 Pasien dengan NLR pra operasi yang lebih rendah mencapai kelangsungan hidup bebas amputasi yang jauh lebih besar pada 4-tahun masa tindak lanjut (NLR rendah 65,5%, NLR sedang, 37,5%, dan NLR tinggi, 17,6 % [P < 0,0001]).16
Dalam penelitian ini, kami melakukan pengurutan RNA (RNA-seq) neutrofil dan limfosit dari pasien yang memenuhi syarat untuk perbaikan bedah vaskular elektif (EVS) untuk menentukan mekanisme potensial peningkatan NLR. Studi tersebut menguji apakah ada dasar molekuler untuk peningkatan NLR. Investigasi kami mengungkapkan bahwa pasien dengan peningkatan NLR yang menjalani perbaikan EVS ditandai dengan penurunan regulasi imunoglobulin dan gen komplemen yang sangat signifikan pada neutrofil.

manfaat cistanche-memperkuat sistem kekebalan tubuh
Metode
Pasien
Blood samples were collected from candidate patients for EVS procedures and healthy volunteers for NLR calculation and RNA sequence studies of neutrophils and lymphocytes. In screening patients for participation, any individual with an active local or systemic infection or obvious inflammatory disease was excluded from participation. Peripheral blood collection was approved by the institutional review board of University Hospitals Cleveland Medical Center (#01-06-02). Informed consent was obtained from each patient and healthy volunteer. All patients for EVS seen in the outpatient department were eligible. Patients in the study were characterized for the type of vascular surgery, age, sex, hypertension (blood pressure >130/80 mm Hg), diabetes mellitus (fasting blood glucose >100 mg/dL), status merokok, pengobatan statin, riwayat penyakit paru obstruktif kronik, kanker, penyakit ginjal kronik, penyakit arteri koroner (CAD), penyakit arteri perifer, penyakit serebrovaskular, dan gagal jantung kronik. Semua pasien menjalani hitung darah lengkap dengan jumlah sel darah putih diferensial. Pasien dibagi menjadi NLR rendah (NLR_Rendah [<3]) and high NLR (NLR_High [≥3]) groups (n = 6 each) and healthy volunteers aged 18 to 71 years (n = 6). Eleven of 12 patients' blood was drawn before surgery. One patient had blood drawn 4 months after surgery.
Pemisahan darah
Darah utuh (20 mL per pasien) dikumpulkan dalam tabung vacutainer 10 mL yang diberi antikoagulan dengan EDTA, dan darah dipisahkan dalam waktu satu jam setelah pengumpulan. Populasi sel neutrofil dan limfosit masing-masing diisolasi dari 8 mL darah menggunakan kit isolasi sel manusia langsung EasySep (STEMCELL Technologies, Vancouver, Kanada) dan magnet Big Easy EasySep (STEMCELL Technologies, Vancouver, Kanada) sesuai dengan protokol pabrikan. Magnet telah didinginkan di atas es sebelumnya, dan sel darah serta reagen dicampur secara lembut dengan membalik tabung, bukan dengan memipet. Rasio reagen juga disesuaikan dengan cara berikut untuk mengoptimalkan pemulihan: 400 mL campuran antibodi, 400 mL manik magnetik, dan 4 mL larutan salin yang mengandung fosfat ditambahkan ke dalam darah sebelum pemisahan pertama, diikuti dengan 200 mL antibodi. campuran dan 400 mL manik-manik sebelum pemisahan kedua dan 200 mL manik-manik sebelum pemisahan ketiga dan terakhir. Aliquot kecil 200 mL diambil dari volume pemulihan akhir untuk penghitungan sel dan persiapan slide. Sisa volume pemulihan disentrifugasi dengan kecepatan 1000 putaran per menit selama 7 menit untuk membuat pelet sel.

Gambar 1. Seluruh transkriptom RNA dari neutrofil dan limfosit yang dikumpulkan dari pasien dengan NLR, tinggi (NLR_Tinggi), rendah (NLR_Rendah), atau kontrol (NLR_Kontrol) . Kode huruf "N" atau "L" pada nama sampel berarti neutrofil atau limfosit adalah sumber RNA. Ada 6 pasien dalam setiap kategori. Biru=mengurangi tingkat ekspresi; merah=ekspresi tingkat tinggi.
Penghitungan sel dan persiapan slide
Sel-sel yang disuspensikan kembali dalam larutan salin yang mengandung fosfat selanjutnya dihilangkan, dicampur dengan tripan biru, dan dihitung secara manual menggunakan hemositometer. Biasanya, 9 × 106 hingga 15 × 106 neutrofil dan 3 × 106 hingga 10 × 106 limfosit diisolasi per sampel. Slide sel yang diisolasi dibuat menggunakan cytocentrifuge, diputar dengan kecepatan 600 putaran per menit selama 3 menit, dan kemudian diwarnai dengan pewarnaan Wright-Giemsa. Kemurnian setiap populasi sel ditentukan dengan penghitungan manual, di mana setidaknya 1000 sel dibedakan per slide. Kemurnian rata-rata pemisahan neutrofil dan limfosit berdasarkan penghitungan sel masing-masing adalah 98,3% dan 96,2%. Flow cytometry dilakukan pada 1 pasangan sampel neutrofil dan limfosit dan menunjukkan kemurnian masing-masing 90,6% dan 92,2%. Sel-sel lain dalam sediaan neutrofil dipecah menjadi limfosit (4%), monosit (2%), eosinofil (2,3%), dan basofil (0,3%). Pada sediaan limfosit, sel lainnya adalah neutrofil (1,2%), monosit (1,4%), eosinofil (1,2%), dan basofil (1,8%). Data RNA-seq massal dari semua sampel individu juga digunakan untuk menentukan tingkat kontaminasi monosit dalam persiapan sel dengan menentukan apakah neutrofil atau limfosit dari sampel NLR_Tinggi atau NLR_Rendah telah meningkatkan CD14 secara signifikan , CD68, CD83, atau CD163. Secara independen, data RNA-seq dimasukkan untuk memperkirakan proporsi sel imun dan kanker (EPIC), sebuah program yang dirancang untuk memperkirakan proporsi sel imun dan kanker dalam data ekspresi gen massal.17 Profil referensi yang digunakan disediakan oleh EPIC untuk sel kekebalan yang beredar dalam darah dan berisi profil sel B, sel T CD4 dan CD8, monosit, neutrofil, dan sel pembunuh alami. Output yang dilaporkan diberikan sebagai fraksi sel per sampel.
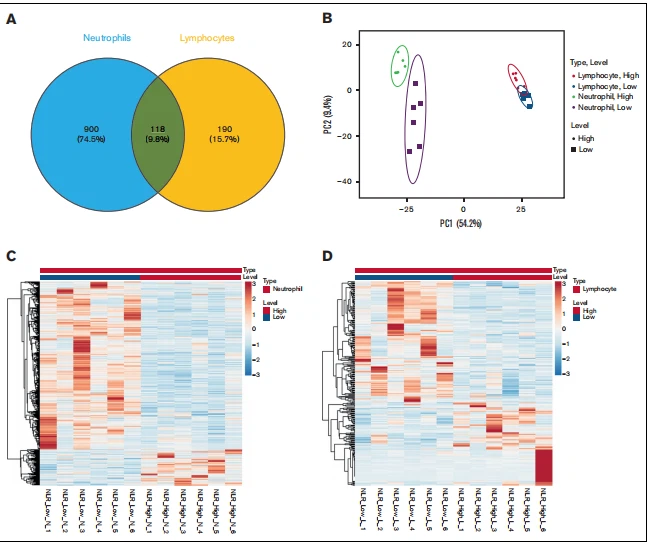
Gambar 2. Gen yang diekspresikan berbeda secara signifikan dari neutrofil dan limfosit. (A) Jumlah gen yang diekspresikan berbeda secara signifikan dalam neutrofil (biru) dan limfosit (oranye). (B) Plot analisis komponen utama dari gen yang diekspresikan secara berbeda secara signifikan dalam neutrofil (hijau dan ungu) dan limfosit (merah dan biru) dalam NLR_Tinggi (lingkaran) dan NLR_Rendah (kotak). (C) Peta panas gen yang diekspresikan berbeda secara signifikan dari NLR_Tinggi vs NLR_RNA neutrofil rendah. (D) Peta panas dari gen yang diekspresikan berbeda secara signifikan dari NLR_Tinggi vs NLR_RNA limfosit rendah.
RNA-seq dan analisis statistik
Metode terperinci untuk ekstraksi dan pengurutan RNA disajikan dalam Metode tambahan. Urutan pembacaan dinilai kualitasnya, dan adaptor dipangkas menggunakan TrimGalore! (Babraham Institute), skrip pembungkus untuk FastQC dan CutAdapt. Pembacaan yang lolos kontrol kualitas diselaraskan dengan genom referensi manusia GRCh38 menggunakan perangkat lunak STAR aligner. Pembacaan yang selaras diproses menggunakan Manset versi 2.2.1 untuk analisis ekspresi diferensial menggunakan anotasi gen GENCODE untuk GRCh38 dan data ekspresi tingkat gen dilaporkan dalam fragmen per kilobase transkrip per juta pembacaan yang dipetakan.18 Gen yang diekspresikan secara berbeda secara signifikan diidentifikasi menggunakan false nilai P batas tingkat penemuan<.05, after the Benjamini-Hochberg correction for multiple testing. Normalized fold-change and P values for all expressed genes were then used as input for downstream analysis using iPathwayGuide (AdvaitaBio) and gene set enrichment analysis (GSEA) using GenePattern and MSigDB (Broad Institute). Additional figures including heat maps and scatterplots were generated in R and ClustVis.
Hasil
Karakteristik pasien
Enam pasang sampel pasien dipilih dari 7 NLR_Tinggi dan 9 NLR_Rendah berdasarkan kualitas RNA tertinggi pada pasangan tersebut sebagaimana dinilai dengan nomor integritas RNA (RIN) (Tabel 1 ). Enam kontrol dari 8 donor sehat juga diperiksa. Pada pasien yang termasuk dalam penelitian ini, rata-rata ± standar deviasi NLR untuk NLR_Tinggi adalah 4,37 ± 0,66 vs untuk NLR_Rendah, 1,87 ± 0. 39 (P < .0001). Rata-rata ± deviasi standar usia pasien adalah 61,0 ± 17,0 tahun untuk NLR_Tinggi dan 64,5 ± 7,5 tahun untuk NLR_Rendah (P= 0,68). Semua pasien kecuali 1 pasien menderita penyakit aneurisma aorta, 9 pasien menderita penyakit toraks/thoracoabdominal, dan 2 pasien menderita penyakit abdominal. Kedua pasien dengan aneurisma aorta perut berada dalam kelompok NLR_Rendah. Sebelas dari 12 pasien memiliki riwayat hipertensi. Empat dari 6 pasien pada kelompok NLR_Tinggi atau NLR_Rendah memiliki riwayat medis kelainan lipid. Empat pasien dalam kelompok NLR_Tinggi dan 3 pasien dalam kelompok NLR_Rendah adalah mantan perokok. Satu pasien dalam kelompok NLR_Rendah adalah perokok aktif. Lima pasien dalam kelompok NLR_Tinggi dan 4 pasien dalam kelompok NLR_Rendah menggunakan statin. Hanya 3 pasien pada kedua kelompok yang menderita diabetes. Satu pasien di setiap kelompok memiliki riwayat CAD, dan 2 pasien di kelompok NLR_Rendah memiliki penyakit arteri perifer.

Gambar 3. Data RNA-seq dalam penyelidikan ini digunakan sebagai alat independen untuk menentukan kontaminasi sel lain dalam sediaan neutrofil dan limfosit. Hanya data dari neutrofil yang ditampilkan. Analisis EPIC dilakukan untuk memperkirakan proporsi sel imun dan kanker dalam data ekspresi gen massal. Analisis ini menghasilkan persentase neutrofil, monosit, sel B, sel T CD4, sel T CD8, sel natural killer (NK), dan sel lain dalam sediaan neutrofil.
Seluruh transkriptom
Kami mengamati perbedaan global dalam keseluruhan transkriptom ketika membandingkan profil ekspresi gen antara neutrofil dan limfosit (Gambar 1). Temuan ini tidak mengejutkan karena ekspresi gen spesifik tipe sel sebelumnya telah ditandai berbeda.19 Pada bagian neutrofil, seluruh pasien dalam NLR_Tinggi, NLR_Rendah, dan NLR{{ 4}}Pada kelompok kontrol, terdapat banyak gen yang diregulasi namun jelas tidak diregulasi di bagian limfosit dan sebaliknya. Pada tingkat transkriptome secara keseluruhan, perbedaan spesifik sel antara neutrofil dan limfosit berbeda dan dominan terlepas dari NLR atau pasien atau kontrol. Namun, jika dicermati lebih dekat, perbedaan mulai terlihat. Plot analisis komponen utama menunjukkan bahwa NLR_Kontrol untuk neutrofil atau limfosit tumpang tindih dengan NLR_Tinggi dan NLR_Rendah di kedua sel (Gambar Tambahan 1). Investigasi selanjutnya berupaya menemukan perbedaan tambahan antara kelompok NLR_Tinggi dan NLR_Rendah dalam gen yang diekspresikan secara berbeda secara signifikan. Telah diamati bahwa 900 (74,5%) gen yang diekspresikan secara berbeda secara signifikan diamati pada neutrofil pada kelompok NLR_Tinggi vs NLR_Rendah (Gambar 2A). Sebagai perbandingan, limfosit hanya memiliki 190 (15,7%) gen yang diekspresikan berbeda secara signifikan. Plot analisis komponen utama NLR_Gen tinggi vs NLR_Gen rendah pada neutrofil dan limfosit mengungkapkan bahwa kelompok gen NLR_Tinggi vs NLR_Gen rendah pada neutrofil dipisahkan menjadi 2 area berbeda, sedangkan gen limfosit NLR_Tinggi dan NLR_Rendah saling tumpang tindih (Gambar 2B). Sekali lagi, seperti seluruh data transkriptome, NLR_Kontrol tumpang tindih dengan NRL_Tinggi dan NLR_Rendah secara signifikan mengekspresikan gen yang berbeda pada neutrofil dan limfosit (Gambar Tambahan 2). Sebagian besar gen yang diekspresikan berbeda secara signifikan dalam neutrofil NLR_Tinggi diturunkan regulasinya dari NLR_Rendah (Gambar 2C). Jumlah gen yang serupa namun jauh lebih rendah mengalami penurunan regulasi pada NLR_Limfosit yang tinggi dibandingkan dengan neutrofil (Gambar 2D). Data ini menunjukkan bahwa kadar NLR sebagian besar terkait dengan perubahan ekspresi gen pada neutrofil. Selain itu, hal ini perlu dibandingkan dengan pasien dari kelompok penyakitnya NLR_Rendah, bukan Kontrol NLR, karena kelompok penyakit sebelumnya jelas dipisahkan dari NLR_Tinggi tetapi bukan NLR_Kontrol ( Gambar 2B; Gambar tambahan 2).

cistanche tubulosa-meningkatkan sistem kekebalan tubuh
Sebelum menyelidiki perbedaan ekspresi gen dan pengayaan set gen, penelitian tambahan mengkarakterisasi tingkat kontaminasi monosit dalam persiapan neutrofil. Dengan menggunakan data RNA-seq, kami mengamati bahwa ekspresi penanda monosit CD14, CD68, CD83, dan CD163 pada NLR_Tinggi vs NLR_Preparasi neutrofil atau limfosit rendah tidak berbeda secara signifikan. Analisis EPIC terhadap data RNA-seq neutrofil menunjukkan bahwa sel nonimun ("sel lain") dan sel T CD4 merupakan kontaminan utama dalam sediaan neutrofil (Gambar 3). Kecuali untuk NLR{{10}}sel T CD4 rendah dan sel B, tidak ada sel pengkontaminasi lainnya yang berbeda secara signifikan pada NLR_Neutrofil rendah vs NLR_Neutrofil tinggi . Pada sediaan neutrofil, kontaminasi monosit dengan analisis EPIC hanya 0.17% ± 0.05% untuk NLR_Rendah vs 0,1% ± 0,033% untuk NLR_Persiapan tinggi (P=.12). Nilai ini menunjukkan bahwa kontaminasi monosit memiliki tingkat yang lebih rendah bila ditentukan oleh analisis data RNA-seq vs flow cytometry.

Gambar 4. Plot gelembung sebar dari kategori kumpulan gen GO yang diekspresikan secara signifikan untuk proses biologis antara NLR_Tinggi dan NLR_Rendah. Rasio k:K pada absis adalah jumlah gen yang diekspresikan berbeda nyata (k) dibandingkan dengan jumlah total gen pada kategori (K). Ordinatnya adalah signifikansi pengayaan yang dinyatakan dalam log (nilai P). (A) Kumpulan gen GO yang berasal dari neutrofil RNA-seq membandingkan NLR_Tinggi dengan NLR_Rendah. (B) Kumpulan gen GO berasal dari limfosit RNA-seq. Kumpulan gen di sudut kiri bawah kedua plot adalah yang paling tidak signifikan. Kumpulan gen di sudut kanan atas kedua plot adalah yang paling signifikan.

Gambar 4 (lanjutan)
Untuk menguji sifat gen yang diekspresikan secara berbeda, kami melakukan GSEA dengan kategori Gene Ontology (GO) untuk proses biologis menggunakan set gen yang diekspresikan secara berbeda secara signifikan antara NLR_Tinggi dan NLR_Rendah. Hasilnya ditunjukkan pada plot scatter bubble (Gambar 4). Pemisahan kumpulan gen di kanan atas setiap plot menunjukkan (1) tingginya persentase gen dalam kumpulan gen yang mengalami perubahan signifikan dan (2) tingginya tingkat signifikansi dalam pengayaan kumpulan gen. Dalam sampel kami, plot gelembung pencar menunjukkan pengayaan kategori GO respon komplemen dan humoral secara independen untuk neutrofil dan limfosit. Pada neutrofil, set gen untuk jalur klasik aktivasi komplemen, regulasi kaskade aktivasi protein, dan respons imun humoral yang dimediasi oleh sirkulasi imunoglobulin adalah yang paling signifikan dengan persentase tertinggi anggota set gen berubah secara signifikan (Gambar 4A). Secara independen, set gen yang identik dalam limfosit juga diamati memiliki rasio tinggi terhadap gen yang berubah secara signifikan dan tingkat signifikansi seperti pada studi neutrofil (Gambar 4B).
Tabel 2. Kumpulan gen imunologi pada neutrofil dan limfosit

Tabel 2 mencantumkan kumpulan gen imunologi yang mengalami perubahan paling signifikan pada neutrofil (Tabel 2, Panel A) dan limfosit (Tabel 2, Panel B). Penelitian ini membandingkan ekspresi gen pada neutrofil atau limfosit antara NLR_sampel Tinggi dan NLR_sampel Rendah. NLR yang sehat_Sampel kontrol tidak dibandingkan karena tingkat ekspresinya tumpang tindih dengan sampel pasien NLR_Tinggi dan NLR_Rendah di seluruh transkriptom dan kumpulan gen yang diekspresikan secara berbeda secara signifikan. Selain itu, sampel kontrol NLR_yang sehat tidak cocok dalam hal usia, penyakit, dan kondisi pembedahan (Gambar tambahan 1 dan 2). Pada neutrofil (Tabel 2) dan limfosit (Tabel 2), data menunjukkan bahwa ekspresi set gen yang terkait dengan sistem kekebalan berbeda secara signifikan ketika NLR_Tinggi dibandingkan dengan NLR_Rendah . Pada seq RNA, setiap tipe sel mempunyai temuan yang sama dengan tipe sel lainnya. Di kedua panel, tingkat signifikansi set gen utama dimaksimalkan pada P < 1E-24. Data ini sangat signifikan terlepas dari apakah neutrofil atau limfosit diperiksa. Untuk fokus pada area konten yang sangat signifikan dari penyelidikan RNA-seq ini, ekspresi gen imunoglobulin yang diekspresikan secara berbeda diperiksa secara signifikan. Pertama, plot analisis komponen utama gen neutrofil menunjukkan bahwa untuk NLR_Tinggi vs NLR_Rendah, gen imunoglobulin yang diekspresikan secara berbeda secara signifikan dipisahkan menjadi 2 kelompok (Gambar 3A tambahan). Alternatifnya, gen limfosit NLR_Tinggi vs NLR_Rendah tersusun (Gambar 3A tambahan). Selanjutnya, peta panas gabungan ekspresi gen terkait kekebalan antara NLR_Tinggi dengan NLR_Rendah dibandingkan pada neutrofil dan limfosit (Gambar 5). Secara keseluruhan, ketika seluruh peta panas diperiksa, terdapat penurunan regulasi yang jelas pada seluruh kelompok gen imunoglobulin pada kelompok neutrofil NLR_Tinggi dibandingkan dengan NLR_Rendah. Sebagian besar gen (69/156, 44%) terkait dengan imunoglobulin. Hanya 12 dari 156 (7,7%) gen yang berhubungan dengan komplemen: C1QA, C1QB, Serping1, C2, C2R, C4BPA, C3AR1, CR1, CR1L, CFH, CFD, dan CD59. Pada kelompok limfosit, terjadi juga penurunan regulasi pada sebagian besar gen imunoglobulin dalam kategori NLR_Tinggi.
Kumpulan gen komplemen pada neutrofil dan limfosit dirinci pada Tabel 3. Pada neutrofil (Tabel 3) dan limfosit (Tabel 3), ekspresi gen pada 3 set gen yang terkait dengan sistem komplemen sangat berbeda nyata (P < 1E{{ 5}}) ketika NLR_sampel Tinggi dibandingkan dengan NLR_sampel Rendah. Pengamatan ini sama baik perbandingannya antara RNA dari neutrofil atau limfosit. 3 set gen tersebut meliputi aktivasi komplemen, jalur klasik aktivasi komplemen, dan regulasi aktivasi komplemen. Plot analisis komponen utama gen neutrofil sekali lagi menunjukkan bahwa untuk NLR_Tinggi vs NLR_Rendah, gen komplemen yang diekspresikan secara berbeda secara signifikan dipisahkan menjadi 2 kelompok (Gambar 3B tambahan). Atau, gen limfosit NLR_Tinggi vs NLR_Rendah tumpang tindih (Gambar 3B tambahan).

Gambar 5. Peta panas dari gen yang diekspresikan secara berbeda secara signifikan dalam set gen imunoglobulin pada neutrofil (kiri) dan limfosit (kanan). Gen yang tercantum di sebelah kanan setiap peta panas adalah anggota imunoglobulin
Peta panas ekspresi neutrofil dan limfosit dari kumpulan gen terkait komplemen yang membandingkan NLR_Tinggi dengan NLR_Rendah ditunjukkan pada Gambar 6. Pada neutrofil, sejumlah besar gen diturunkan regulasinya dalam NLR_Populasi tinggi. Pada rangkaian gen ini, serupa dengan rangkaian gen imunoglobulin, sebagian besar gen (69/86, 80%) terkait dengan imunoglobulin. Hanya 12 dari 86 (14%) yang merupakan komponen komplemen dan gen pengatur (C1QA, C1QB, SERPING1, C2, CR2, C4BPA, C3AR1, CR1, CR1L, CD59, CFH, dan CFD). Pada kelompok limfosit secara keseluruhan, terdapat lebih sedikit ekspresi gen komplemen, dan gen imunoglobulin sedikit lebih diturunkan regulasinya pada kelompok NLR_Tinggi. Karena terdapat pemahaman yang lebih baik mengenai gen sistem komplemen dibandingkan dengan gen sistem imunoglobulin, perhatian difokuskan pada sistem komplemen sebagai kandidat potensial untuk gen target terkait NLR tinggi dan rendah. Peta panas gabungan yang membandingkan NLR_Tinggi dengan NLR_Rendah telah disiapkan yang menunjukkan ekspresi sistem komplemen dan gen terkait dalam sampel neutrofil dan limfosit (Gambar 7). Secara umum, limfosit bukanlah sistem sel reservoir untuk sistem komplemen. Kebanyakan gen komplemen tidak diregulasi dalam limfosit. Hanya C1S, CR2, C5, C8G, C5, dan CFB yang menunjukkan perbedaan ekspresi antara limfosit NLR_Tinggi dan NLR_Rendah (Gambar 7). CD81 dalam limfosit adalah tetraspanin sel B. Ekspresi C1S dan C8G tampaknya jauh lebih tinggi pada NLR limfosit_Tinggi dibandingkan NLR limfosit_Rendah, mirip dengan KLKB1, gen untuk prekallikrein plasma.
Sebaliknya, pada neutrofil, NLR_Tinggi menunjukkan penurunan regulasi gen komponen komplemen C1QA, C1QB, C1QC, SERPING1, C1R, C4BPA, C3, dan C3AR1, serta gen pengatur komplemennya (penghambatan) CD59, CFB, dan CFI . Hanya gen C2 dan CFD yang diregulasi pada pasien NLR_Tinggi_N. CD59 dan C9 relatif diregulasi dalam neutrofil NLR_Rendah_N dibandingkan dengan NLR_Tinggi_N. FGFR4 adalah reseptor faktor pertumbuhan. CFH ada tetapi tampaknya tidak dipengaruhi oleh neutrofil NLR_Tinggi atau NLR_Rendah. Hal ini lebih tinggi diekspresikan dalam limfosit.

manfaat cistanche untuk pria-memperkuat sistem kekebalan tubuh
Klik di sini untuk melihat produk Cistanche Meningkatkan Imunitas
【Minta lebih lanjut】 Email:cindy.xue@wecistanche.com / Aplikasi WhatsApp: 0086 18599088692 / Wechat: 18599088692
Diskusi
NLR pada jumlah leukosit diferensial telah menjadi penanda sederhana yang banyak digunakan untuk mengenali potensi dampak buruk pada berbagai penyakit, termasuk CVD, tumor padat, dan penyakit inflamasi seperti lupus eritematosus sistemik dan sklerosis sistemik. Dalam penyelidikan retrospektif kami pada pasien dengan CVD aterosklerotik, kami mengamati bahwa pasien dengan NLR tinggi memiliki angka kematian lanjut yang lebih tinggi setelah perbaikan aneurisma aorta elektif, angka stroke/kematian lanjut yang lebih tinggi setelah endarterektomi karotis profilaksis, dan penurunan kelangsungan hidup bebas amputasi setelahnya. revaskularisasi femoral-poplitea elektif jika NLR mereka meningkat.14-16 Investigasi ini dimulai untuk menemukan dasar mekanistik untuk NLR tinggi. limfoma, tumor padat multipel, dan kelainan inflamasi seperti lupus eritematosus sistemik dan sklerosis sistemik. Dalam penyelidikan retrospektif kami pada pasien dengan CVD aterosklerotik, kami mengamati bahwa pasien dengan NLR tinggi memiliki angka kematian lanjut yang lebih tinggi setelah perbaikan aneurisma aorta elektif, angka stroke/kematian lanjut yang lebih tinggi setelah endarterektomi karotis profilaksis, dan penurunan kelangsungan hidup bebas amputasi setelahnya. revaskularisasi femoral-poplitea elektif jika NLR mereka meningkat.14-16 Investigasi ini dimulai untuk menemukan dasar mekanistik untuk NLR tinggi.
Tabel 3. Kumpulan gen komplemen pada neutrofil dan limfosit

Untuk mengembangkan pendekatan yang tidak memihak mengenai mekanisme efek diferensial NLR pada hasil CV, kami melakukan RNA-seq pada neutrofil dan limfosit dari pasien yang sama. Untuk penelitian ini, semua pasien dengan penyakit aorta dikumpulkan secara prospektif dan dikelompokkan ke dalam kategori NLR berdasarkan hasilnya. 6 sampel terakhir di masing-masing dari 2 jenis sel dipilih berdasarkan tingkat RIN tertinggi dalam RNA yang disiapkan dari sampel neutrofil dan limfosit berpasangan tanpa memperhatikan jenis kelamin, usia, atau kondisi medis sebelumnya. Seperti dapat dilihat pada Tabel 1, pasien dalam kelompok NLR_Tinggi dan NLR_Rendah cukup mirip dan hanya dibedakan berdasarkan NLRnya.
Kualitas RNA yang digunakan dalam penelitian ini ditunjukkan oleh RIN dan pemisahan lengkap pola ekspresi gen antara neutrofil dan limfosit pada semua kelompok pasien yang dikumpulkan (NLR tinggi, NLR rendah, dan kontrol) (Gambar 1). Plot analisis komponen utama menunjukkan bahwa NLR_Data kontrol tidak relevan dalam penyelidikan ini karena NLR pasien tumpang tindih dengan NLR_Tinggi dan NLR_Rendah pada populasi neutrofil dan limfosit pasien . Analisis GSEA memberikan wawasan yang luar biasa mengenai kumpulan gen mana yang diperkaya dalam kumpulan gen GO dalam proses biologis, dan plot gelembung pencar dengan jelas menunjukkan hal ini dengan memplot signifikansi log vs rasio jumlah gen yang diubah terhadap jumlah total gen. dalam kumpulan gen. Ketika ditinjau, kumpulan gen yang memisahkan diri dari seluruh daftar adalah kumpulan gen yang berada dalam sistem imunitas dan komplemen humoral (imunoglobulin) (Tabel 2 dan 3) berdasarkan rasio dan signifikansi statistik dalam pendekatan penemuan yang tidak memihak.
Banyaknya gen imunoglobulin imunitas humoral yang terlibat sulit untuk dikerjakan karena perbedaan penting antara gen-gen ini tidak diketahui dengan baik. Alternatifnya, lebih banyak yang diketahui tentang sistem komplemen, dan fokus pada sistem komplemen klasik yang diaktifkan oleh imunoglobulin adalah target yang dapat dikenali untuk peradangan dan penyakit yang berhubungan dengan imunoglobulin. Data kami menunjukkan bahwa gen komponen komplemen klasik C1QA, C1QB, C1R, CR1, C1S, SERPING1, C2, C4BPA, C3 C3AR1, C8G, C9, dan beberapa gen pengatur (CD59, CFB CFI, dan CFH) diturunkan regulasinya dalam neutrofil pasien. dengan NLR tinggi (Gambar 7). Temuan ini mengejutkan karena 3 alasan. Pertama, gen yang terlibat sebagian besar berasal dari jalur komplemen klasik. Kedua, pada pasien dengan NLR tinggi, gen komplemen ini sebagian besar mengalami penurunan regulasi dibandingkan dengan pasien dengan NLR rendah. Terakhir, lebih banyak F12 yang diekspresikan dalam neutrofil dari sampel NLR_Tinggi dibandingkan dengan sampel NLR_Rendah. Bentuk enzimatik dari produk protein F12 (faktor XII [FXII]) mengaktifkan jalur klasik komplemen dan neutrofil.20 Sebaliknya, PLG, gen untuk plasminogen dan aktivator FXII, mengalami penurunan regulasi dalam limfosit dan neutrofil dari pasien dalam NLR{ {21}}Tinggi, menunjukkan bahwa aktivasi FXII itu sendiri mungkin merupakan pengatur aktivasi komplemen.
Selain itu, sistem komplemen klasik telah terbukti terlibat dalam percepatan CVD. Komponen komplemen 1q (C1q) merupakan faktor awal dari jalur komplemen, yang memiliki peran penting baik dalam sistem imun bawaan maupun didapat.21 C1q telah terbukti memiliki peran ganda, efek positif dan negatif pada aterosklerosis.22 Dalam studi klasik jalur komplemen, C1q memiliki peran protektif dalam aterosklerosis tahap awal dengan mengatur sinyal molekul makrofag melalui jalur komplemen-independen, memodulasi penyerapan lipoprotein aterogenik, memediasi sel-sel apoptosis, dan eliminasi sisa-sisa sel.23,24 Sebuah studi terbaru oleh Jia et al23 menunjukkan bahwa penurunan serum C1q dikaitkan dengan CAD. Studi lain yang dilakukan oleh Guo et al24 menunjukkan bahwa peningkatan aktivitas C1q dikaitkan dengan CAD. Yang terakhir, penelitian terbaru menunjukkan bahwa pasien diabetes dengan penurunan C1q memiliki kelangsungan hidup yang lebih pendek.25 Data ini menunjukkan bahwa pemeriksaan sistem komplemen mungkin penting dalam memahami patogenesis CVD yang dimediasi peradangan.

Gambar 6. Peta panas dari gen-gen yang diekspresikan secara berbeda secara signifikan dalam kumpulan gen komplemen pada neutrofil (kiri) dan limfosit (kanan). Gen-gen yang tercantum di sebelah kanan setiap peta panas adalah anggota kumpulan gen komplemen. RNA berasal dari neutrofil atau limfosit yang dikumpulkan dari pasien dengan NLR tinggi (NLR_Tinggi) atau rendah (NLR_Rendah). Enam sampel individu dari NLR_Tinggi dibandingkan dengan 6 sampel individu dari NLR_Rendah dari neutrofil dan limfosit.

Gambar 7. Peta panas gabungan komplemen dan gen terkait dari neutrofil atau limfosit NLR_Tinggi atau NLR_Rendah. Di setiap kategori, peta panas komposit disiapkan dari 6 sampel RNA-seq individu dari setiap jenis sel.
Recently, a retrospective investigation of the data from the CANTOS, JUPITER, SPIRE-1, SPIRE-2, and CIRT trials on 60 087 patients was conducted to determine whether NLR predicts major adverse CV events and is modified by anti-inflammatory therapy.26 NLR modestly correlated (ie, r 2 ≤ 0.26) with interleukin 6, C-reactive protein, and fibrinogen levels but minimally with lipids.25 In all 5 trials, NLR predicted incident CV events and death in patients with NLR >3.08.26 Meskipun penurunan lipid tidak berdampak pada NLR, terapi anti-inflamasi dengan canakinumab, penghambat interleukin 1 menurunkan NLR (P <0,0001).26 Data ini menunjukkan bahwa NLR mungkin merupakan penanda CVD yang tidak bergantung pada lipid dan pengaruh statin. Analisis ad hoc terhadap beberapa percobaan prospektif acak ini menunjukkan bahwa NLR mungkin merupakan faktor risiko independen terhadap mortalitas pada CVD.
Ada beberapa keterbatasan dalam penelitian ini. Persiapan neutrofil kami memiliki 4% limfosit dan 2% kontaminasi monosit melalui flow cytometry. Karena neutrofil tidak diketahui mensintesis imunoglobulin, perubahan gen imunoglobin neutrofil mungkin disebabkan oleh kontaminasi sel B. Pada analisis EPIC, terdapat peningkatan signifikan pada kontaminasi sel B pada sampel NLR-Low. Pengamatan ini menunjukkan bahwa peningkatan kadar gen imunoglobulin pada NLR_Sampel neutrofil rendah mungkin timbul dari kontaminasi sel B. Jadi, berkurangnya gen imunoglobulin pada NLR_sampel Tinggi mungkin disebabkan oleh peningkatan sel B pada NLR_Sampel rendah dan belum tentu berkurangnya kadar gen imunoglobulin pada NLR_sampel Tinggi. Demikian pula, neutrofil tidak diketahui sebagai sel penghasil komplemen. Kontaminasi dua persen dengan monosit bisa menjadi sumber gen komplemen. Namun, dengan menggunakan data sekuen RNA, kami mengamati bahwa tidak ada perbedaan yang signifikan dalam kontaminasi monosit pada sediaan neutrofil antara NLR_Rendah dan NLR_Tinggi. Lebih lanjut, melakukan analisis EPIC terhadap data RNA-seq menunjukkan adanya kontaminasi monosit<0.1% (<1:1000) of the neutrophil preparations, indicating that the RNA-seq was unlikely influenced by contaminating monocytes (Figure 3). The contaminating B cells in the NLR_Low samples do not influence the complement data observed. Finally, even now, it is not known that the changes we observed in complement and immunoglobulin genes are specific to vascular surgery patients with high NLR or older patients in general. NLR and genetic studies need to be performed on healthy age- and sex-matched patients without CVD.

manfaat cistanche untuk pria-memperkuat sistem kekebalan tubuh
Singkatnya, temuan utama dalam penelitian ini adalah, pada kondisi NLR tinggi, banyak gen komponen komplemen dan beberapa regulatornya mengalami penurunan regulasi dalam neutrofil. Tidak jelas mengenai arti keseluruhan dan keadaan aktivasi dari gen komplemen yang teregulasi ke bawah yang teridentifikasi. Karena rangkaian gen komplemen sangat menurun, kami berspekulasi bahwa individu dengan NLR_Kelangsungan hidup pascaoperasi yang tinggi dan pendek akan kehilangan mekanisme perlindungan CV utama yang disediakan oleh sistem komplemen. Penilaian ini perlu diperiksa secara prospektif dalam penyelidikan klinis untuk mengetahui mekanisme yang mendasari hasil ini.
Referensi
1. Ross R. Aterosklerosis – penyakit inflamasi. N Engl J Med. 1999;340(2):115-126.
2. Dapatkan GS. Seri tinjauan tematik: sistem kekebalan dan aterogenesis. Fungsi kekebalan dalam aterogenesis. J Lipid Res. 2005;46(1):1-10.
3. Hansson GK, Hermansson A. Sistem imun pada aterosklerosis. Nat Imunol. 2011;12(3):204-212.
4. Duffy BK, Gurm HS, Rajagopal V, Gupta R, Ellis SG, Bhatt DL. Kegunaan peningkatan rasio neutrofil terhadap limfosit dalam memprediksi kematian jangka panjang setelah intervensi koroner perkutan. Apakah J Cardiol. 2006;97(7):993-996.
5. Tamhane UU, Aneja S, Montgomery D, Rogers EK, Eagle KA, Gurm HS. Hubungan antara rasio neutrofil dan limfosit masuk dan hasil pada pasien dengan sindrom koroner akut. Apakah J Cardiol. 2008;102(6):653-657.
6. Gibson PH, Croal BL, Cuthbertson BH, dkk. Rasio neutrofil-limfosit pra operasi dan hasil pencangkokan bypass arteri koroner. Am Heart J. 2007;154(5):995-1002.
7. Fici F, Celik T, Balta S, dkk. Efek perbandingan nebivolol dan metoprolol pada lebar distribusi sel darah merah dan rasio neutrofil/limfosit pada pasien dengan hipertensi esensial yang baru didiagnosis. Farmakol J Cardiovasc. 2013;62(4):388-393.
8. Karaman M, Balta S, Ay SA, dkk. Efek komparatif valsartan dan amlodipine pada Tingkat vWf dan rasio N/L pada pasien dengan hipertensi yang baru didiagnosis. Clin Exp Hipertensi. 2013;35(7):516-522.
9. Uthamalingam S, Patvardhan EA, Subramanian S, dkk. Utilitas rasio neutrofil terhadap limfosit dalam memprediksi hasil jangka panjang pada gagal jantung dekompensasi akut. Apakah J Cardiol. 2011;107(3):433-438.
10. Bhat TM, Afari SAYA, Garcia LA. Rasio limfosit neutrofil pada penyakit pembuluh darah perifer: tinjauan. Pakar Rev Cardiovasc Ada. 2016;14(7):871-875.
11. Bhutta H, Agha R, Wong J, Tang TY, Wilson YG, Walsh SR. Rasio neutrofil-limfosit memprediksi kelangsungan hidup jangka menengah setelah operasi vaskular besar elektif: studi cross-sectional. Bedah Vasc Endovasc. 2011;45(3):227-231.
12. Appleton ND, Bailey DM, Morris-Stiff G, Lewis MH. Rasio neutrofil terhadap limfosit memprediksi mortalitas perioperatif setelah perbaikan elektif terbuka pada aneurisma aorta perut. Bedah Vasc Endovasc. 2014;48(4):311-316.
13. Mandi J, Smith JB, Kruse RL, Vogel TR. Rasio neutrofil-limfosit memprediksi tingkat keparahan penyakit dan hasil setelah prosedur ekstremitas bawah. J Vasc Bedah. 2020;72(2):622-631.
14. Raja AH, Schmaier AH, Harth KC, dkk. Peningkatan rasio neutrofil-limfosit memprediksi mortalitas setelah perbaikan aneurisma endovaskular elektif. J Vasc Bedah. 2020;72(1):129-137.
15. Raja AH, Kim AH, Kwan S, dkk. Peningkatan rasio neutrofil terhadap limfosit dikaitkan dengan hasil yang lebih buruk setelah endarterektomi karotis pada pasien tanpa gejala. J Stroke Cerebrovasc Disc. 2021;30(12):106120.
16. Raja AH, Kwan S, Schmaier AH, dkk. Peningkatan rasio neutrofil terhadap limfosit dikaitkan dengan penurunan kelangsungan hidup bebas amputasi setelah revaskularisasi perkutan femoropopliteal. Int Angiol. 2021;40(5):442-449.
17. Racle J, de Jonge K, Baumgaertner P, Speiser DE, Gfeller D. Pencacahan kanker dan tipe sel imun secara simultan dari data ekspresi gen tumor massal. Elife. 2017;6:e26476.
18. Trapnell C, Roberts A, Goff L, dkk. Analisis ekspresi gen dan transkrip diferensial dari eksperimen RNA-seq dengan TopHat dan Cufflinks. Protokol Nat. 2012;7(3):562-578.
19. Palmer C, Diehn M, Alizadeh AA, Brown PO. Profil ekspresi gen spesifik tipe sel leukosit dalam darah tepi manusia. Genomik BMC. 2006;7:115.
20. Stavrou EX, Fang C, Bane KL, dkk. Faktor XII dan uPAR meningkatkan fungsi neutrofil untuk mempengaruhi penyembuhan luka. J Clin Investasikan. 2018;128(3): 944-959.
21. Dunkelberger JR, Lagu WC. Komplemen dan perannya dalam respon imun bawaan dan adaptif. Resolusi Sel. 2010;20(1):34-50.
22. Speidl WS, Kastl SP, Huber K, Wojta J. Komplemen dalam aterosklerosis: teman atau musuh? J Tromb Haemost. 2011;9(3):428-440.
23. Jia Y, Wen W, Yang Y, dkk. Peran klinis gabungan serum C1q dan hsCRP dalam memprediksi penyakit arteri koroner. Klinik Biokimia. 2021;93:50-58.
24. Guo S, Mao X, Li X, Ouyang H, Gao Y, Ming L. Aktivitas komplemen serum C1q dikaitkan dengan penyakit arteri koroner obstruktif. Med Kardiovaskular Depan. 2021;8:618173.
25. Cavusoglu E, Kassotis JT, Anwar A, dkk. Kegunaan komplemen C1q untuk memprediksi kematian 10-tahun pada pria penderita diabetes melitus yang dirujuk untuk angiografi koroner. Apakah J Cardiol. 2018;122(1):33-38.
26. Adamstein NH, MacFadyen JG, Rose LM, dkk. Rasio neutrofil-limfosit dan kejadian kejadian aterosklerotik: analisis dari lima uji coba acak kontemporer. Euro Heart J. 2021;42(9):896-903.
