Ekstraksi Asam Fenolik, Flavonol, Dan Flavan-3-ols Dengan Bantuan Ultrasound Dari Kulit Dan Biji Anggur Muscadine Menggunakan Pelarut Eutectic Dalam Alami Dan Pemodelan Prediktif Dengan Jaringan Syaraf Tiruan
Feb 23, 2022
Mohon hubungi{0}}untuk informasi lebih lanjut
AbstrakTujuan dari penelitian ini adalah untuk mengetahui efisiensi ekstraksi 9 pelarut eutektik alami dalam (NDES) dengan bantuan ultrasound untukasam fenolik, flavonol, dan flavan-3-ol dalam kulit dan biji anggur muscadine (Carlos) dibandingkan dengan etanol 75 persen. Jaringan saraf tiruan (JST) diterapkan untuk mengoptimalkan kadar air NDES, waktu ultrasonikasi, rasio padat-pelarut, dan suhu ekstraksi untuk mencapai hasil ekstraksi tertinggi untuk asam ellagic, katekin, dan epikatekin. NDES (#1) yang baru diformulasikan terdiri dari kolin klorida:asam levulinat: etilen glikol 1:1:2 dan 20 persen air mengekstrak jumlah asam ellagic tertinggi di kulit pada 22,1 mg/g. Hasil ini adalah 1,73-kali lipat dari 75 persen etanol. NDES yang dimodifikasi (#3) yang terdiri dari kolin klorida: prolin: asam malat 1:1:1 dan 30 persen air mengekstrak jumlah katekin tertinggi (0.61 mg/g) dan epikatekin (0,89 mg/g) di kulit, dan 2,77 mg/g dan 0,37 mg/g di biji, masing-masing. Hasil optimal asam ellagic pada kulit menggunakan NDES #1 adalah 25,3 mg/g (diamati) dan 25,3 mg/g (diprediksi). Hasil optimal (catechin plus epicatechin) dalam benih menggunakan NDES #3 adalah 9,8 mg/g (diamati) dan 9,6 mg/g (prediksi). Studi ini menunjukkan efisiensi ekstraksi yang tinggi dari NDES terpilih untuk polifenol dalam kondisi yang dioptimalkan.

Silakan klik di sini untuk tahu lebih banyak
pengantar
Pelarut eutektik dalam alami (NDES) dibuat dengan mencampur donor ikatan hidrogen dengan akseptor ikatan hidrogen pada rasio molar yang sesuai [1]. Titik leleh salah satu komponen harus lebih rendah dari titik leleh komponen lainnya [1]. Setelah dipanaskan dan dicampur, media ini menjadi cair pada suhu kamar. Air ditambahkan untuk menstabilkan dan mempolarisasi campuran. Penelitian di bidang ekstraksi fitokimia menggunakan NDES telah berkembang karena kemampuan ekstraksi dan kelarutannya yang efektif. Meskipun demikian, beberapa faktor memainkan peran penting ketika membandingkan NDES dengan pelarut organik, termasuk hasil, biaya, pemulihan, dan toksisitas. Penelitian sebelumnya menyelidiki NDES pada ekstraksi polifenol yang berbeda dari berbagai matriks makanan. Misalnya, Bubalo dkk. (2016) membandingkan 5 NDES, air, 70 persen metanol (v/v), dan 70 persen metanol (v/v) diasamkan untuk mengekstrak antosianin, katekin, dan quercetin-3-O-glukosida dari kulit anggur merah. NDES yang terdiri dari kolin klorida: asam oksalat (1:1) dengan 25 persen air (v/v) ditemukan sebagai pelarut ekstraksi yang paling efisien [2]. Dalam studi lain, Pani´c et al. (2019) menguji 8 NDES dan mengasamkan 70 persen etanol dan mengamati kolin klorida: asam sitrat (2:1) dengan 30 persen air (v/v) sebagai NDES terbaik untuk mengekstrak antosianin dari buah anggur pomace [3]. Anggur muscadine (Vitis rotundifolia) berasal dari negara bagian tenggara dan anggur liar pertama yang dibudidayakan di Amerika Serikat [4]. Anggur muscadine diproduksi di 12 negara bagian dan totalnya sekitar 5000 hektar [5]. Ada 100 varietas anggur muscadine dan masing-masing memiliki karakteristik fisik, sensorik, atau kimia yang berbeda [4]. Di antara mereka, Carlos adalah anggur muscadine yang banyak ditanam karena hasil panennya yang tinggi dan konsistensi pertumbuhannya [4]. Anggur Carlos muscadine berukuran sedang, berwarna perunggu, kulitnya lebih tebal dan rata-rata mengandung empat biji. Anggur muscadine mengandung sejumlah besarpolifenolyang diketahui dapat mengurangi peradangan [7], menghambat pertumbuhan tumor prostat [8], dan meningkatkan respons metabolik penderita diabetes [9]. Pomace anggur muscadine, produk sampingan dari jus anggur muscadine atau pembuatan anggur, terdiri dari kulit dan biji. Sebuah studi penelitian sebelumnya menggunakan aseton: air: campuran asam asetat (70:29.7:0.3, v/v) untuk mengekstrak senyawa fenolik dari biji, kulit, dan pulp dari delapan kultivar anggur muscadine yang tumbuh di Florida, termasuk Carlos [10]. Namun, penggunaan pelarut organik yang mudah terbakar dan efisiensi ekstraksi yang rendah menghambat aplikasi praktis. Sebagian besar pomace anggur muscadine masih dibuang sebagai limbah. Jaringan saraf tiruan (JST) adalah sistem pemetaan nonlinier yang terdiri dari berbagai unit pemrosesan dasar yang dihubungkan oleh asosiasi berbobot. Unit pemrosesan ini disebut "neuron" [11]. Jaringan syaraf tiruan adalah pendekatan pembelajaran mesin untuk memprediksi atau meramalkan suatu respon berdasarkan beberapa input [11]. Penelitian sebelumnya telah menerapkan metode permukaan respon (RSM) untuk optimasi ekstraksi dan prediksi. Namun, beberapa penelitian telah menggunakan JST untuk tujuan yang sama. Misalnya, Sinha et al. (2013) menyatakan bahwa ANN memiliki kinerja prediksi yang lebih baik daripada RSM pada ekstraksi pewarna alami dari biji Bixa Orellana (Annatto) [12]. Dalam penelitian serupa, Ciric et al. (2020) melaporkan bahwa model JST lebih baik daripada RSM untuk memprediksi ekstraksi senyawa fenolik dari bawang putih [13]. Penelitian ini bertujuan untuk mengetahui efisiensi ekstraksi 9 NDES untuk asam fenolat, flavonol, dan flavan{17}}ol dibandingkan dengan etanol 75 persen dengan bantuan ultrasound. ANN diterapkan untuk memprediksi dan mengoptimalkan kondisi ekstraksi pada hasil fenolik. Hipotesisnya adalah bahwa NDES dengan komposisi spesifik mengekstrak jumlah asam fenolik, flavonol, dan flavan{19}} yang lebih tinggi daripada etanol 75 persen, dan efisiensi ekstraksi tertinggi dapat dicapai dengan pemodelan prediktif berbasis JST.
2. Bahan dan Metode 2.1. Bahan kimia dan reagen Kolin klorida, asam levulinat, 1,2-propanediol, asam DL-malat, asam oksalat, asam klorida, dan asam format diperoleh dari Acros Organics (Morris Plains, NJ, USA). Asam laktat, etilen glikol, glisin, asetonitril tingkat HPLC, metanol, dan etanol dibeli dari Fishers Scientific (Waltham, Massachusetts, USA). L-prolin dan betaine hidroklorida dibeli dari Alfa Aesar (Ward Hill, MA, USA). Standar tingkat HPLC untuk asam ellagic, asam galat, asam ferulic, ( plus )-catechin, (− )-epicatechin, myricetin, quercetin, dan kaempferol diperoleh dari Sigma Aldrich (St. Louis, MO, USA).

2.2. Desain NDESNDES #1–2 pada Tabel 1 dirancang dalam penelitian kami sebelumnya [14]. Kolin klorida dalam NDES #1–2 dipilih sebagai akseptor hidrogen, sedangkan dua donor hidrogen yang berbeda dipilih untuk setiap NDES baru. Rasio molar antara donor hidrogen dan akseptor dan kadar air ditentukan dalam percobaan awal. NDES #3-9 pada Tabel 1 dipilih dari literatur karena penelitian sebelumnya telah menunjuk mereka sebagai NDES yang efektif dalam mengekstraksi polifenol. Kandungan air dalam NDES #3 dimodifikasi dari literatur yang dikutip. Sebuah metode pemanasan diterapkan untuk mempersiapkan NDES [15]. Secara singkat, akseptor ikatan hidrogen dicampur dengan masing-masing komponen donor ikatan hidrogen dalam labu Erlenmeyer dengan batang pengaduk. Campuran dalam labu ditutup dan dipanaskan pada suhu 50 C selama sekitar 30 menit atau sampai terbentuk cairan bening dan tetap stabil pada suhu kamar. Kadar air pada Tabel 1 dihitung menurut volume akhir campuran NDES. PH NDES yang tercantum dalam Tabel 1 diukur menggunakan pH meter (AB15, Accumet, Fisher Scientific, Waltham, MA, USA). 2.3. Persiapan sampel / Ekstraksi dengan bantuan ultrasound Kulit dan biji anggur muscadine beku (Vitis rotundifolia) (kultivar: Carlos) disediakan oleh Paulk Vineyards (Wray, Georgia, USA). Setelah membuang kulit, daun, atau tangkai daun, pomace dipisahkan menjadi biji dan kulit. Sampel kemudian dikeringkan menggunakan oven vakum (Isotemp, Model 285A, Fisher Scientific, Waltham, Massachusetts, USA) pada 60 C dan tekanan vakum lebih rendah dari − 30 in.Hg. Selanjutnya, sampel dihomogenisasi menjadi serbuk halus menggunakan chimerical grinder (A1{{105}}00, RRH Inc., 2800 W, Zhejiang, China). Menggunakan rasio padat-pelarut awal 1:20 (g: mL), 0,50 g baik kulit anggur muscadine atau biji dicampur dalam 10 mL NDES atau 75 persen etanol dalam rangkap tiga. Sampel kemudian ditempatkan dalam penangas air (60 C) dan disonikasi (VCX 1500, Sonics & Materials Inc., 1500-Watt, 50/60 Hz, Newtown, CT, USA) selama 30 menit pada 100 persen amplitudo untuk dua putaran (15 menit/putaran). Selanjutnya, sampel segera disentrifugasi (Sorvall ST 8, Fisher Scientific, Suzhou, China) pada 3.260 g sampai diperoleh supernatan yang jernih. Terakhir, supernatan dikumpulkan dan disimpan dalam freezer 20 C untuk analisis HPLC asam fenolik (asam ellagic, asam galat, asam ferulat), flavonol (myricetin, quercetin, dan kaempferol), dan flavan{45}}ol (katekin dan epikatekin). 2.4. Analisis HPLC dari asam fenolat, flavonol, dan flavan-3-ol Asam fenolik, flavonol, dan flavan-3-ol dianalisis pada sistem HPLC (Agilent Technologies 1200, Waldbronn, Jerman) menurut metode yang dijelaskan dalam Sandhu dan Gu (2013) [16]. Sistem HPLC terdiri dari pompa biner, autosampler, kompartemen kolom termostat, detektor array dioda, dan detektor fluoresensi. Kulit anggur atau ekstrak biji dihidrolisis sebelum analisis asam fenolik dan flavonol. Hidrolisis dilakukan dengan mencampurkan 1 ml ekstrak dengan 4 ml larutan hidrolisis (1,2 M HCI mengandung 50 persen metanol) dan ditempatkan dalam penangas air (Precision, Model 2837, 400 W, 50/60 Hz, Thermo Scientific, Marietta , OH, USA) pada 90 C selama 80 menit. Selanjutnya, sampel didinginkan hingga 25 C diikuti dengan sonikasi selama 5 menit. Hidrolisis ekstrak tidak diperlukan untuk analisis katekin dan epikatekin. Ekstrak terhidrolisis dan tidak terhidrolisis disaring melalui membran polytetrafluoroethylene (PTFE) 0,45 m sebelum analisis HPLC. Untuk menganalisis asam ellagic, asam galat, asam ferulic, myricetin, quercetin, kaempferol, catechin, dan epicatechin, 10 L disuntikkan ke dalam kolom SB-C18 (4,6 × 250 mm, 5 m, Zorbax, Agilent, Santa Clara, CA, AMERIKA SERIKAT). Fase gerak adalah (A) 0,5 persen asam format dan (B) 100 persen asetonitril. Laju aliran adalah 1 mL/menit dengan gradien modifikasi 25 menit sebagai berikut: 0–5 menit, 10–30 persen B; 5-10 menit, 30-40 persen B; 10–20 menit, 40–50 persen B; 20–25 menit, 50–10 persen B; diikuti dengan 5 menit kesetimbangan. Suhu kolom diatur pada 30 C. Panjang gelombang pendeteksian adalah 260 nm untuk asam ellagic, asam galat, dan asam ferulic dan 360 nm untuk myricetin, quercetin, dan kaempferol pada detektor photodiode array. Eksitasi dan emisi untuk katekin dan epikatekin masing-masing adalah 230 nm, 321 nm, menggunakan detektor fluoresensi. Senyawa polifenol dikuantifikasi menggunakan kurva standar asam ellagic, asam galat, asam ferulat, myricetin, quercetin, kaempferol, catechin, dan epicatechin. Semua kurva standar memiliki 7 poin dan R2 > 0,99. 2.5. Desain khusus untuk jaringan saraf tiruan Empat variabel ekstraksi independen dengan empat level: kadar air (15–60 persen ), waktu ultrasonikasi (5–35 menit), rasio padat-ke-pelarut (1:5–1:20), dan ekstraksi suhu (30-60 C) (Tabel S1) diterapkan untuk mengoptimalkan hasil ekstraksi asam fenolik, flavonol, dan flavan-3-ol. Berbeda dengan desain klasik seperti desain permukaan respons, desain berbasis JST tidak memerlukan pengulangan dan lebih menyukai struktur data yang berbeda. Dalam penelitian kami sebelumnya [14], JST adalah metode yang lebih dapat diandalkan untuk memprediksi hasil ekstraksi daripada RSM. Oleh karena itu, JST dipilih dalam penelitian ini untuk memprediksi rendemen ekstraksi asam ellagic, catechin, dan epicatechin. Desain yang disesuaikan dengan 40 proses (Tabel S2) dibuat di JMP Pro (Versi 14.2, SAS Institute Inc., Cary, NC, USA) untuk menyediakan data khusus untuk pemodelan prediktif JST. Pengacakan dari 40 run diterapkan untuk menghilangkan bias apapun. Persamaan utama JST ditunjukkan sebagai berikut:=jj=1 wh jpg ditambah bhk, k=1toK (1) di mana h adalah jumlah neuron pada lapisan tersembunyi, j dan k adalah jumlah variabel input dan neuron tersembunyi, masing-masing, p adalah variabel input, bh adalah bias dari lapisan tersembunyi, dan wh adalah bobot pada lapisan tersembunyi. Hasil ekstraksi asam ellagic, catechin, dan epicatechin terhadap keempat variabel bebas dianalisis menggunakan JST dengan melatih data terlebih dahulu kemudian memilih jenis aktivasi terbaik dan jumlah neuron yang menghasilkan kesesuaian data yang memadai. Untuk mengevaluasi keberhasilan model prediksi, tiga nilai telah dinilai: R-kuadrat, akar kuadrat dari kesalahan prediksi kuadrat rata-rata (RASE) (persamaan (2)), dan kesalahan absolut rata-rata (AAE). RASE adalah RASE=SSE/n (2) Di mana SSE menyumbang kuadrat dan menjumlahkan kesalahan prediksi (perbedaan antara respons aktual dan respons yang diprediksi) dan n untuk sejumlah pengamatan. R-kuadrat mendekati 1 dengan RASE dan AAE mendekati nol berarti kecocokan data yang lebih tinggi ke dalam model. 2.6. Statistik Ekstraksi hasil asam fenolat, flavonol, dan flavan-3-ol dibandingkan dengan ANOVA satu arah diikuti dengan uji-t Student pada p Kurang dari atau sama dengan 0,05 menggunakan JMP Pro (Versi 14.2, SAS Institute Inc., Cary, NC, AS). Masing-masing nde dan etanol 75 persen dibandingkan menggunakan uji Dunnett pada p Kurang dari atau sama dengan 0,05. Analisis komponen utama (PCA) dilakukan pada JMP Pro (Versi 14.2, SAS Institute Inc., Cary, NC, USA) untuk senyawa fenolik yang diekstraksi dari kulit dan biji anggur muscadine. 3. Hasil dan Pembahasan 3.1. Polifenol yang diekstraksi oleh NDES dari kulit anggur muscadine Sembilan NDES dan 75 persen etanol digunakan untuk ekstraksi polifenol dari kulit anggur muscadine. Tabel 2 menunjukkan hasil ekstraksi asam ellagic, asam galat, asam ferulat, myricetin, quercetin, kaempferol, catechin, dan epicatechin. Asam ellagic adalah polifenol yang dapat diekstraksi paling melimpah di kulit anggur, diikuti oleh asam galat dan asam ferulat. Temuan ini konsisten dengan penelitian sebelumnya [17,18]. NDES #1, #8, #7, #3, #2 dan #9 mengekstraksi asam ellagic dalam jumlah yang jauh lebih tinggi pada kulit anggur daripada etanol 75 persen. Hasil ekstraksi asam ellagic tertinggi dicapai oleh NDES #1 diikuti oleh NDES #8 pada masing-masing 22,1 ± 2,2 mg/g dan 21,3 ± 2,5 mg/g (Tabel 2). Namun, tidak ada perbedaan yang signifikan antara NDES #1 dan NDES #8 menurut uji-t Student. Menariknya, NDES #1 ditemukan sebagai NDES yang paling tidak efektif untuk mengekstrak antosianin dari
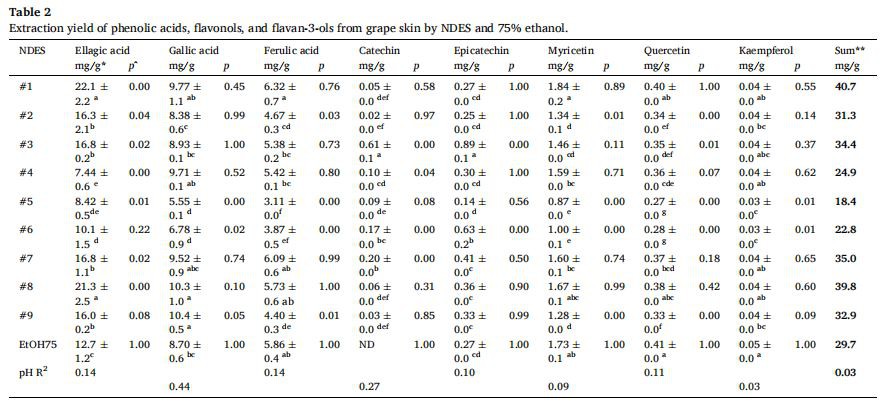
cranberry pomace [14]. Hal ini menunjukkan bahwa NDES #1 dapat secara selektif mengekstrak asam ellagic atau ellagitannins dari matriks makanan yang juga mengandung antosianidin. Selektivitas tersebut dapat dikaitkan dengan perbedaan dalam interaksi molekuler antara NDES dan kelas fenolik tertentu. Gambar S1 (panel A) menunjukkan kromatogram HPLC dari asam galat, asam ellagic, dan asam ferulat yang diekstraksi dari kulit anggur oleh NDES #1 dan terdeteksi pada 260 nm. Etanol 75 persen mengekstraksi 12,7 ± 1,2 mg asam ellagic per gram kulit anggur. Hasil ekstraksi terendah dari asam ellagic diamati pada NDES #4 sebesar 7,44 ± 0,6 mg/g. Hasil ekstraksi asam galat oleh NDES #9, #8, #1, #4, #7, dan #3 sebanding dan secara signifikan lebih tinggi dari 75 persen etanol. Jumlah asam galat tertinggi diekstraksi oleh NDES #9 sebesar 10.4 ± 0.5 mg/g, sedangkan jumlah terendah sebesar 5,55 ± {{40}} .1 mg/g diekstraksi dengan NDES #5. Jumlah asam ferulat tertinggi diekstraksi oleh NDES #1 sebesar 6,32 ± 0.7 mg/g dan jumlah terendah diekstraksi oleh NDES #5 sebesar 3,11 ± 0.{{5{{52 }}}} mg/g. Selanjutnya, tidak ada perbedaan yang signifikan antara NDES #1 dan etanol 75 persen dalam mengekstraksi asam ferulat (Tabel 2). Jumlah katekin dan epikatekin tertinggi diekstraksi oleh NDES #3 sebesar 0.61 ± 0.1 mg/g dan 0.89 ± 0.1 mg/ g, masing-masing (Tabel 2). Sementara itu, NDES #3 dan #6 mengekstrak jumlah epikatekin secara signifikan lebih besar daripada etanol 75 persen. Gambar S2 (panel A) menunjukkan kromatogram HPLC dari katekin dan epikatekin yang diekstraksi oleh NDES #3 dari kulit anggur. Namun, katekin tidak terdeteksi dalam ekstrak etanol 75 persen. Jumlah katekin terendah (0.02 mg/g) dan epikatekin ({{90}}.14 mg/g) diekstraksi dengan NDES #2 dan NDES # 5, masing-masing. Myricetin adalah flavonol yang paling melimpah dan kaempferol adalah yang paling sedikit. Uji Dunnett mengungkapkan bahwa NDE dan 75 persen etanol sebanding dalam mengekstraksi myricetin, quercetin, dan kaempferol (Tabel 2). Jumlah myricetin tertinggi diekstraksi oleh NDES #1 (1,84 mg/g), diikuti oleh etanol 75 persen (1,73 mg/g), dan kemudian NDES #8 (1,67 mg/g). Jumlah kuersetin tertinggi diekstraksi oleh etanol 75 persen (0.41 mg/g), NDES #1 (0.40 mg/g), dan NDES #8 ({ {143}}.38 mg/g). Sebaliknya, jumlah terendah myricetin dan quercetin diekstraksi oleh NDES #5 pada 0.87 mg/g dan 0.27 mg/g, masing-masing. Temuan ini lebih lanjut menekankan kemampuan NDES #5 yang lemah secara keseluruhan untuk mengekstrak polifenol dari kulit anggur. Jumlah kaempferol tertinggi diekstraksi dengan etanol 75 persen (0.05 mg/g), dan terendah diekstraksi oleh NDES #5 dan NDES#6 (0,03 mg/g). Gambar S1 (panel B) menunjukkan kromatogram HPLC dari myricetin, quercetin, dan kaempferol yang diekstraksi dari kulit anggur oleh NDES #1 yang terdeteksi pada 360 nm. Jumlah tertinggi asam fenolat, flavonol, dan flavan-3- ols adalah 40,7 mg/g yang diekstraksi dengan NDES #1 diikuti oleh 39,8 mg/g yang diekstraksi dengan NDES #8, sedangkan jumlah terendah adalah 18,4 mg/g yang diekstraksi oleh NDES #5 (Tabel 2). PH NDES berkisar antara 0,3 dan 3,3 (Tabel 1). Korelasi Rkuadrat antara pH NDE dan asam fenolat, flavonol, dan hasil flavan{119}}ol tercantum dalam Tabel 2. Kurangnya korelasi antara pH dan hasil ekstraksi menunjukkan pH tidak berdampak pada efisiensi ekstraksi. 3.2. Polifenol yang diekstraksi oleh NDES dari biji anggur muscadine Hasil ekstraksi keseluruhan asam fenolik, flavonol, dan flavan{123}}ol dari biji anggur terlihat lebih rendah daripada yang berasal dari kulit (Tabel 3). Polifenol yang paling banyak diekstraksi dalam biji adalah katekin dan epikatekin, sedangkan kaempferol tidak terdeteksi. Matriks biji kompleks yang mengandung minyak (13 persen , b/b basa kering) adalah penjelasan yang mungkin dari rendahnya kemampuan ekstrak senyawa fenolik dari biji anggur [19]. Jumlah katekin tertinggi diekstraksi oleh NDES #3 sebesar 2,77 mg/g (Tabel 3). Hasil ini secara signifikan lebih tinggi daripada semua NDES dan etanol 75 persen lainnya. Gambar S2 (panel B) menunjukkan kromatogram HPLC katekin dan epikatekin yang diekstraksi oleh NDES #3 dari biji anggur. Jumlah katekin terendah diekstraksi oleh NDES #5 pada 0,30 mg/g. Semua NDES kecuali NDES #1, #2, dan #9 mengekstrak jumlah epikatekin secara signifikan lebih tinggi daripada etanol 75 persen (Tabel 3). Konsentrasi epikatekin tertinggi diekstraksi dengan NDES #4 (0,71 mg/g) dan NDES #5 (0,68 mg/g), sedangkan terendah diekstraksi dengan etanol 75 persen (0,11 mg/g). Asam galat adalah asam fenolat yang paling banyak diekstraksi dalam biji anggur, diikuti oleh asam ferulat dan asam ellagic. Jumlah asam galat tertinggi diekstraksi oleh NDES #4 sebesar 0,45 mg/g, diikuti oleh NDES #9 dan NDES #8. NDE ini mengekstraksi asam galat dalam jumlah yang jauh lebih tinggi daripada etanol 75 persen. Jumlah terendah asam galat (0,2 mg/g) diekstraksi dengan NDES #3. Ekstraksi tertinggi

hasil asam ellagic diperoleh dengan NDES #9 (0.26 mg/g) diikuti oleh NDES #6 (0.17 mg/g), yang secara signifikan lebih tinggi dari 75 persen etanol. Demikian pula, NDE #3 mengekstraksi jumlah asam ellagic terendah pada 0.05 mg/g. Selain itu, NDES #6, #7, dan #3 mengekstraksi asam ferulat dalam jumlah yang jauh lebih tinggi daripada etanol 75 persen. Hasil ekstraksi asam ferulat terendah adalah 0.5 mg/g oleh NDES #5. Selanjutnya, asam ferulat tidak terdeteksi pada ekstrak NDES #9. Hal ini kemungkinan karena kelarutan asam ferulat lebih rendah pada NDES #9 dibandingkan dengan NDE lainnya. Ekstrak myricetin tertinggi diperoleh etanol 75 persen dan NDES #7 sebesar 0,18 mg/g, yang lebih tinggi dari semua NDE. Hasil ekstraksi kuersetin tertinggi adalah dengan NDES #6 (0,14 mg/g) dan NDES #3 (0,13 mg/g) dan kedua NDES lebih baik dari 75 persen etanol. Demikian pula, pH NDES tidak mempengaruhi hasil ekstraksi seperti yang ditunjukkan oleh korelasi rendah (R-kuadrat) antara pH NDE dan hasil asam fenolik, flavonol, dan flavan-3-ol yang tercantum pada Tabel 3. 3.3 . Analisis komponen utama (PCA) dilakukan untuk mengasosiasikan hasil ekstraksi berbagai senyawa fenolik dalam kulit dan biji anggur dengan NDE dan 75 persen etanol (Gbr. 1). PCA dilakukan pada matriks korelasi untuk mendeteksi kemungkinan selektivitas beberapa NDE terhadap ekstraksi senyawa atau kelompok fenolik tertentu. Sekitar 85 persen varians data kulit dijelaskan oleh komponen utama 1 dan 2. Plot pemuatan (Gbr. 1B) menunjukkan korelasi yang tinggi antara asam fenolik (asam ellagic, asam galat, asam ferulat) dan flavonol (myricetin, quercetin, dan kaempferol). Untuk mengekstrak kelompok ini, pelarut terbaik adalah NDES #1, #8, #7, dan etanol 75 persen seperti yang ditunjukkan pada plot skor (Gbr. 1A). Sementara itu, katekin dan epikatekin tampak terpisah dari kelompok fenolik lainnya. Seperti yang ditunjukkan pada Gambar. 1A, NDES #3 selektif untuk mengekstrak katekin dan epikatekin dari kulit anggur. Ini adalah pengamatan yang menarik karena NDES#3 termasuk NDES yang paling tidak efektif untuk mengekstrak proanthocyanidins, yang merupakan oligomer dan polimer catechin dan epicatechin [14]. Hal ini menunjukkan bahwa NDES #3 mungkin selektif terhadap proanthocyanidins dengan ukuran molekul yang lebih kecil. Pengelompokan senyawa fenolik pada plot pemuatan kulit (Gbr. 1B) berbeda dari biji (Gbr. 1D) terlepas dari rendahnya hasil senyawa ini dalam biji anggur. Komponen utama pertama dan kedua menjelaskan sekitar 73 persen varians data benih. Quercetin, myricetin, dan asam ferulic diekstraksi lebih efisien dengan NDES #6, #7, dan etanol 75 persen, seperti yang ditunjukkan pada plot skor (Gbr. 1C). Asam ellagic dan asam galat diekstraksi lebih efektif dengan NDES #9. Sekali lagi, katekin diekstraksi dengan efisiensi tertinggi oleh NDES #3 yang serupa dengan yang diamati dengan kulit anggur. Epicatechin diekstraksi dengan efisiensi yang lebih tinggi oleh NDES #5, #4, dan NDES #8.

3.4. Optimalisasi ekstraksi asam fenolik dan flavonol dari kulit anggur muscadine dan pemodelan prediksi ANN Kolin klorida: asam levulinat: etilen glikol 1:1:2 (NDES #1) menunjukkan hasil ekstraksi tertinggi untuk asam ellagic, dan oleh karena itu dipilih untuk optimasi lebih lanjut dan ramalan. Dampak dari empat faktor, termasuk kadar air, waktu ultrasonikasi, rasio padat-pelarut, dan suhu ekstraksi dinilai untuk ekstraksi asam fenolik dan flavonol. Selanjutnya, empat level untuk setiap faktor ekstraksi diterapkan dalam total 40 proses acak. Hasil ekstraksi eksperimental asam ellagic, asam galat, asam ferulat, myricetin, dan quercetin, bersama dengan jumlah dari lima ini, ditunjukkan pada Tabel 4. Secara keseluruhan, kisaran perbedaan hasil ekstraksi antara terendah dan tertinggi relatif besar untuk asam fenolik. Misalnya, hasil terendah untuk asam ellagic adalah 9,03 mg/g (run #17) dan tertinggi adalah 25,3 mg/g (run #15), yang menghasilkan perbedaan 16,2 mg/g (lari #17). Selain itu, jumlah hasil terendah adalah 20,7 mg/g, dan tertinggi adalah 71,5 mg/g. Ini menggambarkan dampak signifikan dari tingkat yang berbeda dari setiap faktor ekstraksi pada hasil ekstraksi. Jalankan #15 mengekstrak jumlah asam ellagic tertinggi. Kondisi ekstraksi run #15 adalah kadar air 45 mL /10{{130}} mL, ultrasonikasi 25 menit, rasio padat-pelarut 1:10 (g: mL) , dan suhu ekstraksi 60 C. Gambar S3 menunjukkan kromatogram HPLC dari asam fenolat yang dioptimalkan yang diekstraksi dari kulit anggur oleh NDES #1 (jalankan#15 pada Tabel 4). Asam galat tertinggi (18,7 mg/g) dicapai pada kondisi ekstraksi pada run #24 dan terendah 6,63 mg/g pada run #40. Untuk asam ferulic, run #22 mengekstrak jumlah tertinggi pada 19,2 mg/g, sedangkan tidak ada asam ferulic yang terdeteksi pada run #14, #17, #29, dan #34. Run #22 diekstraksi dengan kadar air 60 mL/100 mL, ultrasonikasi 5 menit, rasio padat-pelarut 1:5, dan suhu ekstraksi 60 C. Run #2 mengekstrak myricetin tertinggi (10,1 mg/g) dan quercetin (1,87 mg/g). Kondisi ekstraksi run #2 adalah kadar air 60 mL/100 mL, ultrasonikasi 35 menit, rasio padat-pelarut 1:20, dan suhu ekstraksi 60 C. Hasil tertentu saya yang terendah (3,79 mg/g) diekstraksi dengan run#40. Plot kontur pada Gambar. 2 menunjukkan pengaruh parameter ekstraksi (X1, X2, X3, dan X4) pada hasil prediksi asam ellagic yang diekstraksi oleh NDES #1 dari kulit anggur. Hasil prediksi asam ellagic pada Tabel 4 digunakan untuk membangun plot penghitungan ini. Setiap panel menggambarkan dampak dari 2 parameter ekstraksi. Garis kontur diberi label dengan hasil asam ellagic (mg/g). Perkiraan kadar air optimum adalah sekitar 35-45 mL/100 mL NDES, seperti yang ditunjukkan pada Gambar. 2B dan 2C. Waktu ultrasonikasi yang lebih lama meningkatkan hasil asam ellagic (Gbr. 2D dan 2E), yang menunjukkan peran penting sonikasi dalam ekstraksi NDES. Selama ekstraksi, pencampuran kulit anggur atau biji dengan NDES memperkenalkan partikel dan gas, yang menambahkan situs kavitasi akustik untuk ultrasound untuk menghasilkan banyak gelembung kecil di NDES. Meledaknya gelembung-gelembung ini menyebabkan suhu ekstrem, perbedaan tekanan, gaya geser tinggi, turbulensi makro, dan pencampuran mikro, yang secara efektif mengaduk NDES untuk mempercepat difusi dan transfer massa. Ketika gelembung kavitasi meledak pada permukaan biji anggur atau partikel kulit, mikro-jet yang dihasilkan dan tumbukan antar partikel menyebabkan pengelupasan permukaan, erosi, kerusakan partikel, sonoporasi, dan gangguan sel [20]. Semua efek mekanis dari kavitasi yang diinduksi ultrasound ini mengintensifkan penetrasi NDE ke interior sel sehingga fenolik antar sel dari matriks makanan dipindahkan ke dalam pelarut. Rasio padat-pelarut yang optimal adalah 1:10, seperti yang ditunjukkan oleh Gambar. 2B, 2D, dan 2F. Terakhir, suhu ekstraksi yang lebih tinggi hingga 60 C tampaknya memiliki efek positif pada kemampuan ekstraksi asam ellagic seperti yang ditunjukkan pada Gambar 2C, 2E, dan 2F. Hal ini menunjukkan hubungan langsung antara suhu ekstraksi dan hasil asam ellagic yang diekstraksi dari kulit anggur. Hasil ekstraksi asam ellagic (Tabel 4) dianalisis untuk pemodelan prediksi menggunakan jaringan saraf tiruan. Data eksperimen secara acak dibagi menjadi set pelatihan dan set validasi. Alasan untuk memasukkan validasi yang ditetapkan oleh perangkat lunak statistik adalah untuk menekan overfitting. Untuk memprediksi hasil asam ellagic (Y), empat faktor ekstraksi independen yang sama (X1, X2, X3, dan X4), 1-2 lapisan tersembunyi dengan jumlah neuron yang berbeda, dan tiga fungsi aktivasi dinilai. Fungsi aktivasi yang diterapkan adalah tangen hiperbolik, linier, dan gaussian. Selanjutnya, dataset dilatih sampai nilai R-kuadrat tinggi untuk pelatihan dan validasi tercapai. Data prediksi dan model dihasilkan. Struktur JST terbaik dipilih dengan menganalisis empat input (X1, X2, X3, dan X4) dengan satu lapisan tersembunyi menggunakan fungsi Gaussian dengan sepuluh neuron (Gambar S5). R-kuadrat set pelatihan dan validasi adalah 0,99, sedangkan RASE dan AAE model masing-masing adalah 0,062 dan 0,044. R-kuadrat validasi JST asam ellagic dalam penelitian ini (0,99) lebih tinggi dari validasi JST procyanidins (0,95) dan antosianin (0,91) pada penelitian sebelumnya [14]. Namun, peningkatan R2 ini dapat dikaitkan dengan kecocokan model yang dihasilkan lebih baik dari data dalam penelitian ini, yang dapat disebabkan oleh kesalahan eksperimental yang lebih kecil. Model JST prediktif untuk ekstraksi asam ellagic menggunakan NDES #1 ditunjukkan sebagai persamaan 3–13:

Cistanche untuk meningkatkan kekebalan
Kesimpulan
Temuan saat ini menyajikan bukti lebih lanjut tentang efektivitas kemampuan NDES untuk mengekstrak polifenol dari produk sampingan industri makanan. Hasilnya mendukung hipotesis ekstraksi NDES yang dibantu ultrasound lebih dari 75 persen etanol. NDES secara efektif mengekstraksi tiga asam fenolik, dua flavonol, dan tiga flavan-3-ol dari kulit dan biji anggur. NDES #1 adalah NDES yang paling efektif untuk mengekstrak asam ellagic, sedangkan NDES #3 sangat selektif terhadap ekstraksi catechin dan epicatechin. Kelemahan NDES yang nyata adalah viskositasnya yang tinggi, yang menghadirkan tantangan selama penanganan dan pemulihan. Dalam penelitian ini, jaringan saraf tiruan, terlepas dari keterbatasan hasil, menunjukkan pendekatan praktis untuk pemodelan prediktif. NDE adalah media yang kuat untuk memulihkan fitokimia dari sistem pangan. Beberapa NDE juga menghadirkan pelarut yang kurang beracun untuk mempelajari fitokimia ini dalam sel hidup [21,22]. Akhirnya, pelarut eutektik dalam alami adalah media ekstraksi alternatif yang efektif untuk pelarut organik.

Referensi
[1] W. Bi, M. Tian, KH Row, Evaluasi pelarut eutektik dalam berbasis alkohol dalam ekstraksi dan penentuanflavonoiddengan optimasi metodologi respon permukaan, J. Chromatogr. A 1285 (2013) 22–30, https://doi.org/10.1016/j. chroma.2013.02.041.
[2] M. Cvjetko Bubalo, N. Curko, M. Tomaˇsevi´c, K. Kovaˇcevi´c Ghani's, I. Radojˇci´c Redovnikovic, Ekstraksi hijau fenolat kulit anggur dengan menggunakan pelarut eutektik dalam, Food Chem. 200 (2016) 159–166, https://doi.org/10.1016/j. foodchem.2016.01.040.
[3] M. Panic, V. Gunjevi´c, G. Cravotto, I. Radojˇci´c Redovnikovic, Mengaktifkan teknologi untuk ekstraksi antosianin anggur-pomace menggunakan pelarut eutektik alami yang dalam dalam batch hingga setengah liter ekstraksi antosianin anggur-pomace menggunakan NADES, Food Chem. 300 (2019) 125185, https://doi.org/ 10.1016/j.foodchem.2019.125185.
[4] M. Hoffmann, dkk., Panduan Produksi Anggur Muscadine untuk Tenggara, Universitas Negeri Carolina Utara, Publikasi Ekstensi Negara Bagian NC, 2020 https://content. ces.ncsu.edu/muscadine-grape-production-guide (diakses 18 Januari 2021). [5] Cline, B. dan C. Fisk, Tinjauan areal anggur muscadine, kultivar dan area produksi di AS tenggara. Lokakarya Anggur Muscadine untuk Agen Penyuluh Koperasi, di Konsorsium Buah Kecil Wilayah Selatan. 2006: Konsorsium Buah Kecil Wilayah Selatan.
[6] PC Andersen A. Sarkhosh D. Huff J. Breman 2020 6 10.32473/edis-hs100-2020.
[7] P. Greenspan, et al., Sifat antiinflamasi dari anggur muscadine (Vitis rotundifolia), J. Agric. Makanan. Kimia 53 (22) (2005) 8481–8484, https://doi.org/ 10.1021/jf058015.
[8] DN Ignacio, KD Mason, EC Hackett-Morton, C. Albanese, L. Ringer, WD Wagner, PC Wang, MA Carducci, SK Kachhap, CJ Paller, J. Mendonca, L. Li Ying Chan, Bo Lin, DK Hartle, JE Green, CA Brown, TS Hudson, ekstrak kulit anggur Muscadine menghambat sel kanker prostat dengan menginduksi penghentian siklus sel dan mengurangi migrasi melalui heat shock protein 40, Heliyon 5 (1) (2019) e01128, https://doi .org/10.1016/j.heliyon.2019.e01128.
