Nikotin Memperparah Cedera Ginjal yang Diinduksi Tacrolimus Dengan Kematian Sel Terprogram
Mar 23, 2022
Kontak:{0}}/ WhatsApp: 008618081934791
Yu Ji Jiang, Sheng Cui, Kang Luo, Jun Ding
PENGANTAR
Meskipun penemuan imunosupresan baru, tacrolimus (TAC) tetap menjadi landasan rejimen imunosupresif dalam transplantasi organ padat. Namun, penggunaan jangka panjang TAC meningkatkan risiko efek samping (misalnya, nefrotoksisitas, neurotoksisitas, infeksi, keganasan, diabetes, dan keluhan gastrointestinal) [1]. Di antaranya, akutginjalcederaatau nefrotoksisitas TAC kronis telah dilaporkan pada 46 persen penerima transplantasi paru [2] dan 22,4 persen penerima transplantasi ginjal [3]. Sementara akutginjalcederadianggap reversibel setelah pengurangan dosis TAC atau penghentian total, nefrotoksisitas kronis, yang menyebabkan hilangnya allograft, tidak dapat diubah. Nefrotoksisitas TAC kronis ditandai dengan glomerulopati, hyalinosis arteriol aferen, dan striped tubulointerstitial fibrosis (TIF) [4]. Meskipun mekanisme pasti dari dilema klinis ini masih belum diketahui, kami baru-baru ini menunjukkan bahwa peradangan yang berasal dari stres oksidatif, faktor pertumbuhan transformasi 1 (TGF- 1), dan kematian sel terprogram mungkin merupakan pemain penting [5]. Merokok merupakan tantangan kesehatan masyarakat yang kritis dan beban keuangan masyarakat yang mengurangi kualitas hidup. Laporan epidemiologis menunjukkan bahwa saat ini ada lebih dari satu miliar perokok di seluruh dunia dan enam juta kematian setiap tahun karena penggunaan tembakau. Angka ini meningkat, terutama di negara berkembang atau tidak berkembang [6]. Diakui dengan baik bahwa merokok merupakan faktor risiko untuk berbagai jenis kanker, kejadian kardiovaskular (infark miokard dan stroke), dan penyakit paru obstruktif. Di ginjal, merokok meningkatkan keparahan disfungsi ginjal pada pasien dengan diabetes, hipertensi, polikistikginjalpenyakit, dan pasca transplantasi ginjal [7]. Selain itu, merokok juga dapat menyebabkan kerusakan ginjal de novo bahkan pada populasi yang sehat tanpa penyakit ginjal kronis (CKD) yang sudah ada sebelumnya [8]. Penelitian ini berusaha untuk mengevaluasi: (1) apakahnikotin(NIC), komponen toksik utama dari merokok, memperburuk cedera ginjal yang diinduksi TAC; dan, jika demikian, (2) mekanisme mana yang bertanggung jawab atas NIC(nikotin)-percepatan nefrotoksisitas.

cistanches herbal dapat meringankan fungsi ginjal
HASIL
Efek NIC(nikotin)pada parameter dasar
Tabel 1 menguraikan efek NIC(nikotin)pada parameter dasar pada kelompok eksperimen. Kedua NIC(nikotin)dan TAC meningkatkan UV (poliuria), yang selanjutnya ditingkatkan oleh NIC(nikotin)dan pengobatan TAC. Tidak ada NIC(nikotin)maupun TAC mencegah hilangnya BW. Ekskresi protein urin, Scr, BUN, dan Cys-C secara nyata lebih tinggi di kedua NIC(nikotin)dan kelompok TAC dibandingkan dengan kelompok VH; tingkat ini semakin meningkat dengan kombinasi kedua obat, menyiratkan bahwa NIC(nikotin)mempercepat disfungsi ginjal yang diinduksi TAC. Tidak ada perbedaan signifikan antara kelompok SBP. Perawatan TAC empat minggu meningkatkan konsentrasi TAC darah menjadi 11,0±og ng/mL, sementara NIC(nikotin) did not influence blood TAC concentration(12.8±15 ng/mL,p>o.o5 vs. TAC). Selain itu, mengobati tikus normal dengan NIC(nikotin)mengakibatkan konsentrasi kotinin serum dan urin meningkat masing-masing sebesar 56,5±17 ng/mL dan 8;6±192,6 ug/hari. Konsentrasi kotinin serum dan urin ini mirip dengan yang diamati pada manusia yang merupakan perokok aktif [13].
Tabel 1. Pengaruh NIC(nikotin)pada parameter fungsional

Efek NIC(nikotin)pada histopatologi pada nefrotoksisitas TAC kronis
Nefrotoksisitas TAC kronis ditandai dengan gambaran histologis yang unik termasuk TIF bergaris dan glomerulopati. Dengan pewarnaan histologis dan mikroskop elektron, kami menemukan bahwa cedera glomerulus yang disebabkan oleh TAC dimanifestasikan oleh penebalan basement glomerulus dan penipisan prosesus kaki podosit (Gambar IA, IC, dan D), ini mungkin terkait dengan peningkatan ekskresi protein urin. Pada analisis kuantitatif, baik NIC(nikotin)dan TAC meningkatkan area mesangial fraksional, dengan peningkatan lebih lanjut diamati di NIC(nikotin)dan grup TAC. Perubahan utama pada nefrotoksisitas TAC kronis terbatas pada area tubulointerstitial, seperti yang digambarkan oleh deposisi fibrosa tubulointerstitial, atrofi tubular, dan fibrosis bergaris (Gbr.1B, 1E, dan F). Angka dengan jelas menunjukkan bahwa skor TIF di NIC(nikotin)plus TACgroup lebih tinggi daripada di NIC(nikotin)grup atau grup TAC.
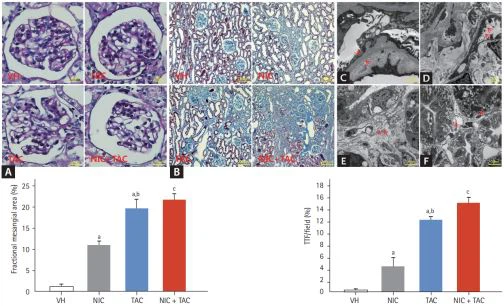
Gambar 1. Fotomikrograf representatif dari asam-Schiff periodik (PAS)(A), Masson trichrome (B), mikroskop elektron transmisi (CF), dan analisis kuantitatif cedera glomerulus dan fibrosis tubulointerstitial (TIF); (C) penebalan membran basal glomerulus (panah); (D) penipisan kaki podosit proses (panah);(E)pembengkakan tubulointerstitium dan deposisi kolagen yang luas (menyebar);(F) tubulus atrofi (panah).VH, kendaraan; NIC(nikotin), nikotin; TAC, takrolimus. p
Efek NIC(nikotin)pada ekspresi sitokin profibrotik pada nefrotoksisitas TAC kronis
Penelitian ini berusaha membandingkan ekspresi sitokin profibrotik TGF- 1 dan CTGF, dan komponen matriks ekstraseluler (ECM) dari ig-h; antara kelompok eksperimen. Konsisten dengan temuan TIF, NIC(nikotin)ekspresi berlebih yang diinduksi TAC dari TGF pro-fibrotik- 1dan CTGF dan ECM ig-h3(Gbr.2)

Gambar 2. Fotomikrograf representatif dari analisis imunoblottinguntuk(A)transforming growth factor 1 (TGF-B1),(B TGF- -diinduksi gen-h( ig-h3), dan (C) faktor pertumbuhan jaringan ikat (CTGF). Nilai untuk ekspresi protein diwakili menggunakan grup kendaraan (VH) sebagai referensi 1oo persen dan dinormalisasi menjadi -aktin(nikotin), nikotin;TAC, takrolimus. 3p
Efek NIC(nikotin)pada peradangan pada nefrotoksisitas TAC kronis
Untuk menentukan efek NIC pada peradangan pada cedera ginjal yang diinduksi TAC, kami mempelajari ekspresi mediator proinflamasi dan gen terkait piroptosis dengan imunoblotting dan imunohistokimia. Gambar 3 menunjukkan bahwa pengobatan TAC meregulasi ekspresi sitokin terkait piroptosis (ⅡL-1, IL-18, dan NLRP3) dan MCP-1, menghasilkan ED-1-positif infiltrasi sel, dan peningkatan lebih lanjut ditemukan dengan pengobatan gabungan NIC(nikotin)dan TAC.

Gambar 3. Fotomikrograf representatif imunohistokimia untuk displasia ektodermal-1 (ED-1)(A) dan analisis imunoblot untuk sitokin proinflamasi (B). VH, kendaraan; NIC(nikotin), nikotin; TAC, takrolimus; MCP-1, protein kemotaktik monosit-1;IL, interleukin; NLRP3, protein yang mengandung domain pyrin reseptor mirip NOD3. p
Efek NIC(nikotin)pada stres oksidatif pada nefrotoksisitas TAC kronis
Seperti yang ditunjukkan pada Gambar.4, kronis(nikotin)Pengobatan TAC terkait erat dengan ketidakseimbangan antara oksidan dan enzim antioksidan [12,14. Analisis imunoblotting menunjukkan bahwa NIC meregulasi ekspresi NOX-2 dan NOX-4 yang diinduksi TAC tetapi menekan ekspresi SOD1 dan SOD2. Selain itu, kadar serum dan urin 8-OHdG, penanda stres oksidatif, lebih tinggi pada kelompok NIC dan TAC dibandingkan dengan kelompok VH dan tertinggi pada kelompok NIC plus TAC. Temuan ini menyiratkan efek sinergis NIC dan TAC pada stres oksidatif dalam model ini.

Gambar 4. Fotomikrograf representatif dari analisis imunoblotting dari serangkaian protein terkait stres oksidatif (A) dan serum (B) dan urin (C)Konsentrasi 8-hidroksi-2'-deoksiguanosin (8-OHdG). VH, kendaraan; NIC(nikotin), nikotin; TAC, tacrolim-kita; SOD, superoksida dismutase; NOX,NADPH oksidase.Bp
Efek NIC(nikotin)pada kematian sel terprogram pada nefrotoksisitas TAC kronis
Baik kematian sel terprogram tipe I (apoptosis) atau tipe II (autophagy) terlibat dalam patogenesis cedera ginjal kronis yang diinduksi TAC [1s]. Menggunakan uji TUNEL, kami mengamati bahwa sebagian besar sel TUNEL-positif atau badan apoptosis terlokalisasi pada sel epitel tubulus dan sel endotel vaskular interstisial, di mana atrofi tubulus dan TIF tipikal berkembang (Gbr.5A). Analisis kuantitatif menunjukkan bahwa kedua NIC(nikotin) dan TAC secara signifikan meningkatkan sel TUNEL-positif dibandingkan dengan kelompok VH; ini lebih jelas pada kelompok NIC plus TAC. Pada tingkat molekuler, penambahan NIC(nikotin)pada tikus yang diobati dengan TAC menghasilkan disregulasi signifikan ekspresi Bcl-2/Bax dan cleaved caspase-3 menuju kematian sel (Gbr. 5B). Selain itu, mikroskop elektron menunjukkan bahwa pengobatan TAC menginduksi pembentukan kompartemen autophagic yang melimpah, seperti vakuola autophagic awal (AVi), vakuola autophagic degradatif (Avd), dan mitofag (suatu bentuk autophagy selektif) di NIC, TAC, dan NIC ditambah grup TAC (Gbr. 6). Imunoblotting kuantitatif mengungkapkan bahwa ekspresi berlebih dari protein p62, LC3B, PINK1, dan Parkin yang terlihat pada ginjal tikus yang diobati dengan TAC semakin meningkat dengan NIC (Gbr.6G dan 6H).
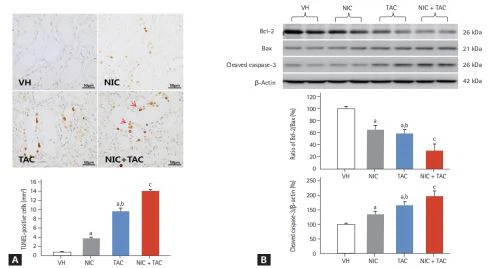
Gambar 5. Fotomikrograf representatif dari uji dUTP-biotin nick end labeling (TUNEL) yang dimediasi TdT(A) dan analisis imunoblotting untuk gen pengontrol apoptosis (B).Nikotinpengobatan meningkatkan sel TUNEL-positif (panah) di ginjal tikus yang diobati dengan tacro-limus.VH, kendaraan; NIC(nikotin),nikotin; TAC, takrolimus; Bcl, B-sellimfoma; Bax, Bcl2-terkait X. p
Efek NIC(nikotin)pada disfungsi mitokondria pada nefrotoksisitas TAC kronis
Dengan mikroskop elektron transmisi, kami dengan jelas mengamati bahwa kedua NIC(nikotin)dan TAC menghancurkan arsitektur mitokondria, seperti yang diilustrasikan oleh pengurangan ukuran dan jumlah mitokondria, krista yang tidak teratur, vakuolisasi, fusi, pembentukan mitofag, dan mitokondria dibagi menjadi dua atau tiga pembelahan organel anak (Gbr.6). Hasil analisis kuantitatif menunjukkan bahwa NIC(nikotin) pengobatan lebih lanjut menurunkan jumlah dan ukuran mitokondria dibandingkan dengan pengobatan NIC atau TAC saja. Analisis imunoblotting mengungkapkan bahwa disregulasi protein terkait mitokondria (OPA1 dan Drpi) yang diinduksi oleh Nicor TAC diperburuk oleh pemberian bersama NIC dan TAC (Gbr. 6).

Gambar 6. Mikrograf elektron transmisi representatif dari autophagy dan morfologi mitokondria(AF), analisis imunoblot (G, H), dan kuantisasi jumlah dan ukuran mitokondria pada setiap kelompok perlakuan. (A) Pembentukan autophagy di ginjal tacrolimus (TAC) dan/ataunikotin(NIC) tikus yang dirawat (panah); (B) kompartemen autophagic yang mengandung mitokondria, ginjal 'TAC dan/atau NIC(nikotin)tikus yang dirawat (mitofag, panah); (C) mitokondria normal; (D) berkurangnya jumlah mitokondria di ginjal TAC dan/atau NIC(nikotin)tikus yang diberi perlakuan;(E) fusi mitokondria terlihat pada ginjal tikus yang diobati dengan TAC dan/atau NIC (lingkaran);(F) mitokondria dibagi menjadi dua atau lebih organel anak pada ginjal tikus yang diberi TAC dan/atau NIC (fisi, lingkaran) . VH, kendaraan;LC3B, rantai ringan 3B;PINK1, fosfat dan ketegangan homolog dihapus pada kromosom sepuluh kinase 1;OPA, protein atrofi optik; Drp, protein terkait dinamin.p

fisetintentangginjal
Efek NIC(nikotin)pada stres retikulum endoplasma pada nefrotoksisitas TAC kronis
Seperti ditunjukkan pada Gbr.7, Nicor TAC menginduksi degranulasi ribosom, sisterna terputus dan melebar, dan vakuolisasi peroksisom dalam retikulum endoplasma kasar (ER), sedangkan struktur ER halus tetap hampir normal (Gbr.7B). Analisis imunoblotting mengungkapkan bahwa baik NIC(nikotin)atau TAC meningkatkan ekspresi gen terkait stres ER termasuk CHOP, Bip, IRE-1 , dan ATF-6, tetapi ekspresinya semakin meningkat dengan kombinasi keduanya (Gbr.7C).

Gambar 7. Fotomikrograf representatif dari mikroskop elektron transmisi (A, B) dan analisis imunoblotting gen yang berhubungan dengan stres retikulum endoplasma (ER) (C).(A) RE kasar normal (panah); (B) degranulasi ribosom, sisterna terputus dan melebar, dan dilatasi vesikel RE kasar dinikotin(NIC) dan/atau tacrolimus(TAC)-diperlakukan ginjal tikus. VH, kendaraan; CHOP, protein homolog C/EBP; Bip, mengikat protein imunoglobulin; IRE-1c, protein yang membutuhkan inositol-1c; ATF, mengaktifkan faktor transkripsi. p< o.01="" vs.vh,="">
DISKUSI
Merokok merupakan faktor risiko penting yang dapat dimodifikasi untuk perkembangan CKD pada populasi sehat dan pasien dengan penyakit yang mendasarinya (misalnya, diabetes, hipertensi). Uji klinis menunjukkan bahwa merokok meningkatkan ekskresi albumin urin dan mempengaruhi fungsi ginjal [16]; selain itu, berhenti merokok dapat meningkatkan proteinuria pada pasien dengan CKD dan diabetes tipe 2 dan memperlambat perkembangan penyakit ginjal stadium akhir [1-,18]. Selain itu, baik perokok penerima atau donor berkontribusi terhadap episode penolakan dan nefropati allograft kronis, yang menyebabkan hilangnya allograft pada transplantasi ginjal [19,2o]. Efek merusak dari merokok ini (NIC(nikotin)) dicerminkan oleh penelitian pada model hewan pengerat nefrektomi s/6 [2al dan nefropati diabetik [o]. Dalam penelitian ini, kami menemukan bahwa NIC(nikotin)area mesangial fraksional yang diinduksi TAC dan TIF. Perubahan patologis ini menyebabkan gangguan fungsi ginjal yang lebih nyata dan meningkatkan ekskresi protein urin. Berdasarkan hasil ini dan laporan lainnya, kami menyarankan bahwa merokok dapat mempercepat kehilangan allograft ginjal pada penerima transplantasi yang menerima imunosupresan berbasis TAC.
Peradangan memainkan peran penting dalam evolusi nefrotoksisitas TAC kronis karena mendahului jaringan parut ginjal yang sedang berlangsung. Peningkatan mediator proinflamasi sebagai respons terhadap rangsangan yang merugikan dapat merekrut sel-sel inflamasi, yang pada gilirannya mengekspresikan sitokin proinflamasi dan profibrotik secara berlebihan seperti kemoatraktan, molekul adhesi, dan TGF- 1. Kami baru-baru ini menunjukkan bahwa NLRP3-inflammasome independen dan dependen terlibat dalam patogenesis nefrotoksisitas TAC kronis [s]. Hasil kami menunjukkan bahwa pemberian NIC(nikotin)pada tikus yang diobati dengan TAC memperkuat ekspresi gen terkait piroptosis (NLRP3, IL-1, dan I-18), mediator proinflamasi MCP-1, dan sitokin profibrotik TGF- dan CTGF, terhadap masuknya sel-sel positif ED-1-yang berlebihan dan peningkatan regulasi ig-h; tanggapan ini mencerminkan tingkat keparahan cedera glomerulus dan tubulus. Temuan kami konsisten dengan Arany et al. [22] dan Agarwal et al [23], yang menunjukkan efek NIC pada peradangan ginjal dan fibrosis.
Meskipun NIC(nikotin)Eksaserbasi berbasis nefrotoksisitas TAC kronis dalam model ini mungkin multifaktorial, kemungkinan terkait dengan dampak stres oksidatif. Telah diketahui dengan baik bahwa pengobatan TAC kronis terkait erat dengan hipoksia terkait arteriolopati aferen, yang selanjutnya terkait dengan stres oksidatif, yang pada gilirannya mengaktifkan ekspresi berlebih TGF- 1 profibrotik, yang menyebabkan fibrosis. Konstruksi ini didukung oleh pengamatan bahwa terapi antioksidan (misalnya, koenzim Q10) melemahkan ekspresi TGF- 1 dan TIF melalui pelestarian integritas mitokondria pada nefrotoksisitas TAC kronis 24]. Baru-baru ini, banyak bukti dari studi in vitro menunjukkan hubungan timbal balik antara paparan NIC kronis dan stres oksidatif dalam berbagai cedera ginjal [o,25,26. Di sini, kami menemukan bahwa NIC meningkatkan kadar 8-OHdG serum dan urin dan meningkatkan ekspresi protein oksidan, sementara itu menekan ekspresi protein antioksidan, sehingga meningkatkan stres oksidatif yang diinduksi TAC serta fibrosis. Memang, kejengkelan NIC pada ginjal yang diobati dengan TAC dalam penelitian ini dapat dikaitkan dengan stres oksidatif.

disfungsi ereksi cistanche
Ada kemungkinan juga bahwa baik apoptosis (kematian sel terprogram tipe I) dan autophagy (kematian sel terprogram tipe II) terlibat dalam NIC(nikotin)- nefrotoksisitas TAC kronis yang dipercepat. Seperti yang diilustrasikan sebelumnya, NIC secara langsung menginduksi podosit dan apoptosis sel tubulus proksimal ginjal [27,28]; itu juga secara tidak langsung menginduksi kematian sel apoptosis melalui stres oksidatif[2g] atau aktivasi TGF- 1[22].NIC(nikotin)juga dapat menginduksi autophagy dalam sel stellata pankreas Bo], miosit jantung tikus neonatus 31], dan sel otot polos pembuluh darah 32]. Dengan demikian, stres oksidatif dan kematian sel terprogram saling terkait. Menggunakan uji TUNEL dan mikroskop elektron, kami dengan jelas mengamati bahwa NIC secara signifikan meningkatkan jumlah sel TUNEL-positif dalam sel epitel tubular, sel endotel vaskular interstisial, dan kompartemen autophagic pada ginjal tikus yang diobati dengan TAC. Perubahan morfologis ini disertai dengan disregulasi gen terkait apoptosis atau autophagy pada ginjal tikus, yang menyebabkan kematian sel. Bukti kumulatif ini menunjukkan bahwa NIC(nikotin)itu sendiri tidak hanya menginduksi stres oksidatif dan kematian sel terprogram tetapi juga mempromosikan efek buruk TAC pada ginjal, mengakibatkan disfungsi ginjal dan kerusakan arsitektur, seperti yang dilaporkan sebelumnya dalam model nefropati diabetik yang diinduksi streptozotocin (STZ) [o] dan CKD ( s/6 nefrektomi) B3].
Selain itu, organel intraseluler yang berasal dari stres oksidatif seperti disfungsi mitokondria dan stres ER memainkan peran penting dalam integritas nefrotoksisitas TAC kronis, memicu stres ER, dan disregulasi mitokondria dan gen pengontrol stres ER dan efeknya diperburuk oleh pengobatan gabungan dengan keduanya. . Dengan demikian, penurunan kebugaran mitokondria dan tekanan ER dapat menjelaskan efek NIC(nikotin) pada cedera ginjal yang diinduksi TAC
Studi kami mengungkapkan bahwa NIC(nikotin)pada dosis 15mg/kg memperburuk cedera ginjal yang diinduksi TAC melalui stres oksidatif, peradangan, dan kematian sel terprogram, konsisten dengan penelitian sebelumnya [27,37,38]. Namun, yang lain telah mengamati temuan yang berlawanan. Sadis et al.Bg] menunjukkan bahwa NICat dosis os mg/kg melindungi ginjal dari cedera iskemia/reperfusi melalui jalur anti-inflamasi kolinergik. Studi lain oleh Agarwal et al.[23] melaporkan bahwa pengobatan oral jangka panjang dengan NIC(nikotin)(28 minggu) memberikan efek renoprotektif pada model tikus dengan proteinuria spontan Munich-Wistar-Frömter rats). Alasan perbedaan dalam peran NIC pada ginjal tidak diketahui tetapi mungkin tergantung pada dosis NIC, durasi pengobatan obat, atau model hewan pengerat. Studi lebih lanjut diperlukan untuk menyelesaikan masalah ini. Studi ini dengan jelas menunjukkan bahwa NIC memperburuk cedera ginjal yang diinduksi TAC pada model tikus dengan nefrotoksisitas TAC kronis. Kejengkelan stres oksidatif dan kematian sel terprogram mungkin merupakan salah satu mekanisme yang mendasari efek merusak dari NIC. Temuan kami memberikan wawasan yang lebih besar tentang dampak merokok di antara penerima transplantasi.

cistamche dalam fungsi ginjal
REFERENSI
1. Bentata Y. Tacrolimus: 2o tahun digunakan pada transplantasi ginjal dewasa: apa yang harus kita ketahui tentang nefrotoksisitasnya. Organ Artef 202044140-152.
2. Sikma MA, Hunault CC, van de Graaf EA, dkk. Konsentrasi darah tacrolimus yang tinggi lebih awal setelah transplantasi paru-paru dan risiko cedera ginjal. Eur J Clin Pharmacol 201773:573-58o.
3. Yagisawa T, Omoto K, Shimizu T, Ishida H, Tanabe K. Arteriosklerosis pada biopsi waktu nol merupakan faktor risiko untuk nefrotoksisitas kronis yang diinduksi tacrolimus. Nefrologi (Carlton)201s;2o Suppl2:s1-57.
4. Nankivell BJ, P'Ng CH, O'Connell PJ, Chapman JR. Nefrotoksisitas inhibitor kalsineurin melalui lensa histologi longitudinal: perbandingan era siklosporin dan tacrolimus. Transplantasi 2016;1oo:1723-171.
5. Lim SW, Shin Y, Luo K, dkk. Pengaruh Klotho pada pembersihan autophagy pada cedera ginjal yang diinduksi tacrolimus. FASEB J 2o193:2694-2706.
6. Lim SS, Vos T, Flaxman AD, dkk. Penilaian risiko komparatif beban penyakit dan cedera yang disebabkan oleh 67 faktor risiko dan kelompok faktor risiko di 21 wilayah,199o-201o: analisis sistematis untuk Studi Beban Penyakit Global 201o.Lancet 2o12;38o:2224-226o.
7. Formanek P, Salisbury-Afshar E, Afshar M.Membantu pasien dengan ESRD dan tahap awal CKD untuk berhenti merokok. Am J Kidney Dis 2018;72:255-266.
8. Jain G, Jaimes EA.Nikotinsinyal dan perkembangan penyakit ginjal kronis pada perokok. Biochem Pharmacol 2013;861215-1223.
9. Zhang LY, Jin J, Luo K, et al.Shen-Kang melindungi dari cedera ginjal akibat tacrolimus. Med JI Intern Korea 2019341078-1090.
10. Ibrahim ZS, Alkafafy ME, Ahmed MM, Soliman MM. Efek renoprotektif kurkumin terhadap stres oksidatif gabungan diabetes dannikotinpada tikus. Mol Med Rep 2016;13:3O17-3026.
