Baik Varian TP53 S47 Maupun P72 di Afrika-Sentris Tidak Berhubungan Dengan Penurunan Risiko Demam Malaria dalam Studi Kohort di Mali
Sep 26, 2023
Latar belakang. TP53 telah terbukti berperan dalam proses inflamasi, termasuk malaria. Kami sebelumnya menemukan bahwa p53 melemahkan peradangan yang disebabkan oleh parasit dan memprediksi perlindungan klinis terhadap infeksi Plasmodium falciparum pada anak-anak di Mali. Di sini, kami menyelidiki apakah polimorfisme p53 kodon 47 dan 72 dikaitkan dengan perbedaan risiko infeksi P. falciparum dan malaria tanpa komplikasi dalam studi kohort prospektif tentang kekebalan malaria.
Metode. polimorfisme p53 kodon 47 dan 72 ditentukan dengan mengurutkan TP53 ekson 4 pada 631 anak-anak dan orang dewasa Mali yang terdaftar dalam studi kohort Kalifabougou. Dampak dari polimorfisme ini terhadap risiko prospektif malaria demam, kejadian parasitemia, dan waktu terjadinya demam setelah kejadian parasitemia selama 6 bulan penularan malaria yang intens dinilai menggunakan model bahaya proporsional Cox.
Apa yang dilakukan ramuan cistanche—Anti-inflamasi
Hasil. Perancu risiko malaria, termasuk usia dan hemoglobin S atau C, serupa antara individu dengan atau tanpa polimorfisme p53 S47 dan R72. Sehubungan dengan varian umum masing-masing, baik S47 maupun R72 tidak dikaitkan dengan perbedaan risiko prospektif malaria demam, insiden parasitemia, atau malaria demam setelah parasitemia.
Kesimpulan. Temuan ini menunjukkan bahwa polimorfisme kodon p53 47 dan 72 tidak berhubungan dengan perlindungan terhadap insiden parasitemia P. falciparum atau malaria demam tanpa komplikasi.

manfaat suplemen cistanche—Anti-inflamasi
Kata kunci. malaria; P47S; polimorfisme p53; P72R; studi kohort prospektif.
Agen malaria yang paling signifikan secara klinis di Afrika, Plasmodium falciparum, telah menginfeksi manusia selama hampir 10,{1}} tahun [1]. Selama ini, tingginya angka kematian akibat malaria falciparum parah telah memberikan tekanan selektif yang kuat pada genom manusia [2]. Dengan demikian, polimorfisme eritrosit spesifik yang mungkin merugikan inangnya (misalnya, mutasi hemoglobin sabit [HbS] yang menyebabkan penyakit sel sabit) tetap dipertahankan pada populasi endemik malaria karena mutasi ini menyebabkan resistensi terhadap malaria dengan menjadikan eritrosit kurang ramah terhadap penyakit. parasit yang menyerang [3-5]. Studi asosiasi genom telah mengidentifikasi polimorfisme tambahan yang tidak terkait dengan fungsi eritrosit sebagai pelindung terhadap malaria berat, namun sebanyak 89% kerentanan terhadap malaria berat belum dikaitkan dengan lokus genom tertentu [6-9]. Selain itu, bukti mengenai polimorfisme inang eritrosit yang mungkin memberikan perlindungan terhadap malaria tanpa komplikasi (tidak parah) masih kurang. Penelitian sebelumnya telah mengimplikasikan penekan tumor p53 dalam pengendalian infeksi malaria. Peningkatan p53 inang telah terbukti mengurangi beban tahap hati Plasmodium pada tikus [10]. Kelompok kami sebelumnya menunjukkan peningkatan ekspresi gen target TP53 dan p53 dalam darah anak-anak Mali yang tidak terinfeksi yang kemudian mengalami parasitemia P. falciparum tanpa gejala dibandingkan dengan anak-anak yang kemudian menderita malaria demam [11]. Pengamatan ini menimbulkan pertanyaan apakah polimorfisme TP53 dapat menjelaskan perbedaan fenotip klinis ini. TP53 adalah gen yang paling sering bermutasi pada kanker manusia, dengan sebagian besar mutasi missense terjadi di hot spot baik dalam domain kaya prolin (asam amino 55-100) atau domain pengikatan DNA (asam amino 102-192) [12, 13]. Mutasi alami yang paling umum terjadi pada kodon 72 (rs1042522), yang timbul dari polimorfisme nukleotida tunggal (SNP) pada ekson 4 [14, 15]. Residu prolin pada posisi ini (P72), yang dianggap sebagai bentuk nenek moyang, lebih disukai ditemukan pada individu keturunan Afrika, sedangkan residu arginin (R72) lebih umum terjadi pada orang Amerika dan Eropa berkulit putih non-Hispanik, dengan frekuensi yang meningkat secara linier seiring dengan garis lintang [ 16, 17]. Meskipun substitusi prolin dengan arginin menghasilkan perubahan struktural dan fungsional yang signifikan [18], kedua residu tersebut diyakini berfungsi cukup untuk melindungi terhadap berbagai jenis kanker yang mungkin ditemui individu di garis lintang masing-masing (diulas dalam [13]). Khususnya, varian R72 dikaitkan dengan suhu dingin dan intensitas UV yang rendah [19], namun penelitian yang mengevaluasi hubungan polimorfisme kodon 72 dengan kanker kulit menghasilkan temuan yang tidak konsisten [20-23]. Meskipun frekuensi P72 meningkat di antara orang Afrika dibandingkan dengan orang Eropa [17], ada pendapat lain yang menyatakan bahwa varian R72 mungkin melindungi terhadap infeksi malaria pada manusia [24], berdasarkan bukti bahwa R72 telah meningkatkan potensi apoptosis dibandingkan P72 [ 25] dan apoptosis adalah mekanisme dimana inang menghilangkan hepatosit yang diparasit di hati [10]. SNP pengkodean p53 kedua yang paling sering juga terjadi pada ekson 4 dan terlokalisasi dalam wilayah pengkodean domain transaktivasi terminal-N pada kodon 47 (rs1800371) [26], di mana prolin yang lebih umum (P47) dapat digantikan oleh serin (S47 ) [27]. Berbeda dengan polimorfisme yang sangat umum pada kodon 72, varian S47 relatif jarang terjadi pada manusia, dengan frekuensi alel 2% –4% pada populasi Afrika [26, 27]. Karena S47 belum terdeteksi di Amerika yang bukan berasal dari Afrika [28], polimorfisme ini disebut sebagai varian Afrika-sentris dalam literatur. Varian S47 dapat memberikan resistensi terhadap kematian sel terprogram (ferroptosis) yang bergantung pada zat besi, yang menyebabkan peningkatan risiko kanker spontan [27, 29]. Pada tikus S47, cacat ferroptosis ini dapat menyebabkan akumulasi zat besi dan respons anti-inflamasi terhadap pigmen hemozoin malaria, sehingga menimbulkan spekulasi bahwa varian S47 dapat membatasi peradangan yang disebabkan oleh malaria dan dengan demikian meningkatkan kelangsungan hidup pada individu yang tinggal di daerah dengan penularan malaria yang intens. 30]. Studi tentang polimorfisme p53 dan kerentanan malaria pada manusia masih terbatas hingga saat ini. Dua penelitian telah meneliti hubungan antara varian kodon 72 dan risiko malaria pada manusia dengan hasil yang bertentangan [24, 31]. Namun, sepengetahuan kami, hubungan antara polimorfisme kodon 47 p53 dan risiko malaria belum diteliti pada manusia. Dalam penelitian ini, kami menguji apakah polimorfisme p53 kodon 47 dan 72 mempengaruhi risiko infeksi P. falciparum dan malaria klinis pada kohort prospektif anak-anak dan orang dewasa di Mali.
cistanche tubulosa—Anti inflamasi
Klik di sini untuk melihat produk Cistanche
【Minta lebih banyak】Email:cindy.xue@wecistanche.com / Aplikasi WhatsApp: 0086 18599088692 / Wechat: 18599088692
METODE
Desain Studi dan Peserta
Lokasi penelitian dan populasi penelitian telah dijelaskan di tempat lain [32]. Secara singkat, penelitian ini dilakukan di desa Kalifabougou, Mali, dimana penularan malaria P. falciparum sangat intens dan bersifat musiman, terjadi dari bulan Juni hingga Desember [32]. Pada bulan Mei 2011, kami mendaftarkan 695 anak-anak dan orang dewasa yang sehat, berusia 3 bulan hingga 25 tahun, ke dalam studi kohort observasional longitudinal untuk mengetahui kekebalan terhadap malaria, yang mana surveilans aktif malaria dua mingguan dilakukan dengan pemeriksaan rumah berkala setiap minggu dan surveilans pasif mandiri. -rujukan. Kriteria eksklusi pada saat pendaftaran termasuk kadar hemoglobin<7 g/dL, axillary temperature >37.5°C, acute systemic illness, underlying chronic disease, use of antimalarial or immunosuppressive medications in the past 30 days, and pregnancy. Malaria episodes were defined as parasitemia of >2500 parasit per mikroliter, suhu aksila lebih besar atau sama dengan 37,5 derajat dalam waktu 24 jam, dan tidak ada penyebab demam lain yang terlihat melalui pemeriksaan fisik. Episode dideteksi secara prospektif melalui rujukan ke klinik penelitian dan kunjungan pengawasan klinis aktif mingguan. Semua individu dengan tanda dan gejala malaria dan tingkat parasitemia apa pun yang terdeteksi melalui mikroskop diobati sesuai dengan pedoman Program Pengendalian Malaria Nasional Mali. Selama kunjungan klinik yang dijadwalkan, darah dikumpulkan dengan tusukan jari setiap 2 minggu untuk apusan darah dan bercak darah kering (DBS) pada kertas saring. Infeksi P. falciparum tanpa gejala terdeteksi melalui pemeriksaan mikroskopis apusan darah dan analisis bercak darah Polymerase Chain Reaction (PCR) pada akhir masa surveilans. Infeksi P. falciparum pertama dideteksi secara retrospektif dengan PCR dari DBS yang dikumpulkan secara longitudinal, seperti dijelaskan di tempat lain [32]. Episode malaria pertama ditentukan dari data kunjungan klinis. Nilai hemoglobin, diukur dengan alat analisa HemoCue, digunakan untuk menentukan status anemia, berdasarkan kriteria Organisasi Kesehatan Dunia. Pengetikan hemoglobin untuk HbS dilakukan dengan D-10 Sistem Pengujian Hemoglobin (Bio-Rad). Tiga kelas klinis dengan tingkat imunitas klinis berbeda telah dijelaskan di tempat lain [11].
Isolasi dan Urutan DNA
DNA genom diekstraksi dari sampel darah utuh menggunakan 3 metode: (1) dari pelet darah utuh (100 μL) menggunakan Kit Darah DNA QIAamp 96 (Qiagen), sesuai protokol pabrikan; (2) dari DBS yang menggunakan QIAamp DNA Mini Kit (Qiagen), sesuai protokol pabrikan; atau (3) dari DBS menggunakan metode ekstraksi throughput tinggi khusus, seperti yang dijelaskan di tempat lain [33]. DNA genom yang dimurnikan digunakan untuk memperkuat ekson 4 TP53 oleh PCR menggunakan primer berikut yang diterbitkan sebelumnya [34]: 5′-TGAGGACCTGGTCCTCTGAC- 3′ (maju) dan membalikkan 5′-AGAGGAATCCCAAAGTTC CA-3′ ( balik). Amplifikasi PCR dilakukan menggunakan HotStarTaq Plus Master Mix Kit (Qiagen) pada suhu anil 60 derajat, sesuai protokol yang direkomendasikan pabrikan. Produk PCR yang diperkuat dimurnikan dan diurutkan dengan metode terminasi rantai di Quintara Biosciences. File sekuens yang diterima dianalisis menggunakan perangkat lunak Benchling (rilis 2022.2.3; https://benchling.com) dan diselaraskan dengan sekuens referensi TP53 (pengidentifikasi gen 7157; Pusat Informasi Bioteknologi Nasional). Panggilan dasar yang dilaporkan oleh perangkat lunak diperiksa secara manual terhadap kromatogram. Urutan yang dihasilkan akan tersedia di GenBank (nos tambahan OP593553–OP594185).
Analisis statistik
Kurva Kaplan-Meier digunakan untuk memperkirakan probabilitas masing-masing untuk tetap bebas dari (1) malaria klinis, (2) parasitemia P. falciparum, atau (3) malaria demam yang pernah bersifat parasitemik. Untuk waktu demam malaria sekali parasitemia, waktu kejadian parasitemia yang diperkirakan merupakan titik tengah antara hasil PCR P. falciparum negatif terakhir dan hasil PCR P. falciparum positif pertama digunakan sebagai waktu mulainya. Model bahaya proporsional Cox digunakan untuk memperkirakan statistik Wald untuk menguji signifikansi perbedaan waktu terhadap kejadian pertama antara varian TP53 pada kodon 47 atau 72 baik dalam analisis univariat atau analisis yang menyertakan kovariat seperti yang ditunjukkan dalam tabel. Tes jumlah peringkat Kruskal-Wallis digunakan untuk membandingkan perbedaan antar kelompok untuk mendapatkan hasil yang berkelanjutan. Untuk variabel kategori, perbandingan kelompok dilakukan dengan menggunakan tes χ 2. Signifikansi statistik didefinisikan sebagai nilai P berekor 2-<.05. All analyses were performed using R software (version 4.2.0).

tanaman cistanche meningkatkan sistem kekebalan tubuh
Persetujuan Etis
Studi kohort Kalifabougou disetujui oleh Komite Etika Fakultas Kedokteran, Farmasi dan Kedokteran Gigi di Universitas Sains, Teknik dan Teknologi Bamako, dan Dewan Peninjau Institusional dari Institut Nasional Alergi dan Penyakit Menular, Institut Kesehatan Nasional. . Persetujuan tertulis diperoleh dari peserta dewasa dan orang tua atau wali anak-anak yang berpartisipasi. Penelitian ini disetujui sebagai penelitian subjek manusia yang dikecualikan oleh Indiana University Institutional Review Board (protokol 2005922267).
HASIL
Frekuensi Polimorfisme TP53 Diantara Peserta Penelitian
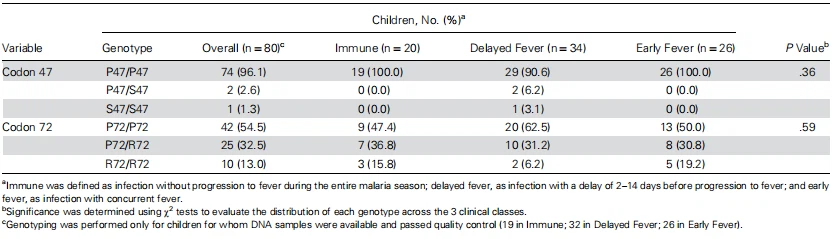
Dari 695 orang yang awalnya terdaftar dalam kelompok Kalifabougou, 631 memiliki DNA genom yang cukup untuk pengurutan TP53 ekson 4. Penyelarasan urutan mengungkapkan 40 individu (6,3%) dengan polimorfisme S47, dimana 33 di antaranya heterozigot dan 7 homozigot (Tabel 1). Polimorfisme R72 diamati pada 327 individu (51,8%), dimana 206 (32,6%) adalah heterozigot dan 121 (19,2%) adalah homozigot (Tabel 1). Baik polimorfisme kodon 47 maupun kodon 72 tidak berada dalam kesetimbangan Hardy-Weinberg (uji eksak Haldane, masing-masing P=6.5 × 10−6 dan P=1.0 × 10−12). Distribusi potensi pengubah risiko malaria (usia, jenis kelamin, HbS atau hemoglobin, parasitemia P. falciparum, dan anemia) tidak berbeda secara signifikan di antara kelompok varian TP53 baik untuk S47 maupun R72 (Tabel 1). Keenam individu yang heterozigot untuk alel S47 dan R72 adalah laki-laki dan PCR positif untuk P. falciparum pada saat pendaftaran (Tabel 1).
Tidak Ada Hubungan Polimorfisme TP53 Codon 47 dan Codon 72 Dengan Penurunan Risiko Episode atau Insiden Malaria Klinis P. falciparumParasitemia
Analisis waktu-ke-peristiwa dilakukan untuk menguji hubungan antara varian S47 dan P72 dan risiko demam malaria. Analisis awal antara P47/P47, P47/S47, dan S47/S47 menunjukkan tidak ada perbedaan signifikan dalam risiko malaria (data tidak ditampilkan), mungkin karena kecilnya ukuran sampel untuk genotipe P47/S47 heterozigot dan S47/S47 homozigot. Dengan demikian, genotipe-genotipe ini dipecah menjadi satu strata. Untuk kodon 72, genotipe heterozigot dan homozigot dipertahankan sebagai 3 strata terpisah. Tidak ada perbedaan yang signifikan dalam waktu timbulnya episode malaria klinis pertama antara genotipe P47/P47 (median [interval kepercayaan 95%], 184 [165–210] hari) dan varian S47 (151 [133–210] hari) atau antara Genotipe P72/P72 (183 [59–210] hari) dan P72/R72 (210 [160–210] hari) atau R72/R72 (159 [142–210] hari) baik dalam analisis univariat (Gambar 1A dan 1B ) atau analisis yang disesuaikan yang mencakup usia, jenis kelamin, parasitemia awal, anemia, dan keberadaan HbS sebagai kovariat (Tabel Tambahan 1). Individu dengan P47/S47 dan P72/R72 menunjukkan risiko malaria klinis yang sama dengan individu homozigot P47/P47 dan P72/P72 (Gambar Tambahan 1). Peningkatan p53 telah terbukti mengurangi beban tahap hati Plasmodium pada model tikus [10]. Oleh karena itu kami menentukan apakah polimorfisme TP53 dikaitkan dengan perbedaan risiko kejadian infeksi P. falciparum sebagaimana ditentukan oleh pengawasan PCR aktif dan intensif pada individu yang memulai penelitian dengan hasil negatif P. falciparum dengan PCR (n=330). Kami tidak mendeteksi perbedaan yang signifikan dalam waktu pertama kali infeksi P. falciparum terdeteksi PCR antara P47/P47 (median [interval kepercayaan 95%], 85 [81–91] hari) dan varian S47 (85 [58–124]) hari) atau antara genotipe P72/P72 (88 [80–95] hari) dan P72/R72 (81 [72–91] hari) atau R72/R72 (91 [80–116] hari) dalam analisis univariat ( Gambar 1C dan 1D) atau analisis yang disesuaikan yang mencakup kovariat yang relevan (Tabel Tambahan 2).
Tidak Ada Hubungan Polimorfisme TP53 Dengan Perlindungan Dari Demam Malaria Pasca Kejadian Parasitemia P. falciparum atau Perbedaan Ekspresi Gen
Kelompok kami sebelumnya mengidentifikasi sebagian anak-anak dalam kelompok Kalifabougou yang tidak demam pada saat kejadian, parasitemia P. falciparum yang dikonfirmasi dengan PCR [11]. Anak-anak ini diklasifikasikan sebagai "demam tertunda" atau "kebal" tergantung pada apakah mereka mengalami demam setelah 2-14 hari atau tidak menunjukkan gejala selama sisa musim malaria. Kedua subset ini menunjukkan peningkatan ekspresi gen target TP53 dan TP53 pada awal prainfeksi dibandingkan dengan anak-anak yang demam pada saat kejadian parasitemia P. falciparum (“demam dini”) [11]. Untuk menentukan apakah polimorfisme TP53 dikaitkan dengan demam tertunda atau fenotip imun, kami memeriksa distribusi polimorfisme S47 dan R72 dalam himpunan bagian ini tetapi tidak mengamati adanya perbedaan yang signifikan antara 3 fenotip klinis (Tabel 2). Pemeriksaan ulang ekspresi TP53 dalam transkriptom RNA-seq yang diperoleh pada garis dasar sehat setiap anak (n=80) [11] dengan polimorfisme kodon 47 dan 72 menunjukkan tidak ada perbedaan antara polimorfisme umum dan variannya masing-masing (Gambar 2). Untuk menentukan apakah varian S47 atau P72 dikaitkan dengan perlindungan dari demam malaria setelah parasitemia pada kelompok induk, kami menentukan risiko malaria demam, dengan menggunakan waktu parasitemia pertama sebagai waktu mulainya. Di sini, kami menyertakan semua individu yang memulai penelitian dengan hasil PCR negatif P. falciparum dan kemudian memiliki parasitemia P. falciparum yang dikonfirmasi dengan PCR (n=292). Tidak ada perbedaan yang signifikan dalam waktu terjadinya demam pertama setelah parasitemia diamati pada subkelompok dengan polimorfisme S47 atau P72 relatif terhadap genotipe umum masing-masing dengan analisis univariat (Gambar 3A dan 3B). Meskipun ada kecenderungan peningkatan risiko malaria demam yang bersifat parasitemia untuk S47 dibandingkan dengan P47/P47 (Gambar 3A), perbedaan ini menjadi lebih tidak signifikan secara statistik ketika disesuaikan dengan kovariat yang relevan seperti usia dan HbS (Tambahan Tabel 3).
DISKUSI
Berbeda dengan malaria berat, polimorfisme genetik inang yang berhubungan dengan resistensi terhadap malaria tanpa komplikasi terutama melibatkan varian gen eritrosit [2, 5]. Meskipun beberapa gen non eritrosit telah dikaitkan dengan perlindungan terhadap malaria berat [6, 7, 9], hanya segelintir gen yang terlibat dalam respons inflamasi, yaitu NOS2, dan TNF, yang secara spesifik dikaitkan dengan risiko diferensial malaria tanpa komplikasi atau ringan. [2, 35–38]. Faktor transkripsi p53 mempertahankan homeostasis seluler sebagai respons terhadap sinyal stres dengan mengatur berbagai target hilir, termasuk jalur inflamasi, yang bersama-sama menekan proses onkogenik (39). Potensi onkogenik dari peradangan kronis telah diketahui [40], dan terdapat semakin banyak bukti bahwa p53 dapat memodulasi peradangan inang dalam konteks patogen [41, 42]. Untuk mendukung hal ini, kelompok kami sebelumnya mengamati bahwa peningkatan ekspresi TP53 dan target hilirnya dikaitkan dengan perlindungan dari demam selama insiden parasitemia P. falciparum, menunjukkan bahwa p53 pada awalnya dapat mengurangi respons demam selama infeksi malaria [11]. Dalam penelitian sebelumnya, tikus dengan varian p53 S47 menunjukkan respons anti-inflamasi terhadap hemozoin pigmen malaria, menunjukkan bahwa polimorfisme p53 spesifik dapat membatasi peradangan selama infeksi malaria pada manusia [30]. Dalam konteks tantangan inflamasi dengan lipopolisakarida, tikus dengan polimorfisme p53 R72 menunjukkan peningkatan kelangsungan hidup dibandingkan dengan tikus P72, menyiratkan bahwa varian R72 dapat melindungi terhadap respon patologis terhadap bakteri gram negatif [43]. Di sini, kami mengevaluasi apakah polimorfisme kodon 47 atau 72 mempengaruhi risiko malaria P. falciparum dalam kohort longitudinal prospektif dan menunjukkan bahwa tidak satu pun dari polimorfisme ini dikaitkan dengan perbedaan risiko insiden parasitemia atau insiden malaria demam. Selain itu, tidak satu pun dari polimorfisme TP53 ini yang terwakili secara berlebihan di antara anak-anak yang terlindungi dari demam malaria dan yang menunjukkan peningkatan ekspresi TP53 dan targetnya pada awal prainfeksi pada penelitian kelompok kami sebelumnya [11]. Temuan kami konsisten dengan studi cross-sectional pada wanita primipara Ghana (n=314) dan anak-anak Rwanda (n=545), yang tidak menunjukkan hubungan antara polimorfisme R72 dan prevalensi infeksi P. falciparum atau intensitas parasit [31]. Satu-satunya investigasi lain yang dipublikasikan mengenai polimorfisme p53 pada malaria adalah penelitian terhadap bayi baru lahir di Sardinia, yang menemukan frekuensi yang lebih besar dari genotipe homozigot R72 yang dianggap sebagai pelindung malaria di daerah dengan endemisitas malaria yang sebelumnya lebih tinggi (n=46) dibandingkan dengan daerah dengan endemisitas malaria yang sebelumnya lebih rendah (n=47) [24]. Berdasarkan premis bahwa varian R72 dari p53 telah meningkatkan potensi apoptosis [25] dan dengan demikian dapat mencegah infeksi tahap hati melalui apoptosis hepatosit yang diparasit [10], penulis menyarankan bahwa endemisitas malaria mungkin telah dipilih secara positif untuk polimorfisme R72 [24 ]. Namun, hipotesis ini tidak didukung oleh data kami yang menunjukkan tidak ada perbedaan waktu timbulnya parasitemia yang dikonfirmasi PCR di antara genotipe kodon 72. Selain itu, polimorfisme R72 yang melindungi terhadap malaria tidak dapat menjelaskan mengapa alel P72 lebih umum di Afrika dibandingkan di Eropa [17], sebuah pengamatan yang menyiratkan P72 sebagai alel yang dipilih untuk dipertahankan pada populasi endemik malaria menurut " hipotesis malaria" [8]. Mungkin aktivitas fungsional yang diberikan oleh R72 tidak relevan dengan risiko demam malaria. Seperti disebutkan di atas, meskipun varian R72 dapat melindungi tikus terhadap tantangan lipopolisakarida [43], varian ini juga terbukti mendorong peradangan dalam konteks diet tinggi lemak [44] atau kanker payudara [45] dalam penelitian pada tikus. Jadi, bagaimana polimorfisme R72 mempengaruhi respon inflamasi mungkin bergantung pada jenis dan ketajaman gangguan.
Tabel 1. Potensi Perancu Risiko Malaria dan Genotipe TP53
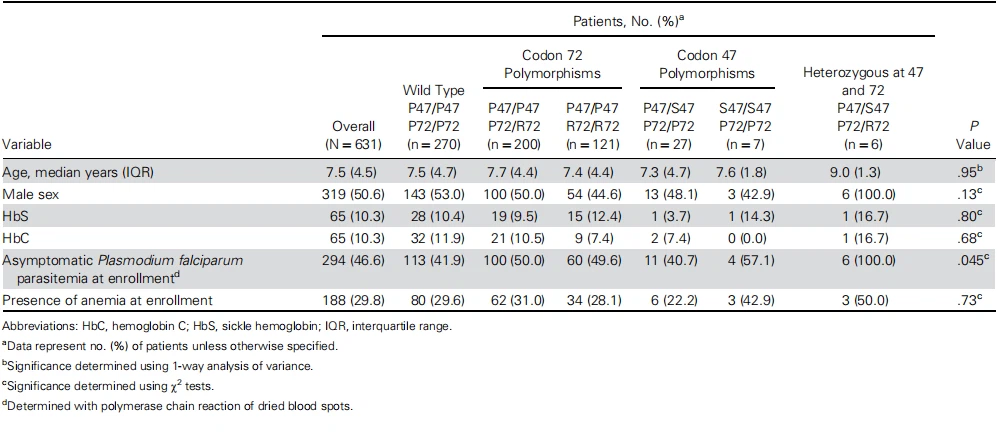
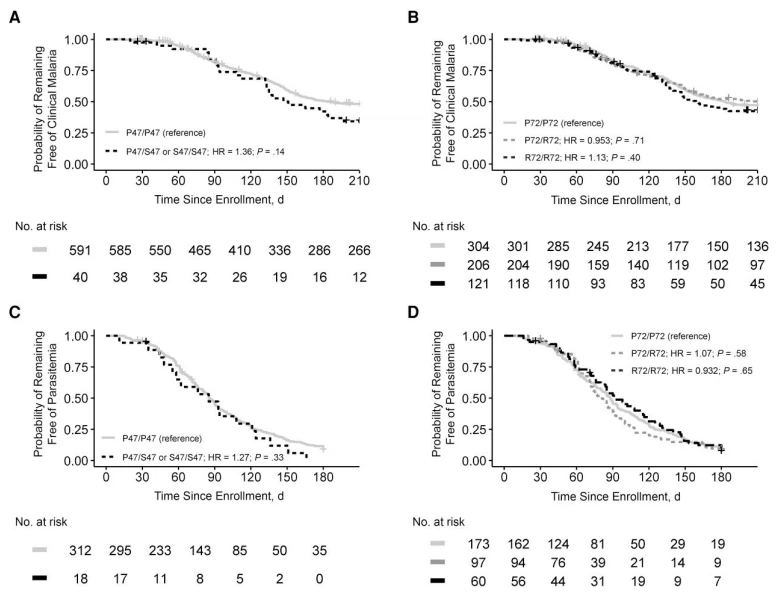
Figure 1. p53 Codon 47 and 72 polymorphisms and malaria risk in the Kalifabougou cohort during the 2011 malaria season. Kaplan-Meier curves of time to first febrile malaria episode (defined as >2500 parasites per microliter by blood smear and axillary temperature >37,5 derajat ) (A, B) dan waktu reaksi berantai polimerase (PCR) pertama – dikonfirmasi parasitemia Plasmodium falciparum (C, D), dikelompokkan berdasarkan genotipe varian p53 yang ditunjukkan. Untuk C dan D, analisis hanya mencakup individu yang memulai musim malaria dengan hasil PCR negatif untuk P. falciparum. Signifikansi ditentukan oleh bahaya proporsional Cox, menggunakan statistik uji Wald. Tabel menunjukkan jumlah individu yang berisiko pada hari-hari tertentu sejak pendaftaran. Singkatan: HR, rasio bahaya.
Tabel 2. Distribusi Genotipe TP53 pada Anak dengan Kerentanan Berbeda Demam Malaria Setelah Parasitemia Plasmodium falciparum Awal
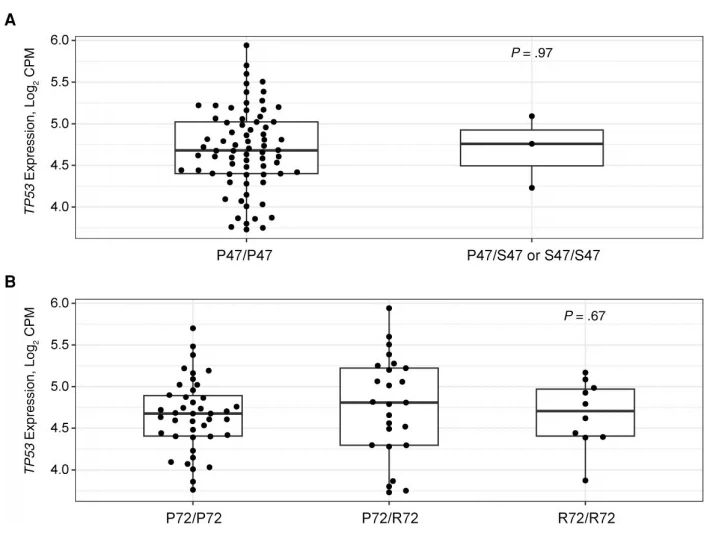
Gambar 2. Ekspresi TP53 berdasarkan polimorfisme kodon 47 dan 72. Ekspresi TP53 dengan menunjukkan polimorfisme kodon p53 47 (A) dan 72 (B) dalam sampel darah lengkap dari 80 anak-anak Mali pada awal sehat dan tidak terinfeksi pada Mei 2011, sebelum musim malaria [11]. Signifikansi ditentukan dengan menggunakan uji Wilcoxon (A) atau analisis varians (B). Ekspresi gen dilaporkan sebagai jumlah log2 per juta (CPM).
Kurangnya hubungan antara varian kodon 47 atau kodon 72 dan perlindungan dari malaria juga dapat dijelaskan oleh kurangnya efek terhadap ekspresi p53 seperti yang terlihat dalam data kami (Gambar 2) dan penelitian sebelumnya [27, 46]. Salah satu temuan utama dari penelitian kelompok kami sebelumnya adalah bahwa ekspresi p53 dan target hilirnya meningkat pada anak-anak yang terlindungi dari demam dini selama insiden parasitemia [11], menunjukkan bahwa induksi ekspresi p53 mungkin diperlukan untuk mengendalikan peradangan. Meskipun varian S47 menurunkan kemampuan untuk menginduksi apoptosis dibandingkan dengan P47, ekspresi protein p53 di dalam sel masih dipertahankan pada tingkat yang sama (27). Hal ini, dikombinasikan dengan pengamatan bahwa tidak ada anak-anak dalam kelompok “kekebalan” yang paling terlindungi yang memiliki varian S47, menunjukkan bahwa pengurangan apoptosis melalui polimorfisme ini tidak mungkin menjadi mekanisme p53 mempengaruhi demam malaria. Demikian pula, polimorfisme R72 secara fungsional signifikan tetapi tidak selalu menghasilkan peningkatan ekspresi p53 [25, 46]. Kekuatan selektif dapat meningkatkan frekuensi alel yang disukai seiring waktu. Alel S47 terdapat pada 6,3% peserta yang dievaluasi, dengan 1,1% bersifat homozigot, memberikan frekuensi alel sebesar 3,7%, yang konsisten dengan 2% –4% yang dilaporkan sebelumnya untuk orang Afrika dari Afrika sub-Sahara [28]. Sebaliknya, alel R72 terdapat pada 51,8% peserta (19,2% homozigot), sehingga memberikan frekuensi alel sebesar 35,5% pada populasi ini. Dominasi alel P72 pada kohort Mali konsisten dengan peningkatan frekuensi alel ini pada garis lintang yang lebih dekat ke khatulistiwa, sebuah temuan yang dikaitkan dengan seleksi alam [17].

manfaat cistanche untuk pria-memperkuat sistem kekebalan tubuh
Sangat menggoda untuk berspekulasi mengapa alel S47 dipertahankan pada tingkat yang rendah di antara orang Afrika. Mengingat bahwa S47 mengalami penurunan potensi apoptosis dibandingkan dengan P47 (27), rendahnya frekuensi alel S47 dapat dijelaskan oleh biaya kesesuaian yang dikeluarkan untuk pemeliharaannya karena kerugian selektif yang tidak terkait dengan peradangan patologis selama malaria, seperti peningkatan risiko kanker payudara pramenopause. [47]. Namun, varian S47, dengan membatasi respon inflamasi yang diinduksi hemozoin [30], masih dapat memberikan perlindungan terhadap malaria yang lebih parah. Karena penelitian ini hanya mengevaluasi malaria P. falciparum tanpa komplikasi, penelitian ini tidak membahas apakah salah satu dari polimorfisme ini dikaitkan dengan penurunan risiko malaria berat. Hubungan yang cukup signifikan antara heterozigositas ganda (P47/S47 dan P72/R72) dan parasitemia P. falciparum tanpa gejala pada pendaftaran bulan Mei perlu diperhatikan (Tabel 1). Di daerah dengan malaria musiman yang intens, infeksi P. falciparum kronis tanpa gejala pada akhir musim kemarau mencerminkan kekebalan malaria kumulatif yang lebih tinggi [48]. Karena 6 individu heterozigot ganda ini memiliki median usia yang lebih tinggi dibandingkan dengan kelompok lain, representasi parasitemia asimtomatik yang berlebihan dalam genotipe ini mungkin hanya merupakan fungsi kebetulan dari paparan malaria di masa lalu dan bukan konsekuensi dari polimorfisme p53. Studi kohort tambahan tentang polimorfisme kodon 47 dan 72 p53 dan risiko malaria akan diperlukan untuk mengkonfirmasi pentingnya genotipe heterozigot ganda. Keterbatasan lain dari penelitian ini harus diperhatikan. Meskipun penelitian kami adalah salah satu penelitian yang lebih besar mengenai polimorfisme p53 dan risiko malaria hingga saat ini, hanya 7 dari 631 peserta yang homozigot untuk S47, sehingga membatasi kekuatan kami untuk mendeteksi hubungan tersebut. Selain itu, kami hanya mengevaluasi polimorfisme p53 dalam ekson 4 dan dengan demikian mungkin melewatkan dampak mutasi lain yang berpotensi relevan, termasuk mutasi 3KR (K117R + K161R + K162R) yang melibatkan situs asetilasi p53 (49). Sebagai catatan, kami mengevaluasi kodon 117, yang terletak di ekson 4 dan hanya menemukan lisin. Kami juga tidak mengevaluasi polimorfisme di daerah nonkode TP53 atau regulator p53 yang dapat mempengaruhi p53 pada tingkat protein, seperti MDM2 (28, 50). Pendekatan pengurutan generasi berikutnya yang secara komprehensif menilai polimorfisme di wilayah 5′ dan 3′ yang tidak diterjemahkan serta semua wilayah pengkodean untuk regulator TP53 dan p53 dapat mengatasi keterbatasan ini. Terakhir, kami tidak menentukan apakah genotipe p53 berbeda dalam ekspresi p53 pada tingkat sel, yang mungkin memberikan wawasan penting mengenai apakah polimorfisme kodon 47 dan 72 dapat memengaruhi jalur yang diatur p53-. Singkatnya, penelitian ini memberikan bukti bahwa baik varian p53 kodon 47 maupun kodon 72 tidak memberikan perlindungan terhadap malaria sebagaimana diukur berdasarkan waktu terjadinya parasitemia P. falciparum dan malaria demam tanpa komplikasi. Mengingat frekuensi alel S47 yang lebih rendah pada populasi ini, diperlukan penelitian yang lebih besar untuk memastikan kurangnya hubungan varian S47 dengan risiko malaria.
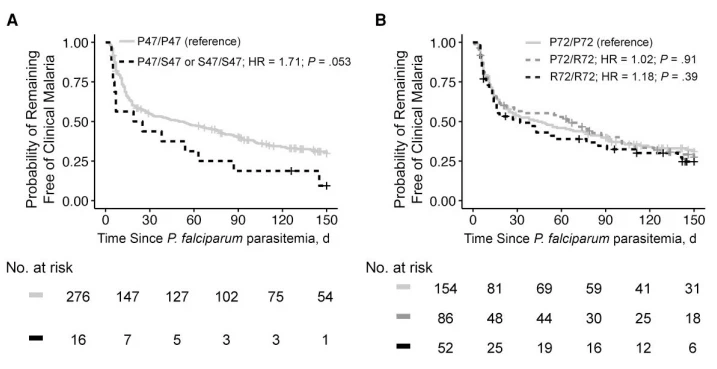
Gambar 3. Polimorfisme kodon 47 dan 72 p53 dan risiko terjadinya demam malaria setelah kejadian parasitemia. Kaplan-Meier memplot waktu untuk malaria demam pertama menggunakan infeksi tahap darah Plasmodium falciparum yang dikonfirmasi dengan reaksi berantai polimerase pertama sebagai waktu mulai yang dikelompokkan berdasarkan polimorfisme varian kodon 47 (A) atau kodon 72 (B) p53. Signifikansi ditentukan oleh bahaya proporsional Cox menggunakan statistik uji Wald. Tabel menunjukkan jumlah individu yang berisiko pada waktu yang ditentukan sejak pendaftaran. Singkatan: HR, rasio bahaya.
Data pelengkap
Materi pelengkap tersedia di The Journal of Infectious Diseases online. Terdiri dari data yang disediakan oleh penulis untuk memberi manfaat bagi pembaca, materi yang diposting tidak disalin dan merupakan tanggung jawab penulis sepenuhnya, jadi pertanyaan atau komentar harus ditujukan kepada penulis terkait.
Catatan
Ucapan Terima Kasih. Kami mengucapkan terima kasih kepada peserta penelitian dan staf pendukung penelitian di Kalifabougou dan Bamako, Mali. Kami juga berterima kasih kepada Shanping Li, Emily LaVerriere, dan Daniel E. Neafsey yang telah memberikan materi genom dan panduan teknis.
Kontribusi penulis. PDC dan TMT menyusun proyek ini. SD, KK, AO, BT, PDC, dan TMT merancang studi kohort awal, dan SD, KK, AO, dan BT menerapkannya. ELG melakukan eksperimen. JB, AU, ELG, dan TMT melakukan analisis data. PDC menyumbangkan sumber daya tambahan. JB, PDC, dan TMT menulis naskahnya. Seluruh penulis telah membaca dan menyetujui manuskrip itu.
Penafian. Konten tersebut sepenuhnya merupakan tanggung jawab penulis dan tidak mewakili pandangan resmi National Institutes of Health.
Dukungan finansial. Pekerjaan ini didukung oleh Institut Nasional Alergi dan Penyakit Menular (NIAID), dan Institut Kesehatan Nasional (hibah R01AI158719 dan K08AI125682 kepada TMT). Studi kohort Kalifabougou didukung oleh Divisi Penelitian Intramural NIAID.
Potensi konflik kepentingan. Semua penulis: Tidak ada konflik yang dilaporkan. Semua penulis telah menyerahkan Formulir ICMJE untuk Pengungkapan Potensi Konflik Kepentingan. Konflik yang dianggap relevan oleh editor dengan isi naskah telah diungkapkan.
Referensi
1. Sundararaman SA, Plenderleith LJ, Liu W, dkk. Genom spesies Plasmodium simpanse samar mengungkap peristiwa evolusi penting yang menyebabkan malaria pada manusia. Nat Commun 2016; 7:11078.
2. Kwiatkowski DP. Bagaimana malaria telah mempengaruhi genom manusia dan apa yang dapat diajarkan genetika manusia kepada kita tentang malaria. Am J Hum Genet 2005; 77:171–92.
3. Allison AC. Perlindungan diberikan oleh sifat sel sabit terhadap infeksi malaria subtertian. Br Med J 1954; 1:290–4.
4. Lell B, Mei J, Schmidt-Ott RJ, dkk. Peran polimorfisme sel darah merah dalam resistensi dan kerentanan terhadap malaria. Clin Menginfeksi Dis 1999; 28:794–9.
5. Lopera-Mesa TM, Doumbia S, Konate D, dkk. Pengaruh varian sel darah merah pada malaria pada masa kanak-kanak di Mali: studi kohort prospektif. Lancet Hematol 2015; 2: e140–9.
6. Ravenhall M, Campino S, Sepulveda N, dkk. Polimorfisme genetik baru yang terkait dengan malaria parah dan di bawah tekanan selektif di Tanzania timur laut. Genet PLoS 2018; 14:e1007172.
7. Ndila CM, Uyoga S, Macharia AW, dkk. Polimorfisme gen kandidat manusia dan risiko malaria parah pada anak-anak di Kilifi, Kenya: studi asosiasi kasus-kontrol. Lancet Hematol 2018; 5:e333–45.
8. Ebel ER, Uricchio LH, Petrov DA, Egan ES. Meninjau kembali hipotesis malaria: memperhitungkan poligenisitas dan pleiotropi. Tren Parasitol 2022; 38:290–301.
9. Jaringan Epidemiologi Genomik Malaria. Wawasan mengenai kerentanan malaria menggunakan data genom pada 17.{3}} individu dari Afrika, Asia, dan Oseania. Nat Commun 2019; 10:5732.
10. Kaushansky A, Kamu AS, Austin LS, dkk. Penekanan host p53 sangat penting untuk infeksi stadium hati Plasmodium. Perwakilan Sel 2013; 3:630–7.
11. Tran TM, Guha R, Portugal S, dkk. Tanda tangan molekuler dalam darah mengungkapkan peran p53 dalam mengatur peradangan akibat malaria. Imunitas 2019; 51:750–65.e10.
12. Baugh EH, Ke H, Levine AJ, Bonneau RA, Chan CS. Mengapa terdapat mutasi hotspot pada gen TP53 pada kanker manusia? Perbedaan Kematian Sel 2018; 25:154–60.
13. Hoyos D, Greenbaum B, Levine AJ. Genotipe dan fenotipe mutasi missense pada domain prolin protein p53. Perbedaan Kematian Sel 2022; 29:938–45.
14. Harris N, Brill E, Shohat O, dkk. Dasar molekuler untuk heterogenitas protein p53 manusia. Biol Sel Mol 1986; 6:4650–6.
15. Matlashewski GJ, Tuck S, Pim D, Lamb P, Schneider J, Crawford LV. Polimorfisme struktur primer pada residu asam amino 72 p53 manusia. Biol Sel Mol 1987; 7: 961–3.
16. Katkoori VR, Jia X, Shanmugam C, dkk. Signifikansi prognostik polimorfisme kodon 72 p53 berbeda dengan ras pada adenokarsinoma kolorektal. Klinik Kanker Res 2009; 15: 2406–16.
17. Beckman G, Birgander R, Sjalander A, dkk. Apakah polimorfisme p53 dipertahankan oleh seleksi alam? Bersenandung Di Sini 1994; 44:266–70.
18. Thomas M, Kalita A, Labrecque S, Pim D, Banks L, Matlashewski G. Dua varian polimorfik p53 tipe liar berbeda secara biokimia dan biologis. Biol Sel Mol 1999; 19:1092–100. 19. Shi H, Tan SJ, Zhong H, dkk. Suhu musim dingin dan sinar UV terkait erat dengan perubahan genetik pada jalur penekan tumor p53 di Asia Timur. Apakah J Hum Genet 2009; 84:534–41.
20. McGregor JM, Harwood CA, Brooks L, dkk. Hubungan antara polimorfisme kodon 72 p53 dan kerentanan terhadap sengatan matahari dan kanker kulit. J Investasikan Dermatol 2002; 119: 84–90.
21. Nan H, Qureshi AA, Hunter DJ, Han J. Interaksi antara polimorfisme p53 kodon 72 dan varian reseptor melanocortin 1 terhadap respon berjemur dan risiko melanoma kulit. Br J Dermatol 2008; 159:314–21.
22. Cotignola J, Chou JF, Roy P, dkk. Investigasi efek polimorfisme MDM2 SNP309 dan TP53 Arg72Pro pada usia timbulnya melanoma kulit. J Investasikan Dermatol 2012; 132:1471–8.
23. Liu T, Lei Z, Pan Z, dkk. Hubungan genetik antara polimorfisme kodon p53 72 dan risiko karsinoma sel skuamosa kulit. Biologi Tumor 2014; 35:3899–903.
24. Gloria-Bottini FMG, Saccucci P, Bottini E. P53 kodon 72 dan morbiditas malaria masa lalu di Sardinia. Eliminasi Malar Chemoth Cont 2013; 2(1):107.
25. Dumont P, Leu JI, Della Pietra AC 3rd, George DL, Murphy M. Varian polimorfik kodon 72 p53 memiliki potensi apoptosis yang sangat berbeda. Nat Genet 2003; 33:357–65. 26. Felley-Bosco E, Weston A, Cawley HM, Bennett WP, Harris CC. Studi fungsional tentang polimorfisme garis kuman pada kodon 47 dalam gen p53. Am J Hum Genet 1993; 53:752–9.
27. Li X, Dumont P, Della Pietra A, Shetler C, Murphy ME. Polimorfisme kodon 47 pada p53 signifikan secara fungsional. J Biol Kimia 2005; 280:24245–51.
28. Barnoud T, Parris JLD, Murphy ME. Varian genetik umum pada jalur TP53 dan dampaknya terhadap kanker. Biol Sel J Mol 2019; 11:578–85.
29. Jennis M, Kung CP, Basu S, dkk. Polimorfisme spesifik Afrika pada gen TP53 merusak fungsi penekan tumor p53 pada model tikus. Pengembangan Gen 2016; 30: 918–30.
30. Singh KS, Leu JI, Barnoud T, dkk. Varian TP53 yang berpusat di Afrika meningkatkan akumulasi zat besi dan patogenesis bakteri tetapi meningkatkan respons terhadap toksin malaria. Nat Commun 2020; 11:473.
31. Gai PP, Meese S, Bedu-Addo G, Gahutu JB, Mockenhaupt FP. Tidak ada hubungan polimorfisme kodon 72 p53 dengan malaria pada anak primipara Ghana dan anak-anak Rwanda. Am J Trop Med Hyg 2014; 90:1133–4.
32. Tran TM, Li S, Doumbo S, dkk. Sebuah studi kohort longitudinal yang intensif terhadap anak-anak dan orang dewasa di Mali tidak menunjukkan bukti adanya kekebalan terhadap infeksi Plasmodium falciparum. Clin Menginfeksi Dis 2013; 57:40–7.
33. LaVerriere E, Schwabl P, Carrasquilla M, dkk. Desain dan implementasi panel pengurutan amplikon multipleks untuk melayani epidemiologi genom penyakit menular: studi kasus malaria. Sumber Daya Mol Ecol 2022; 22: 2285–303.
34. Kawaguchi H, Ohno S, Araki K, dkk. p53 Polimorfisme pada kanker esofagus terkait human papillomavirus. Kanker Res 2000; 60:2753–5.
35. Kun JF, Mordmuller B, Perkins DJ, dkk. Sintase oksida nitrat 2Lambaréné (G-954C), meningkatkan produksi oksida nitrat, dan perlindungan terhadap malaria. J Menginfeksi Dis 2001; 184:330–6.
36. Flori L, Delahaye NF, Irak FA, Hernandez-Valladares M, Fumoux F, Rihet P. TNF sebagai gen kandidat malaria: skrining polimorfisme dan analisis asosiasi berbasis keluarga terhadap serangan malaria ringan dan parasitemia di Burkina Faso. Gen Imun 2005; 6:472–80.
37. Fugtagbi G, Otu PS, Abdul-Rahman M, dkk. Asosiasi TNF-alpha, MBL2, NOS2, dan G6PD dengan hasil malaria pada masyarakat di Ghana Selatan. Genet Res (Camb) 2022; 2022:6686406.
38. Meyer CG, Mei J, Luty AJ, Lell B, Kremsner PG. TNFalpha-308A dikaitkan dengan interval infeksi ulang Plasmodium falciparum yang lebih pendek. Antigen Jaringan 2002; 59:287–92.
39. Cooks T, Harris CC, Oren M. Terperangkap dalam baku tembak: p53 dalam peradangan. Karsinogenesis 2014; 35:1680–90.
40. Coussens LM, Werb Z. Peradangan dan kanker. Alam 2002; 420:860–7.
41. Madenspacher JH, Azzam KM, Gowdy KM, dkk. p53 Mengintegrasikan pertahanan inang dan nasib sel selama pneumonia bakterial. J Exp Med 2013; 210:891–904.
42. Menendez D, Shatz M, Azzam K, Garantziotis S, Fessler MB, Resnick MA. Keluarga gen reseptor mirip Tol diintegrasikan ke dalam kerusakan DNA manusia dan jaringan p53. Genet PLoS 2011; 7:e1001360.
43. Frank AK, Leu JI, Zhou Y, dkk. Polimorfisme kodon 72 p53 mengatur interaksi dengan NF-κB dan transaktivasi gen yang terlibat dalam imunitas dan peradangan. Biol Sel Mol 2011; 31:1201–13.
44. Kung CP, Leu JI, Basu S, dkk. Polimorfisme P72R dari p53 merupakan predisposisi obesitas dan disfungsi metabolisme. Perwakilan Sel 2016; 14:2413–25.
45. Gunaratna RT, Santos A, Luo L, dkk. Peran dinamis polimorfisme nukleotida tunggal kodon 72 p53 dalam tumorigenesis payudara dalam model tikus yang dimanusiakan. Onkogen 2019; 38:3535–50.
46. Kim BY, Lee SY, Chung SK. Regulasi transkripsi diferensial kodon p53 polimorfik 72 dalam jalur metabolisme. Int J Mol Sci 2021; 22:10793.
47. Murphy ME, Liu S, Yao S, dkk. SNP yang signifikan secara fungsional pada TP53 dan risiko kanker payudara pada wanita Afrika-Amerika. NPJ Kanker Payudara 2017; 3:5.
48. Portugal S, Tran TM, Ongoiba A, dkk. Pengobatan infeksi Plasmodium falciparum kronis tanpa gejala tidak meningkatkan risiko malaria klinis setelah infeksi ulang. Clin Menginfeksi Dis 2017; 64:645–53.
49. Li T, Kon N, Jiang L, dkk. Penekanan tumor tanpa adanya penghentian siklus sel yang dimediasi p53-, apoptosis, dan penuaan. Sel 2012; 149:1269–83.
50. Grochola LF, Zeron-Medina J, Meriaux S, Bond GL. Polimorfisme nukleotida tunggal pada jalur pensinyalan p53. Biol Perspektif Cold Spring Harb 2010; 2:a001032.