Populasi Sel T CD8 Dan CD4 di Ginjal Manusia
Mar 25, 2022
Abstrak:Latar Belakang: Di situs perbatasan, dan di organ internal, sel T memori residen jaringan (TRM) berkontribusi pada penghalang kekebalan terhadap patogen seperti virus, bakteri, jamur, dan kanker. Namun, informasi tentang keberadaan dan fungsi sel-sel ini di ginjal manusia masih sedikit. Untuk lebih memahami pertahanan imunologi yang dimediasi sel T di organ ini, kami bertujuan untuk menentukan aspek fenotipik dan fungsional sel T CD8 dan CD4 yang ada dalam kondisi sehat dan allograft.ginjal tisu. Metode: Menggunakan multichannel fellow cytometry, kami menilai fenotipe dan fungsi sel T dalam sampel jaringan ginjal yang sehat (n=5) danginjaljaringan allograft (n=7) dan membandingkan aspek-aspek ini dengan sel T dalam darah tepi dari kontrol yang sehat (n=13). Hasil:Ginjalsampel jaringan mengandung sejumlah besar sel T CD8 dan CD4. Berbeda dengan sel yang bersirkulasi,ginjalSel T sering mengekspresikan CD69 dan CD103 dan lebih sering aktif bersepeda. Selanjutnya, hampir semuaginjalSel T mengekspresikan CXCR3, dan sering mengekspresikan CXCR6 dibandingkan dengan sel T dalam sirkulasi. Jelas,ginjalSel T menghasilkan jumlah IFN yang lebih besar daripada sel yang bersirkulasi dan seringkali bersifat polifungsional. Kesimpulan: Sel T fungsional dengan ciri khas TRM berada pada manusiaginjaltisu. Sel-sel ini lebih sering aktif bersepeda dan sering mengekspresikan CXCR3 dan CXCR6.
Kata kunci:limfosit residen jaringan; sel-T; CD8; CD4; CD69; CD103; ginjal; allograft

CISTANCHE AKAN MENINGKATKAN PENYAKIT GINJAL/GINJAL
1. PerkenalanSel T memori residen (TRM) bertahan di jaringan untuk memberikan pertahanan lokal jangka panjang terhadap patogen. Berbeda dengan resirkulasi sel T, populasi TRM tidak dapat dideteksi dalam darah perifer, dan berbeda secara signifikan dari populasi sel T resirkulasi dalam hal fenotipe, fungsi, dan metabolisme [1]. Memang, ini tidak mengherankan mengingat fakta bahwa sistem organ yang berbeda, seperti paru-paru, terkena beban yang lebih tinggi dari patogen yang berbeda daripada kasus sirkulasi, yang umumnya terisolasi dari dunia luar [2].Retensi jaringan TkM bertahan selama bertahun-tahun dan dimediasi oleh mekanisme yang melibatkan sumbu Sphingosine-1-phosphate receptor1 (S1PR1)-sphingosine 1-phosphate (SP1). S1PR1 adalah reseptor yang diekspresikan oleh sel T yang memediasi egression dari organ limfoid sekunder setelah mengikat molekul sinyal bioaktif SP1, yang merupakan mediator penting dari perdagangan sel T. Sumbu ini dapat diinterupsi oleh CD69, lektin tipe-c terikat-membran yang menentang ekspresi S1PR1, sehingga memediasi retensi. Lebih lanjut, pada tikus ekspresi S1PR1 diinduksi oleh faktor transkripsi Krüppel-like Factor 2 (KLF2), yang ditemukan diturunkan regulasinya di TRM, sehingga juga menghambat jalan keluar limfosit [3]. Pada gilirannya, downregulasi KLF2 terbukti dimediasi oleh faktor transkripsi homolog Blimpl dalam sel T (Hobit), yang diekspresikan dengan cara spesifik TpM dalam sel T murine [4]. Selanjutnya, beberapa TRM juga mengekspresikan CD103 (integrin E), dimana TRM dapat diidentifikasi menggunakan ekspresi CD69 dan CD103 [1].
Sementara pengetahuan tentang fenotipe dan fungsi TRM meningkat untuk berbagai jaringan manusia, sedikit yang diketahui tentang aspek-aspek ini dalamginjal. Di sini, sel T terpapar pada serangkaian patogen yang berbeda seperti bakteri yang naik dari saluran kemih bagian bawah dan virus renotropik seperti polyomavirus BK (BKPyV). Memang, kami baru-baru ini menggambarkan bagaimana ginjal manusia mengandung subset sel T yang mengekspresikan CD69 dan/atau CD103, di antaranya ada sel T CD8 yang secara khusus menargetkan protein BKpyV, protein virion1(VP1) dan protein antigen T besar (LTAG) [5]. Kami, dan lainnya, juga menunjukkan adanya CD69/CD103-mengekspresikan sel T (MAIT) terkait mukosa diginjaljaringan [6,7].
Untuk lebih memahami jenis sel T apa yang merupakan respons imun terlokalisasi di organ ini, kami menggunakan sitometri aliran multichannel untuk menyelidiki fenotipe dan fungsiginjalTRM, diisolasi dari donorginjalbahan penerima transplantasi ginjal (RTR) dan dari yang sehatginjaljaringan yang berdekatan dengan karsinoma sel jernih ginjal, untuk melihat bagaimana populasi ini dibandingkan dengan populasi sel T dalam sirkulasi.Kami menemukan manusia ituginjaljaringan memegang sejumlah besar sel T CD4 dan CD8 yang mengekspresikan hanya CD69, CD69, dan CD103, atau tidak satupun dari penanda ini. Kami menemukan bahwa sel CD69-CD103- diginjaljaringan berbeda secara substansial dari sel T dalam sirkulasi dan mungkin mewakili populasi TRM yang tidak memiliki penanda TRM kanonik. Lebih lanjut, kami menunjukkan bahwa sel T ginjal lebih sering aktif bersepeda, sebagaimana dinilai dari peningkatan ekspresi Ki-67, bila dibandingkan dengan darah. Kami juga menemukan bahwa sel T CD8 dan CD4 dalamginjaljaringan hampir selalu mengekspresikan CXCR3 dan sering mengekspresikan CXCR6. Temuan ini mengimplikasikan peran reseptor kemokin ini dalam daya tarik dan pemeliharaan populasi sel T memori residen ginjal.
2. Bahan-bahan dan metode-metode
2.1. Pasien dan SampelSampel diperoleh dari Biobank Renal Diseases of the Amsterdam UMC location AMC. Di Biobank ini, sampel pasien, seperti darah danginjaljaringan, dikumpulkan dan disimpan dari hidup sehatginjaldonor dan RTR yang diikuti sebelum dan sesudah transplantasi ginjal. Penelitian ini dilakukan sesuai dengan prinsip-prinsip yang digariskan dalam Deklarasi Helsinki dan Istanbul dan semua peserta memberikan persetujuan tertulis sebelum pendaftaran di Biobank. Selain itu, sisa jaringan dari pasien yang menjalani tumor nephrectomy (jaringan ginjal yang jauh dari tumor) disumbangkan oleh Departemen Patologi dan juga disimpan di Biobank. Jaringan ini diproses secara anonim menurut Kode Etik Federasi Masyarakat Ilmiah Medis Belanda (Penelitian Jaringan dan Medis Manusia: Kode Etik untuk Penggunaan yang Bertanggung Jawab, 2011 www.federa.org).
2.2. Sel Mononuklear Darah Perifer (PBMC)Sampel darah diperoleh dari cytomegalovirus (CMV) -kontrol sehat seronegatif (hidup).ginjaldonor sebelum operasi, n= 13). Karakteristik peserta dalam penelitian ini ditampilkan pada Tabel 1. PBMC diisolasi dari darah natrium heparin dengan sentrifugasi gradien densitas standar dan selanjutnya dikriopreservasi sampai hari analisis.
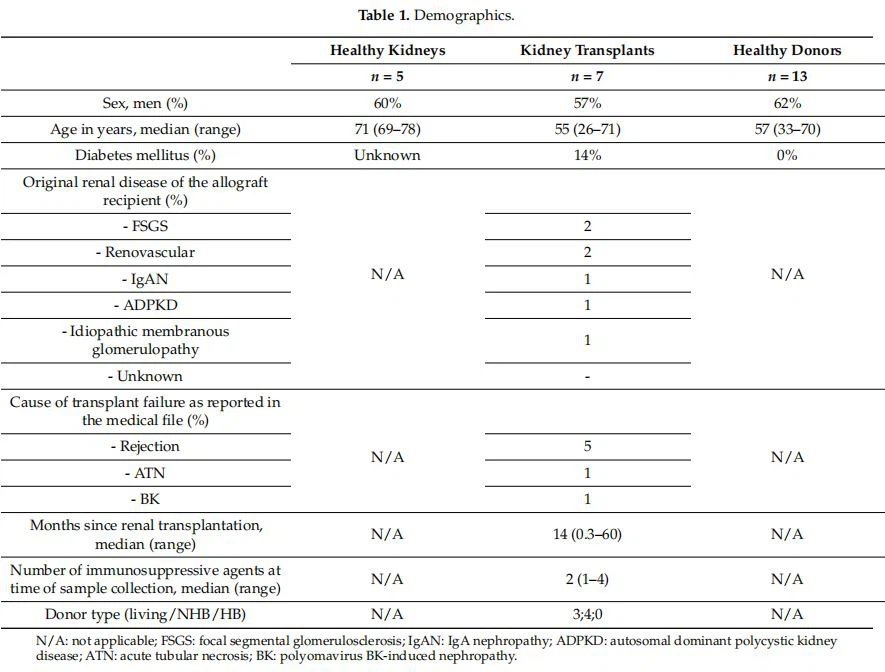
2.3. Jaringan GinjalSampel jaringan ginjal yang sehat (n {{0}}) diperoleh dari ginjal yang diangkat melalui pembedahan karena karsinoma sel ginjal (jaringan nontumor yang jauh dari kutub kontralateral ginjal) dan jaringan ginjal transplantasi (n {{1 }}) diperoleh dari allograft ginjal yang dieksplan setelah kegagalan transplantasi. Sampel ini masing-masing disebut sebagai sampel ginjal yang sehat dan transplantasi. Irisan korteks ginjal dipotong menjadi kubus 1-mm dengan McElwain Tissue Chopper (Ted Pella, Redding, CA, USA), dipindahkan ke tabung 50 mL, dan dicuci dengan PBS dingin sampai tidak ada darah. terlihat jelas dan supernatannya jernih. Media pencernaan yang dipanaskan (37 derajat ) ditambahkan, 40 mL per 10 g jaringan (DNAse Tipe IV (50 KU/mL) (Sigma Aldrich, Zwiindrecht, Belanda), kolagenase tipe IV (0,5 mg/mL) (Worthington Biochemical, Lakewood, NJ, USA), BSA(60 mg/mL)(Sigma Aldrich), 20 uL/mL serum janin betis (FCS, VWR International BV, Amsterdam, Belanda), TRIS (0,025 M)(Merck BV, Amsterdam, Belanda), penisilin-streptomisin (Biochrom GMBH, Berlin, Jerman) di HBSS (Westburg BV, Leusden, Belanda)), dan diinkubasi dalam shaker selama 20 menit pada 37 derajat. Suspensi hangat dipindahkan ke tabung-C (Miltenvi, Bergisch Gladbach, Jerman) dan dikenai program M_limfa_04.01 pada GentleMacs (Miltenyi). Media pencernaan dinonaktifkan dengan PBS dingin dan suspensi sel yang dihasilkan melewati saringan sel untuk mendapatkan suspensi sel tunggal, yang menjadi sasaran sentrifugasi gradien densitas standar sesuai dengan protokol pabrikan (Lymphoprep, Abbott Diagnostics Technologies AS, Oslo, Norwegia ). Sel mononuklear terisolasi (MNC ginjal) adalahcryopreserved sampai hari analisis dalam IMDM ditambah dengan 20 persen FCS,000036 v/v persen -mercaptoethanol, 5 persen DMSO, penisilin, dan streptomisin.
2.4. Aliran SitometriPengukuran dilakukan pada flow cytometer LSRFortessa (BD Biosciences). Untuk setiap sampel, 2x106 PBMC atau 0,5x106 hingga 10x106 MNC ginjal dianalisis. Volume setiap reaksi pewarnaan relatif terhadap jumlah sel dan konsentrasi antibodi tetap konstan. Sel diinkubasi dengan antibodi permukaan (Tabel Tambahan S1) selama 30 menit pada 4 derajat dalam gelap. Sel-sel mati dikeluarkan menggunakan pewarna viabilitas yang dapat diperbaiki eFluor455UV (eBioscience Inc., Thermo Fisher Scientific, San Diego, CA, USA). Antibodi monoklonal dengan target intraseluler (Tabel Tambahan S1) ditambahkan setelah fiksasi dan permeabilisasi sel menggunakan FoxP3/Transcription Factor Staining Set (eBioscience Inc.). Metode yang dipublikasikan untuk flow cytometry dan penyortiran sel untuk tujuan imunologi diikuti [8]. Strategi gating yang digunakan untuk analisis fenotipik dapat ditemukan pada Gambar Tambahan S1. Kami sebelumnya telah menunjukkan bahwa tidak ada penanda yang dianalisis dipengaruhi oleh metode pencernaan yang digunakan untuk mengisolasi MNC ginjal [7].
Keterbatasan sampel jaringan mengakibatkan pengecualian sampel dari panel tirai. Jumlah CD3 plus yang dianalisis per sampel pada PBMC yang sehat, MNC ginjal yang sehat, dan ginjal TX dapat ditemukan pada Gambar S3. Sampel MNC hanya dianalisis ketika mengandung lebih dari 50 persen sel hidup di dalam limfosit, sebagaimana dinilai oleh viabilitas dve, dan subset sel T berbasis CD69/CD103 hanya dikarakterisasi lebih lanjut jika jumlah sel totalnya melebihi 50.

CISTANCHE AKAN MENINGKATKAN GAGAL GINJAL/GINJAL
2.5. Uji StimulasiPBMC dan MNC ginjal dirangsang seperti yang dijelaskan sebelumnya [7,9]. PBMC dan MNC ginjal dicairkan dengan adanya DNAse I (200 KU/mL), dicuci, dan dibiarkan pulih semalaman dalam pelat 96-well plate (Corning) yang tidak diolah, dasar bulat (Corning) dalam media kultur (RPMI dilengkapi dengan 10 persen FCS dan penisilin-streptomisin) pada konsentrasi 20 × 106/mL 100 L/sumur).
Keesokan paginya, phorbol 12-miristat 13-asetat (PMA, 10 ng/mL; Sigma Aldrich) dan ionomycin (1 ug/mL; Sigma Aldrich) ditambahkan untuk merangsang sel. Medium saja ditambahkan sebagai kontrol negatif. Semua inkubasi dilakukan dalam media kultur dengan adanya CD28 (klon 15E8;2 ug/mL), CD29 (klon TS 2/16;1 ug/mL), brefeldin A (10 ug/mL, Invitrogen), dan GolgiStop ( BD Biosciences) dalam volume akhir 200 uL selama 4 jam pada 37 derajat dan 5 persen CO2.
Selanjutnya, sel-sel diinkubasi selama 30 menit dengan antibodi permukaan (Tabel Tambahan S2). Sel-sel mati dikeluarkan menggunakan pewarna viabilitas yang dapat diperbaiki eFluor780 (bioscience Inc., Thermo Fisher Scientific, San Diego, CA, USA). Antibodi monoklonal untuk pewarnaan intraseluler (Tabel S1) ditambahkan setelah fiksasi dan permeabilisasi sel menggunakan Cytofix/Cytoperm Reagent Set (BD Biosciences). Sel dicuci dua kali dan dianalisis pada flow cytometer LSRFortessa. Strategi gating yang digunakan dalam analisis fungsional dapat ditemukan pada Gambar Tambahan S2. Untuk menentukan polifungsi dari setiap subset sel T, jumlah rata-rata fungsi setiap populasi dihitung menggunakan rumus berikut:((persentase sel yang memproduksi 1 sitokin]*1) ditambah ([persentase sel yang memproduksi 2 sitokin]*2) plus ([persentase sel yang memproduksi 3 sitokin]*3) plus ([persentase sel yang memproduksi 4 sitokin]*4) plus ([persentase sel yang memproduksi semua 5 sitokin]*5))/100.
2.6.Analisis Data
Data dianalisis menggunakan FlowJo versi 10 (FlowJo, Ashland, OR, USA). Semua grafik dan gambar dibuat menggunakan Graphpad Prism versi 8.00 untuk Windows(GraphPad Software, La Jolla, CA, USA). Program yang sama juga digunakan untuk analisis statistik data. Uji Mann-Whitney-U nonparametrik digunakan untuk menentukan signifikansi sampel yang tidak berpasangan. Untuk membandingkan sampel berpasangan, uji peringkat bertanda Wilcoxon digunakan. nilai-p<0.05 were="" considered="" statistically="">
3. Hasil
3.1. Ekspresi yang Berbeda dari CD8 dan/atau CD4 dan Penanda Residensi Jaringan oleh Sel T di Jaringan Ginjal SehatPertama, kami membandingkan ekspresi CD4 dan CD8 oleh CD3-sel T positif dalam darah tepi dengan sel yang terdeteksi pada jaringan ginjal yang sehat. CD4-CD8 plus (CD8) Sel T secara signifikan lebih sering terdeteksi di jaringan ginjal daripada di darah ((median)25 persen vs.38 persen )(Gambar la). Sebaliknya, CD4*CD{{9} }(CD4)Sel T terdeteksi dalam frekuensi yang lebih tinggi dalam darah daripada di jaringan ginjal ((70 persen vs.52 persen )Gambar la). Secara keseluruhan, sel T CD4 terlihat lebih sering pada jaringan ginjal yang sehat daripada sel T CD8 (Gambar 1b).
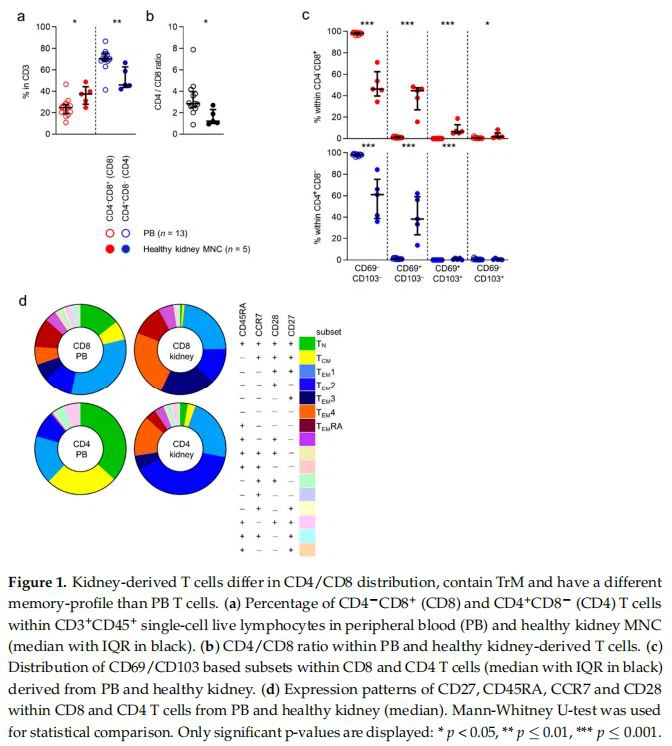
Selanjutnya, kami menyelidiki ekspresi penanda residensi jaringan, CD69 dan CD103, dalam subset sel T yang ditentukan CD8 dan CD4-. Seperti yang diharapkan, CD69 dan CD103 sebenarnya tidak diekspresikan oleh sel-sel dalam darah tepi (Gambar 1c). Dalam jaringan sehat, fenotipe CD69-CD103-, CD69 plus CD103-, CD69tCD103 plus , dan CD69-CD103 plus diekspresikan oleh, 46 persen , 45 persen , 6,6 persen , dan 1,8 persen sel CD8T, masing-masing 61 persen ,38 persen ,0,44 persen , dan 0,43 persen sel CD4T (Gambar lc). Kesimpulannya, CD8, tetapi terutama sel T CD4 terdeteksi dalam jumlah besar di jaringan ginjal manusia yang sehat. Selanjutnya, ekspresi CD69 dan CD103, penanda residensi jaringan, terdeteksi terutama di antara sel T yang ditemukan di jaringan sehat dan bukan dalam darah.
3.2.Pola Ekspresi Berbeda dari Penanda Subset-Denominasi Umum oleh Sel T di Jaringan Kesehatan/oleh Ginjal
CD45RA, suatu tirosin fosfatase, CCR7, suatu reseptor kemokin yang diketahui memediasi perdagangan sel T ke organ limfoid sekunder, dan CD28 dan CD27, keduanya reseptor kostimulatori yang sangat terlibat dalam aktivasi sel T, semuanya merupakan penanda yang secara tradisional digunakan untuk mengidentifikasi subset sel T fungsional J1{ {53}},1l. Kami ingin menyelidiki sejauh mana distribusi himpunan bagian ini dalam darah berbeda dari distribusi di jaringan ginjal. Seperti yang diharapkan, subset sel T CD8 terbesar yang terdeteksi dalam sirkulasi (yaitu, yang mengenai Lebih dari atau sama dengan 5 persen dari total populasi) adalah mereka yang memiliki CD45RA plus CCR7 plus CD28 plus CD27 plus (sel T naif atau TN, ( median) 13 persen ), CD45RA-CCR7 ditambah CD28 ditambah CD27 plus (Tcells memori pusat atau TcM, 6 persen ), CD45RA-CCR7-CD28 ditambah CD27 plus (TEv1,30 persen ), CD45RA-CCR7-CD28 ditambah CD27-(Tau2,10 persen ), CD45RA-CCR7-CD28-CD27*(TEy3,6 persen ) , CD45RA-CCR7-CD28-CD27-(TM4,6 persen )dan CD45RA ditambah CCR7-CD28-CD27-(TEMRA ,10 persen )fenotipe. Dalam jaringan sehat, hampir tidak ada (0,6 persen) sel T CD8 yang terdeteksi dengan fenotipe TN dan hanya sedikit (0,8 persen) yang menunjukkan fenotipe Pajak. Sebaliknya, sel T CD8 yang terdeteksi pada jaringan ginjal yang sehat terdiri dari TEv1-(22 persen ),TEM2-(12 persen ), Tpx3-(18 persen ),TEx{ {65}} (23 persen ), dan TEyRA(11 persen )populasi sel T (Gambar ld dan Gambar S4). Ketika melihat sel T CD4 dalam darah, populasi terbesar adalah mereka yang mengekspresikan Ty-(35 persen ), TcM-(25 persen ), TEMl-(16 persen ), TFM2-(9 persen ), dan populasi dengan fenotipe CD45RAtCCR7-CD28 plus CD27* yang tidak ditentukan lain (0,4 persen )(Gambar 1d dan Gambar S4). Dalam jaringan ginjal yang sehat, beberapa sel T CD4 mengekspresikan TN- (3 persen ) atau TcM -(3 persen )fenotipe. Sebaliknya, sejumlah besar sel dengan fenotipe TEM1-(22 persen ), TEM2-(40 persen ), atau TEM4(14 persen ) terdeteksi di jaringan sehat (Gambar ld dan Gambar S4) . Sebagai kesimpulan, distribusi subset sel T CD8 dan CD4 yang ditentukan CD45RA/CCR7/CD28/CD{} sangat berbeda antara darah dan jaringan ginjal yang sehat.
3.3. Sel T CD8 dan CD4 dalam Jaringan Ginjal Manusia yang Sehat Lebih Sering Terdiri dari Sel Bersepeda AktifSelanjutnya, kami menyelidiki apakah ada perbedaan dalam ekspresi penanda khas profil efektor-memori sitotoksik, antara populasi sel T CD8 dan CD4 dalam darah dan jaringan ginjal. Pertama, kami melihat ekspresi faktor transkripsi T-box T-bet dan eomeso-dermin(Eomes). Regulator transkripsi ini terlibat langsung dalam menghasilkan sel efektor fase akut, menginduksi ekspresi molekul seperti interferon-y dan granzim B, dan dalam generasi respons memori sekunder. Seperti yang diharapkan, ekspresi taruhan-T sering terjadi di antara sel T CD8 peredaran darah (54 persen), sedangkan sel T CD4 peredaran darah jarang mengungkapkan faktor transkripsi ini (13 persen). Menariknya, untuk sel T CD4, ekspresi T-bet secara signifikan lebih tinggi di antara sel T yang terdeteksi di jaringan ginjal yang sehat daripada di sirkulasi (53 persen vs 13 persen). Beberapa ekspresi juga sering terdeteksi di antara sel T CD8 peredaran darah (59 persen), sementara sekali lagi jarang di antara sel T CD4 peredaran darah (15 persen). Namun, ekspresi Eomes lebih sering di antara sel T CD4 di jaringan ginjal (32 persen ) daripada di darah (Gambar 2a,b).
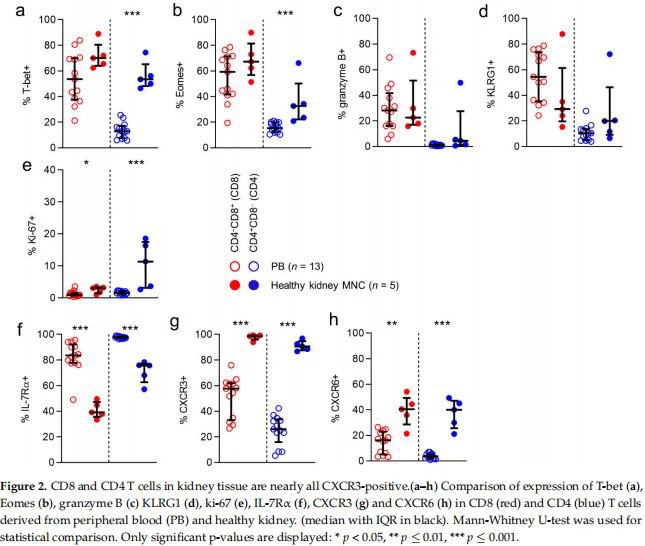
Selanjutnya, kami menyelidiki ekspresi granzyme B, protease serin yang diketahui memediasi apoptosis setelah injeksi ke dalam sitoplasma oleh sel T sitotoksik. Sejalan dengan laporan sebelumnya, T-bet dan ekspresi granzyme B terdeteksi dalam jumlah besar dalam sel T CD8 yang bersirkulasi (28 persen). Namun, ekspresinya jarang terjadi di antara sel T CD4 yang bersirkulasi (1 persen ), Untuk sel T CD8, ekspresi granzim B serupa pada jaringan ginjal dan populasi yang bersirkulasi (28 persen ys.23 persen ) (Gambar 2c). Menariknya, frekuensi ekspresi T-bet dan Eomes yang lebih tinggi yang terdeteksi dalam sel T CD4 ginjal tidak sesuai dengan frekuensi ekspresi granzyme B yang lebih tinggi di kompartemen ini (5 persen). Kami kemudian melihat ekspresi KLRGl, reseptor coinhibitory yang diketahui diekspresikan secara dominan oleh sel efektor fase akut sitotoksik dan sel memori efektor. KLRG1 sering diekspresikan oleh sel T CD8 yang bersirkulasi (54 persen ), tetapi tidak oleh sel T CD4 ( 10 persen ). Tidak ada perbedaan yang ditemukan antara kompartemen anatomi dalam ekspresi KLRG1l untuk sel T CD8 atau CD4. Terakhir, kami menyelidiki ekspresi Ki-67, penanda yang menunjukkan sel yang bersepeda secara aktif. Sejalan dengan pengamatan sebelumnya, ekspresi Ki-67 di antara sel T CD8 dan CD4 yang bersirkulasi jarang terjadi (masing-masing 1 persen dan 2 persen). Menariknya, di antara sel T CD8, tetapi khususnya di antara sel T CD4, ekspresi Ki-67 secara signifikan lebih sering terdeteksi pada sel T di jaringan ginjal (masing-masing 3 persen dan 11 persen) (Gambar 2e). Kesimpulannya, sel T CD4 terdeteksi di jaringan ginjal manusia yang sehat, tetapi tidak sel T CD8 di kompartemen ini, lebih sering diekspresikan T-bet dan Homes. Namun, ini tidak diterjemahkan menjadi ekspresi granzim B yang lebih sering oleh sel T CD4 ginjal. Selain itu, meskipun jumlah keseluruhan sel siklus rendah, jaringan ginjal secara signifikan mengandung sel CD8 dan CD4 siklus yang lebih aktif daripada sirkulasi.
3.4. Sel T CD8 dan CD4 di Jaringan Ginjal Sehat Hampir Semua CXCR3-PosisiKami kemudian mencari perbedaan dalam ekspresi penanda lain, tipikal dalam populasi sel memori sitotoksik yang tidak segera bersirkulasi, seperti yang ditunjukkan sebelumnya untuk populasi sel T yang bersirkulasi. Kami pertama kali melihat ekspresi IL-7R , yang diekspresikan terutama pada sel memori yang naif dan berdiferensiasi awal dalam sirkulasi, di mana ia terlibat dalam mempertahankan proliferasi homeostatik [10,12,13]. Dalam darah tepi, IL-7Ra sering diekspresikan oleh sel T CD8 (84 persen ) dan sel T CD4 (98 persen ). Sel T CD8 dan CD4 dalam jaringan ginjal yang sehat mengekspresikan penanda ini secara signifikan lebih jarang daripada sel T yang bersirkulasi (masing-masing 71 persen dan 76 persen) (Gambar 2f).
Selanjutnya, kami menyelidiki ekspresi berbagai reseptor kemokin lainnya Menariknya, CXCR3, reseptor kemokin yang terlibat dalam perdagangan sel T ke jaringan yang meradang[14-17], diekspresikan oleh sejumlah besar sel T CD8 dan CD4 di jaringan ginjal (99 persen dan 91 persen , masing-masing), dan secara signifikan lebih jarang oleh sel T yang bersirkulasi (masing-masing 58 persen dan 26 persen) (Gambar 2g). Akhirnya, kami menentukan ekspresi CXCR6, yang diketahui terlibat dalam pembentukan populasi TRM [18-22]. Sementara CXCR6 diekspresikan hanya oleh populasi kecil sel T CD8 yang bersirkulasi (16 persen), dan hampir tidak diekspresikan oleh sel T CD4 yang bersirkulasi. proporsi sel T CD8 dan CD4 yang jauh lebih besar dalam jaringan ginjal mengekspresikan molekul ini (masing-masing 40 persen dan 40 persen) (Gambar 2h). Kesimpulannya, penanda yang biasanya terkait dengan keadaan tidak langsung terdiferensiasi dalam sirkulasi, kemungkinan-7Ra, CCR7, CD28, dan CD27, secara signifikan lebih jarang diekspresikan oleh sel CD8 dan T ginjal bila dibandingkan dengan yang ada dalam darah. Sebaliknya, sel T ginjal lebih sering mengekspresikan CXCR6 dan hampir selalu mengekspresikan CXCR3.
3.5.Perbedaan Fenotipe antara Ginjal Sehat dan Sel T Allograft MinimalSelanjutnya, kami ingin menyelidiki apakah temuan ini tetap berdiri di jaringan dari transplantasi allograft ginjal yang diperoleh untuk berbagai indikasi klinis (Tabl 1).Berkenaan dengan jumlah sel T CD8 dan CD4 dalam jaringan sehat dan allograft, tidak ada perbedaan yang terlihat (Gambar 3a). Namun, kami melihat tren yang tidak signifikan menuju lebih banyak sel CD4T dan lebih sedikit sel CD8T di jaringan sehat daripada di jaringan allograft (Gambar 3b). Selain itu, ketika melihat ekspresi CD69/CD103 dan subset yang ditentukan CD45RA/CCR7/CD28/CD27-, tidak ada perbedaan dalam distribusi CD69/CD103- atau CD45RA/CCR7/CD28/CD27- himpunan bagian yang ditentukan dicatat, terlepas dari fenotipe CD8/CD4 (Gambar 3d dan Gambar S5). Ketika memeriksa frekuensi ekspresi penanda yang lebih khas untuk sel T sirkulasi sitotoksik, kami tidak menemukan perbedaan ekspresi T-bet, KLRG1 atau granzyme B antara ginjal yang sehat atau sel T allograft (Gambar 3a, gh). Kami menemukan bahwa ekspresi Eomes terlihat lebih jarang pada sel T CD4 jaringan allograft, dibandingkan pada sel T jaringan sehat (Gambar 3f). Tidak ada perbedaan dalam ekspresi penanda lain yang diamati. (Gambar 3-l dan Gambar S5b-d). Kesimpulannya, terlepas dari frekuensi ekspresi Eomes yang lebih rendah di antara sel T CD4 allograft, populasi sel tidak berbeda di antara populasi penelitian.
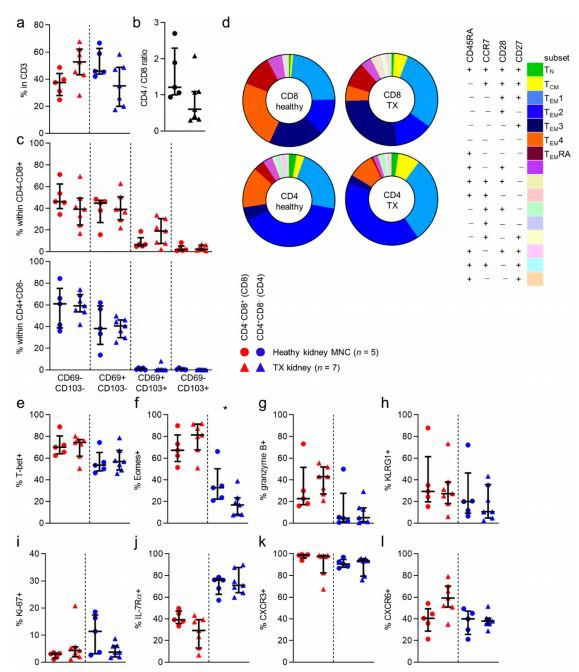

3.6. CD69-CD103-Sel T di Jaringan Ginjal Berbeda dengan Sel yang BeredarMengingat susunan fenotipik sel T CD8 dan CD4 yang serupa ditemukan pada jaringan ginjal yang sehat dan pada jaringan allograft ginjal, kami mengumpulkan data dari kedua kelompok studi untuk memeriksa lebih lanjut karakteristik sel-sel ini menurut ekspresi CD69 dan CD103. Karena sel CD69-CD103 plus selalu terdeteksi dalam frekuensi yang sangat rendah(<50 events),="" we="" excluded="" these="" cells="" from="" further="" analyses.="">Pertama, kami menyelidiki perbedaan dalam himpunan bagian ini menurut co-ekspresi CD69/CD103 dalam populasi sel T ginjal (Gambar 4 dan Gambar S6). Menariknya, untuk sel T CD8 dan CD4, perbedaan substansial dicatat dalam distribusi subset yang ditentukan CD45RA/CCR7/CD28/CD27-di antara CD69-CD103-,CD69 plus CD{ {14}}dan subset CD69*CD103*. Untuk sel T CD8, sel CD69-CD103-mengandung populasi sel TeyRA yang cukup besar (21 persen ) yang jauh lebih kecil di antara subset CD69 plus CD103- dan CD69 plus CD103 (5,8 persen dan 2,2 persen , masing-masing). Sebaliknya, populasi terakhir ini berisi TEy3 jauh lebih besar (masing-masing 13 persen, 30 persen, dan 32 persen) dan TEy4 (masing-masing 8 persen, 19 persen, dan 33 persen) subpopulasi. Untuk sel T CD4, beberapa sel TEyRA terlihat di antara subset CD69-CD103-, CD69*CD103-, dan CD69 plus CD103* (2,6 persen ,0 persen , dan 1,7 persen , masing-masing). Sebaliknya, sel-sel ini memiliki subpopulasi besar TFw1 (masing-masing 26 persen, 24 persen, dan 10 persen) dan TEy2 (masing-masing 30 persen, 46 persen, dan 27 persen). Di antara CD69 plus CD103-dan khususnya di antara sel CD69*CD103*, subpopulasi TEM4 yang jauh lebih besar terlihat (masing-masing 6 persen , 11 persen dan 34 persen ).
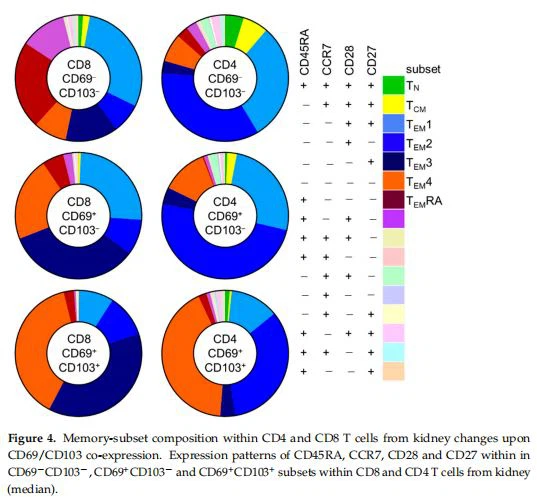
Mengingat perbedaan ini dan pengamatan sebelumnya bahwa populasi sel T ginjal hampir tidak terdiri dari sel TN dan TcM, kami menyelidiki lebih lanjut sel CD69-CD103-yang ditemukan di jaringan ginjal untuk menentukan sejauh mana sel-sel ini tidak hanya sel-sel yang bersirkulasi melewati sirkulasi ginjal. Untuk melakukannya, kami membandingkan sel-sel ini dengan sel-sel yang bersirkulasi. CD69-CD103~sel di jaringan ginjal berbeda secara signifikan dari yang ada di sirkulasi: T-bet, Ki-67, dan CXCR3 lebih sering diekspresikan oleh sel T ginjal, terlepas dari fenotipe CD8/CD4 (Gambar 5a-c). Sebaliknya, IL-7R , CCR7, CD28, dan CD27 semuanya diekspresikan secara signifikan lebih jarang oleh sel T ginjal CD69-CD103-, terlepas dari fenotipe CD8/CD4 (Gambar 5d- g). CD69-CD103-Tsel CD4 dalam jaringan ginjal mengekspresikan KLRG1 secara signifikan lebih sering daripada dalam darah dan CD69-sel T CD103-CD8 dalam jaringan ginjal mengekspresikan Eomes secara signifikan lebih sering daripada dalam darah.

Selanjutnya, kami ingin melihat bagaimana koekspresi CD69 dan CD103 memengaruhi penanda potensi fungsional. Pertama, kami melihat penanda yang terkait dengan potensi sitotoksik. Meskipun perbedaan dicatat antara subpopulasi individu, tidak ada pola konsekuen yang terlihat untuk T-bet dan Eomes dalam sel T CD8 ketika CD69 atau CD103 diekspresikan bersama (Gambar 6a,b). Sebaliknya, pada sel T CD4 faktor transkripsi ini keduanya meningkat bersama dengan Koekspresi CD69 dan CD103 (Gambar 6a,b). Saat melihat KLRG1, kami memperhatikan bahwa untuk sel T CD8, ekspresi KLRG1 menurun bersama dengan koekspresi CD69/CD103. Untuk sel T CD4 tren serupa terlihat. Namun, di sini hanya sel CD69-CD103-yang mengekspresikan KLRG1 pada frekuensi yang lebih tinggi daripada sel CD69 plus CD103- dan CD69 plus CD103* (Gambar 6c). Frekuensi ekspresi granzyme B juga menurun bersama dengan penanda residensi jaringan, dengan frekuensi ekspresinya paling rendah di antara sel CD69 plus CD103*, dalam sel T CD8 dan CD4 (Gambar 6d). Ekspresi Ki-67, yang lebih tinggi di antara sel T ginjal bila dibandingkan dengan sel T dalam darah, tidak berbeda menurut koekspresi CD69 atau CD103 (Gambar 6e).
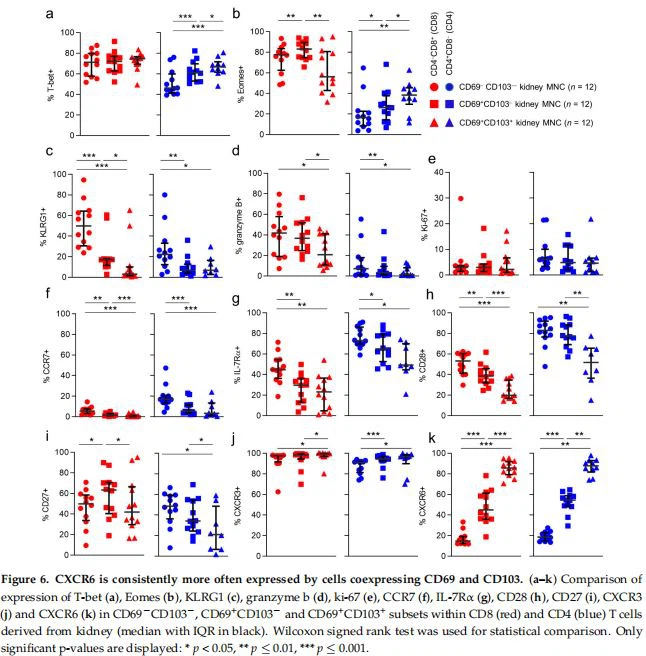
Kami kemudian menyelidiki penanda yang biasanya terkait dengan profil memori nonsitotoksik menurut koekspresi CD69/CD103. Ekspresi IL-7Ra, CCR7, dan CD28 tertinggi dalam populasi CD69-CD{103-, dengan tren dalam mendefinisikan ekspresi bersama dengan koekspresi CD69/CD103 (Gambar 6f-h ). Kami kemudian melihat ekspresi CXCR3 dan CXCR6. Kedua reseptor kemokin paling sering diekspresikan oleh sel CD69tCD103t, terlepas dari fenotipe CD8/CD4, dan menunjukkan tren naik dengan koekspresi CD69/CD103. Hanya untuk CXCR6, tren ini signifikan secara statistik, mempengaruhi jumlah CD8 dan CD4 (Gambar 6j,k). Kesimpulannya, sel CD69-CD103- di jaringan ginjal berbeda secara substansial dari sel dalam sirkulasi dan mungkin menyangkut populasi TBv lain yang tidak ditandai dengan ekspresi CD69 atau CD103. Satu-satunya penanda yang berbeda secara konsisten, terlepas dari fenotipe CD8/CD4, dalam hal koekspresi CD69 dan CD103, adalah CXCR6.
3.7. Sel T di Jaringan Ginjal Lebih Sering Menghasilkan Interferon daripada Sel T dalam DarahAkhirnya, kami menyelidiki kapasitas produksi sitokin oleh CD8/CD4-populasi sel T yang ditentukan dalam jaringan ginjal. Pertama, kami membandingkan produksi interferon-y (IFNy), faktor nekrosis tumor (TNF ), interleukin-2 (IL-2), faktor perangsang koloni granulosit-makrofag (GM-CSF), dan IL-17 oleh CD8/CD terstimulasi4-mendefinisikan populasi sel T yang ditemukan dalam darah dengan yang ada di jaringan ginjal yang sehat (Gambar 7a-e). Menariknya, hanya IFNy yang secara konsisten diekspresikan oleh proporsi sel T yang lebih besar dalam jaringan ginjal yang sehat, jika dibandingkan dengan sel T dalam darah, terlepas dari fenotipe CD8/CD4 (Gambar 7a). Perbedaan juga terlihat pada tingkat subset individu. Secara khusus, TNF dan GM-CSF lebih sering diproduksi oleh sel T CD4 di jaringan ginjal (Gambar 7b.c). Berkenaan dengan polifungsi (yaitu, jumlah sitokin yang diproduksi secara bersamaan), sel T CD4 dalam jaringan ginjal ditemukan lebih polifungsional daripada sel CD4 dalam darah (Gambar 7f).
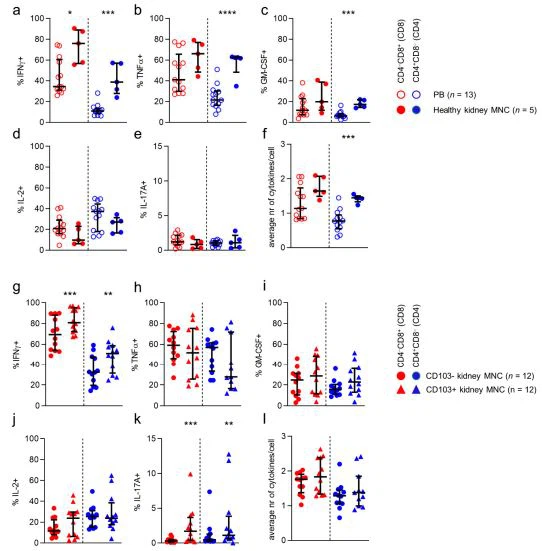

Selanjutnya, kami melihat perbedaan kapasitas produksi sitokin antara sel T terstimulasi dari jaringan sehat dan allograft. Tidak ada perbedaan dalam produksi sitokin individu, atau dalam sejumlah sitokin yang diproduksi secara bersamaan terdeteksi antara sel T dari jaringan ginjal yang sehat atau allograft (Gambar S7). Karena CD69 diekspresikan pada stimulasi sel T, kami hanya mempelajari perbedaan antara CD103-negatif dan CD103-yang mengekspresikan CD4 dan CD8 sel T (Gambar 7g-). Ketika membandingkan sel T CD4 dan CD8 yang mengekspresikan CD103 dengan sel yang tidak mengekspresikan CD103 dalam jaringan ginjal, kami melihat bahwa sel CD8 dan CD4 CD103 mengekspresikan lebih banyak IFNy daripada sel CD103-(Gambar 7g). Selain itu, meskipun sel penghasil IL-1ZA rendah di antara sel CD103 plus CD8 dan CD4 T di jaringan ginjal, mereka secara konsisten ditemukan lebih sering pada populasi ini dibandingkan dengan populasi CD103-. Kesimpulannya, lebih banyak sel T' di jaringan ginjal yang menghasilkan IFNy jika dibandingkan dengan sel T yang bersirkulasi, terlepas dari fenotipe CD8/CD4. Memang, persentase tertinggi sel penghasil IFNy ditemukan di antara CD 103-mengekspresikan CD4 dan CD8 sel T yang diturunkan dari ginjal. Selain itu, sel T pada alograf ginjal tidak berbeda dengan sel T pada jaringan ginjal yang sehat dalam hal parameter ini.
4. Diskusi
Dalam penelitian saat ini kami membahas keragaman subset sel T, menurut ekspresi CD8 dan CD4, dan penanda residensi jaringan, CD69 dan CD103, pada ginjal manusia dan membandingkannya dengan darah. Sejumlah besar sel T CD8 dan CD4 memang terdeteksi di jaringan ginjal. Selanjutnya, sel T di ginjal ini mengandung sejumlah besar sel CD69*CD103-. Sel CD69 plus CD103 plus juga terdeteksi, tetapi sebagian besar di antara sel T CD8 dan hampir tidak ada di antara sel T CD4. Temuan serupa terkait TRM paru sebelumnya [23]. Seperti yang diharapkan, populasi pengekspresi CD69 dan CD103-seperti itu malah hampir tidak ada dalam sirkulasi. Perbedaan mencolok ketika membandingkan sel T di ginjal dengan yang ada di darah, berkaitan dengan distribusi yang berbeda dari subset yang ditentukan CD45RA/CCR7/CD28/CD27-tradisional. Menariknya, ekspresi CD28 lebih sering tidak diekspresikan ketika sel T mengekspresikan CD69 sendiri atau dalam kombinasi dengan CD103. Secara teoritis, ini akan membuat populasi ini kurang rentan terhadap sinyal kostimulatori oleh CD80 dan CD86. Perbedaan lain menyangkut frekuensi ekspresi CXCR3, CXCR6, dan Ki-67 yang lebih tinggi. Selain itu, sel T ginjal lebih sering mengandung sel penghasil IFNy dan sering polifungsional. Memang, di dalam ginjal, CD103 plus Tpys mengandung lebih banyak sel penghasil IFN daripada rekan CD103-negatif mereka. Selain itu, sel CD103T lebih sering menghasilkan IL-17, meskipun ini menyangkut Populasi sederhana.

CISTANCHE AKAN MENINGKATKAN INFEKSI GINJAL/GINJAL
Berkenaan dengan ekspresi CXCR3 yang lebih sering oleh sel T ginjal CD8 dan CD4, sumbu CXCR3/CXCL10 sebelumnya terbukti terlibat dalam pembentukan populasi TpM di kulit, hati, dan jaringan limfoid [24-28]. Selain itu, terlibat dalam perdagangan ke epitel stres dan peradangan dalam arti umum [14-17]. Mengingat frekuensi tinggi CXCR3 di antara sel-sel T ini dalam jaringan ginjal yang sehat, CXCR3 tampaknya juga terlibat dalam homeostasis TRM di jaringan ginjal dan mungkin tidak selalu melibatkan peradangan atau sinyal bahaya untuk melakukannya. Berkenaan dengan CXCR6, sumbu CXCR6/CXCL16 memang telah terbukti penting untuk perdagangan Tpst ke kompartemen yang berbeda seperti paru-paru, kulit, hati, dan otak, dan mungkin menyangkut mekanisme universal yang penting untuk memandu dan mempertahankan TRM ke dan di jaringan, juga tentang TRM di jaringan ginjal manusia [18-22].
Farber dan rekan kerja telah secara ekstensif mengkarakterisasi dan membandingkan populasi CD8 dan CD4 TRM yang berada di berbagai jenis jaringan manusia yang berasal dari donor organ. Mereka menggambarkan bagaimana populasi TRM di paru-paru, limpa, usus kecil, dan berbagai jaringan limfoid sekunder berbeda sehubungan dengan transkriptom, tetapi juga untuk ekspresi berbagai protein, termasuk sitokin, diselidiki dalam penelitian ini [29-31. Namun, penyelidikan ini tidak mencakup populasi TRM di ginjal manusia, dan data tentang ini
subjeknya langka. Kami sebelumnya menunjukkan bahwa sel T CD8 yang menargetkan protein polyomavirus BK VP1 dan LTAG, yang berasal dari virus yang memiliki tropisme kuat untuk sel epitel ginjal, dapat dideteksi pada ginjal allograft. Sel T spesifik virus ini mengekspresikan CD69 dan CD103 dalam jumlah yang lebih tinggi daripada rekan mereka yang ditemukan dalam sirkulasi pasien yang sama. Selanjutnya, sel T ini umumnya mengekspresikan fenotipe CD45RA-CD27-granzyme B-negatif[5]. Kemudian, yang lain juga melaporkan populasi TRM dalam jaringan ginjal manusia yang diperoleh dari nefrektomi transplantasi. Dalam publikasi ini, penulis melaporkan bahwa sel T dalam jaringan ini terutama berkaitan dengan sel T CD8 [321. Kami malah menemukan bahwa sel T CD4, pada kenyataannya, terdiri dari subset sel T terbesar. Namun, kami juga menemukan bahwa keseimbangan bergeser, meskipun tidak signifikan, menuju jumlah sel T CD8 yang lebih besar dalam jaringan allograft jika dibandingkan dengan jaringan ginjal yang sehat. Dengan demikian, perbedaan ini dapat dijelaskan oleh kelompok studi yang berbeda, dan mungkin dalam kesehatan, pertahanan imunologis lebih terfokus pada ancaman ekstraseluler, seperti bakteri, dibandingkan ancaman intraseluler yang lebih banyak, seperti virus dan kanker pada inang yang immunocompromised. Kami tidak menemukan perbedaan lain dalam penanda yang dipelajari, antara ginjal yang sehat dan sel T allograft. Namun, penelitian lebih lanjut, menggunakan teknik dengan pandangan yang lebih luas pada transkriptom, seperti sekuensing RNA, atau proteom, seperti spektrometri massa, harus digunakan untuk menentukan apakah ini memang kasusnya.
Selain itu, de Leur et al. menggambarkan bagaimana TRM di ginjal sering mengekspresikan granzyme B, sementara kami hanya mendeteksi granzyme B dalam jumlah rendah di kedua jaringan ginjal sehat dan allograft [32]. Namun, kami mendeteksi sel T-bet dan sel T yang mengekspresikan Eomes dalam jaringan ginjal, yang dalam populasi sel T yang bersirkulasi, biasanya memang terkait dengan ekspresi granzim B yang lebih tinggi [10]. Sementara yang terakhir mungkin tidak mengejutkan, mengingat fakta bahwa ekspresi granzim B juga secara langsung diinduksi oleh T-bet [33,34], hubungan ini tidak terlihat di antara sel T ginjal dalam penelitian ini. Seperti yang kami dan orang lain telah tunjukkan bahwa TRM yang diturunkan dari paru-paru, otak, dan kulit manusia [25,26,3536], serta MAIT lls 6,7】 yang berasal dari jaringan yang berasal dari ginjal memiliki kadar granzim B yang rendah. konten, sementara sering mengekspresikan sejumlah besar T-taruhan dan Eomes, ini mungkin merupakan ciri umum TkM (manusia). Selanjutnya, ekspresi granzyme B TRM paru terlihat diregulasi dengan cepat pada stimulasi [35l, menunjukkan bahwa ini mungkin juga terjadi pada TeM lainnya. Di sini, penulis berhipotesis bahwa 'sitotoksisitas tersembunyi tersebut berfungsi untuk melindungi integritas struktural jaringan dari kerusakan oleh sel T sitotoksik.

Sebagai kesimpulan, kami menunjukkan bahwa T cls dalam jaringan ginjal hadir dalam jumlah besar dan terdiri dari populasi yang sering mengekspresikan CD69 plus dan CD103 plus , molekul di mana sel T melekat, dan bertahan di, jaringan. Namun demikian, sel T CD69-CD103- di jaringan ginjal tampaknya berbeda dari sel T yang bersirkulasi dan mungkin menyangkut populasi TiM lain yang berbeda, mungkin bertahan di ginjal oleh mekanisme lain yang akan diungkapkan oleh dokter hewan. Pilihan lain mungkin bahwa sel CD69-CD103-T ini menyangkut populasi yang baru saja keluar dari sirkulasi, dan haye hanya memperoleh sifat fenotipik baru secara sementara karena interaksi dengan lingkungan mikro ginjal. Investigasi lebih lanjut ke populasi ini diperlukan untuk menjelaskan kemungkinan ini. Lebih-lebih lagi. Sel T ginjal CD8 dan CD4 sering aktif bersepeda dan lebih sering mengekspresikan CXCR6. Selain itu, populasi CD8 dan CD4 menggantikan ekspresi CXCR3 yang sangat tinggi, yang secara kuat melibatkan reseptor kemokin ini, serta CXCR6 dalam akrual TRM dan kegigihan pada ginjal manusia. Oleh karena itu, penyelidikan lebih lanjut diperlukan untuk meningkatkan citra kami tentang populasi Tpv di ginjal manusia. Namun demikian, temuan yang disajikan di sini membentuk langkah pertama yang solid menuju karakterisasi populasi sel T yang lebih rinci dalam jaringan ginjal dan perannya dalam kesehatan dan penyakit.
