Bioassay Untuk Memantau Efek Anti-penuaan Perawatan Darah Tali Pusat
Feb 27, 2022
Kontak:jerry.he@wecistanche.com
Sang-Hun Bae1*, Ala Jo1,2*, Jae Hyun Park1, Chul-Woo Lim1, Yuri Choi1, Juhyun Oh2, Ji-Min Park1, TaeHo Kong1, Ralph Weissleder2,3, Hakho Lee2, Jisook Moon1
1. Departemen Bioteknologi, Sekolah Tinggi Ilmu Hayati, Universitas CHA, Gyeonggi-do 13488, Republik Korea
2. Pusat Biologi Sistem, Rumah Sakit Umum Massachusetts, Sekolah Kedokteran Harvard, Boston, MA 02114, AS
3. Department of Systems Biology, Harvard Medical School, Boston, MA 02115, USA *Para penulis ini memberikan kontribusi yang sama.
Penulis koresponden: Hakho Lee, PhD. Pusat Sistem Biologi, Rumah Sakit Umum Massachusetts, 185 Cambridge St, CPZN 5206, Boston, MA 02114, AS. 617-726-8226 hlee@mgh.harvard.edu Jisook Moon, PhD. Departemen Bioteknologi, Sekolah Tinggi Ilmu Hayati, Universitas CHA, Pangyo-ro 335, Bundang-gu, Seongnam-si, Gyeonggi-do 13488, Republik Korea. 82-31-881-7210 jmoon@cha.ac.kr
© Penerbit Internasional Ivyspring. Ini adalah artikel akses terbuka yang didistribusikan di bawah persyaratan lisensi Creative Commons Attribution (CC BY-NC) (https://creativecommons.org/licenses/by-nc/4.0/). Lihat http://ivyspring.com/terms untuk syarat dan ketentuan lengkap.
Diterima: 2018.10.04; Diterima: 2018. 11. 18; Diterbitkan: 2019.01.01

Cistanche memiliki efek anti-penuaan
Abstrak
Latar belakang: Mengobati hewan tua dengan plasma tahap perkembangan awal (misalnya, plasma tali pusat) menunjukkan potensi yang mengesankan untuk memperlambat degradasi fungsi saraf dan kognitif terkait usia. Menerjemahkan temuan tersebut ke realitas klinis, bagaimanapun, membutuhkan cara yang efektif untuk menilai kemanjuran pengobatan; metode ideal harus minimal invasif, setuju untuk tes serial, hemat biaya, dan kuantitatif.
Metode: Kami mengembangkan pendekatan biosensor baru untuk memantauanti penuaanterapi. Kami memajukan dua komponen sensor utama: i) metabolit yang terbawa darah diidentifikasi sebagai penanda penuaan pengganti; dan ii) sistem pengujian yang ringkas dan hemat biaya dikembangkan untuk aplikasi di lokasi. Kami merawat tikus tua baik dengan plasma tali pusat manusia atau saline; profil metabolit yang tidak bias pada plasma tikus mengungkapkan asam arakidonat (AA) sebagai indikator kuat yang terkait dengananti penuaanmemengaruhi. Kami selanjutnya menerapkan sensor magneto-elektrokimia kompetitif (cMES) yang dioptimalkan untuk deteksi AA langsung dari plasma. Platform yang dikembangkan dapat mendeteksi AA langsung dari plasma volume kecil (0.5 L) dalam waktu 1,5 jam.
Hasil: uji cMES mengkonfirmasi korelasi yang kuat antara kadar AA danefek anti penuaan: Tingkat AA, sementara menurun seiring bertambahnya usia, meningkat pada tikus tua yang diobati dengan plasma yang juga menunjukkan peningkatan kinerja pembelajaran dan memori.
Kesimpulan: Platform cMES akan memberdayakan pra-dan klinisanti penuaanpenelitian dengan memungkinkan pengawasan pengobatan longitudinal minimal invasif; kapasitas ini akan mempercepat pengembangananti penuaanterapi, meningkatkan kualitas hidup individu.
Kata kunci: Anti-penuaan, Asam arakidonat, Profil metabolit, Sensor Magneto-elektrokimia, Biosensor
pengantar
Penuaan semakin diakui sebagai faktor risiko klinis untuk degenerasi kognitif (misalnya, neurodegenerasi, demensia) dan penyakit kronis lainnya (misalnya, kanker, penyakit kardiovaskular, degenerasi otot) [1]. Dengan bertambahnya umur manusia dan bertambahnya populasi lansia, upaya signifikan sedang dilakukan untuk menjelaskan mekanisme penuaan [1–3] dan untuk menemukan strategi terapi untuk memperlambat atau bahkan membalikkan proses penuaan [4]. Memang, hasil yang menjanjikan dari penelitian pada hewan telah dilaporkan; tikus dewasa yang menerima transfusi plasma dari tikus muda mendapatkan kembali fungsi kognitif, plastisitas sinaptik, dan aktivitas saraf [5]. Perkembangan pesat dianti penuaanperawatan dan terjemahannya ke dalam percobaan manusia diantisipasi [6]. Metrik saat ini untuk memantau efek pengobatan, bagaimanapun, memiliki kepraktisan yang terbatas, karena metode seringkali sulit untuk diterapkan pada manusia (misalnya, pencitraan otak invasif, pengamatan perilaku terkontrol) dan subjektif (misalnya, kuesioner tentang pengalaman pasien). Salah satu syarat utama dalam memajukananti penuaanterapi sehingga terletak pada pengembangan kuantitatif, tes invasif minimal untuk pemantauan pengobatan.
Kami beralasan bahwa metabolit akan menjadi sumber yang kuat untukanti penuaanbiomarker. Metabolit adalah fenotipe penting dalam suatu organisme dan sedang dipelajari sebagai biomarker diagnostik untuk penyakit lain [7]. Secara khusus, penuaan biasanya dikaitkan dengan perubahan atau disfungsi metabolik, yang mempengaruhi profil metabolit secara keseluruhan dalam organisme. Dengan demikian, dapat dibayangkan bahwa penelusuran komposisi dan/atau kadar metabolit akan menginformasikan kemanjurananti penuaanperlakuan. Selanjutnya, uji metabolit, khususnya dalam bentuk tes darah, dapat bersifat kuantitatif dan minimal invasif; manfaat ini akan memfasilitasi penerapan rejimen pengobatan atau kelompok pasien yang berbeda, dan memantau dinamika (anti-)penuaan melalui pengambilan sampel serial.
Kami di sini menjelaskan strategi biosensor baru untuk pemantauananti penuaanperlakuan. Dua elemen kunci dikembangkan: i) metabolit yang terbawa darah diidentifikasi sebagai penanda penuaan pengganti; dan ii) sistem pengujian yang cepat dan hemat biaya dikembangkan untuk aplikasi dalam pengaturan klinis rutin. Secara khusus, kami merawat sekelompok tikus tua (sekitar 2 tahun) dengan plasma dari darah tali pusat manusia. Analisis metabolomik komprehensif pada darah tikus mengungkapkan bahwa asam arakidonat (AA), yang kadarnya menurun secara signifikan seiring bertambahnya usia, sebaliknya meningkat pada kelompok yang diobati. Pengamatan ini mengarahkan kami untuk merancang sensor magneto-elektrokimia untuk target molekul kecil: kami mengoptimalkan reaksi elektrokimia kompetitif di mana AA ditangkap pada manik-manik magnetik dan terkonsentrasi untuk sensitivitas yang lebih tinggi. Platform yang dikembangkan dapat mendeteksi AA langsung dari volume plasma kecil (0.5 L) dalam waktu 1,5 jam. Dengan menggunakan platform ini, kami selanjutnya dapat membangun korelasi positif antara kadar AA darah dan kinerja hewan yang lebih baik dalam tugas motorik.
Hasil
Mengobati tikus dewasa dengan plasma darah tali pusat Gambar 1a menunjukkan skema percobaan secara keseluruhan.
Sebagai agen, kami menggunakan plasma yang berasal dari sampel darah tali pusat manusia. Studi sebelumnya menunjukkan bahwa tikus tua yang disuntik dengan plasma tikus muda memulihkan fungsi memori spasial, dan pemberian sistemik plasma darah tali pusat meningkatkan kognisi yang bergantung pada hipokampus pada tikus tua [5, 8]. Menyuntikkan plasma, yang tidak memiliki komponen seluler, meminimalkan risiko penolakan kekebalan yang berasal dari ketidakcocokan spesies. Tikus tua (usia mulai, 18 bulan) diacak dan menerima plasma (kelompok perlakuan) atau buffer salin (kelompok palsu) melalui injeksi tail-vain (130 L; lihat Gambar. S1 untuk detailnya). Sebagai kontrol positif, digunakan mencit muda (3 bulan). Plasma yang berasal dari darah tali pusat tidak dikumpulkan dan setiap tikus berulang kali diinfus dengan plasma dari donor yang sama (Gbr. S1). Setelah pengobatan 4-minggu, tikus menjadi sasaran tes perilaku (yaitu, rotarod), dan darah diambil untuk analisis.
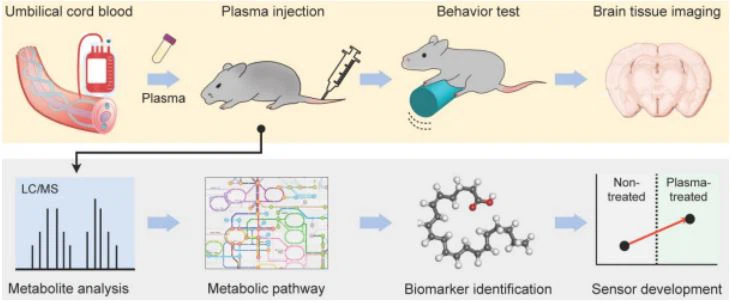
Gambar 1. Desain Eksperimental. Plasma darah tali pusat manusia diberikan kepada kelompok muda (3-bulan), tua (20- dan 23-bulan), dan kelompok tua yang diobati dengan plasma (20- dan 23-berusia sebulan). Ketiga kelompok menjadi sasaran 2-tes percobaan Rotarod untuk mengukur koordinasi motorik dan pembelajaran. Profil metabolit yang tidak ditargetkan dilakukan pada darah dari tiga kelompok, dan yang paling banyakanti penuaanJalur yang relevan ditentukan melalui pendekatan bioinformatika. Biosensor dikembangkan untuk mendeteksi metabolit terpenting dari jalur tersebut.
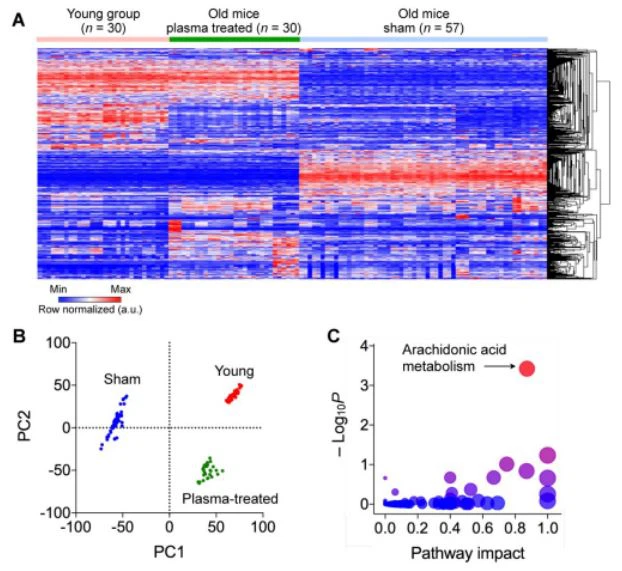
Gambar 2. Penentuan biomarker metabolit yang terkait dengan pengobatan plasma darah tali pusat manusia. (A) Profil global gangguan metabolit. Baris sesuai dengan fitur (kombinasi unik dari nilai m/z dan waktu retensi) dari LC/MS dan kolom ke sampel. Baris dikelompokkan secara hierarkis. (B) Plot skor PCA untuk pengurangan dimensi. Sampel diplot terhadap komponen utama (PC) 1 dan 2. Nilai dalam tanda kurung legenda sumbu adalah proporsi varians yang dijelaskan oleh komponen tersebut. PC1 kemungkinan besar menjelaskan efek anti-penuaan, mengingat bahwa kelompok perlakuan plasma lebih dekat dengan kelompok muda daripada kelompok palsu. (C) Analisis pengayaan jalur. Metabolit diidentifikasi dengan mencocokkan nilai m/z terukur dengan informasi massa molekul. Setiap lingkaran mewakili jalur tertentu yang ditemukan. Untuk jalur tertentu, lokasi x atau ukuran lingkaran sesuai dengan sentralitas relatif-antara (ukuran dampak jalur) metabolit, dan lokasi atau warna y (nilai p lebih rendah untuk merah dan lebih tinggi untuk biru) sejauh metabolit mana yang terwakili secara berlebihan. Jalur dominan memiliki nilai x dan y yang lebih tinggi. Dengan demikian, metabolisme asam arakidonat (AA) diidentifikasi sebagai jalur yang paling mungkin untuk menjelaskanefek anti penuaandari plasma darah tali pusat.

Analisis metabolik pada sampel darah tikus
Kami pertama kali melakukan profil metabolit molekul kecil yang tidak bias dalam plasma tikus. Sampel darah dari ketiga kelompok tikus menjadi sasaran analisis kromatografi cair dan spektrometri massa (LC/MS). Kami memproses data m/z dengan MAIT (perangkat identifikasi otomatis metabolit) dan mengidentifikasi fitur yang signifikan secara statistik melalui ANOVA (8572 kombinasi unik m/z dan waktu retensi) (Gbr. 2a). Analisis pengelompokan hierarkis (HCA) metabolit mengungkapkan dua pola utama: i) profil metabolit berbeda antara tikus tua (tidak diobati) dan tikus muda; dan ii) profil tikus tua yang diobati dengan plasma lebih dekat dengan tikus muda.
Analisis komponen utama (PCA) mengungkapkan struktur yang melekat pada data metabolomik (Gbr. 2b). Sekitar 50 persen dari total variasi dijelaskan oleh komponen utama pertama (PC1) dan kedua (PC2). Ketiga kohort (yaitu, kelompok muda, perlakuan plasma, dan kelompok palsu) menetap pada posisi terpisah, menunjukkan bahwa fitur yang relevan secara biologis untuk membedakan kelas kelompok telah diidentifikasi. Menariknya, kelompok tua yang diobati dengan plasma menjauh dari kepura-puraan menuju kelompok muda. Untuk mengukur pemisahan kelompok, kami menghitung pengelompokan hierarkis pada dua komponen utama. Dalam dendrogram, kelompok muda dan kelompok yang diberi perlakuan plasma dikelompokkan pada tingkat ketidaksamaan yang lebih rendah (atau tingkat kesamaan yang lebih tinggi, 1120,9) dibandingkan kelompok yang tidak diobati (3162,5) (Gbr. S2). Hasil ini menunjukkan bahwa fitur yang dipilih (variabel atau baris pada Gambar. 2a) dapat digunakan untuk menyimpulkan biomarker metabolit yang relevan dengan penuaan dananti penuaan. Kami menjelaskan fitur dengan metabolit yang diketahui menggunakan database di domain publik [9].
Kami selanjutnya menilai fungsi dan interkonektivitas dari metabolit yang teridentifikasi, menerapkan pemetaan KEGG (Kyoto Encyclopedia of Gens and Genomes) [10]. Untuk jalur tertentu, kami mengukur i) representasi yang berlebihan dari calon metabolit dan ii) pentingnya (yaitu, sentralitas antara) [11] sebagai simpul perantara utama antara pasangan metabolit lain (lihat Metode untuk detailnya). Kami menemukan bahwa metabolisme asam arakidonat (AA) adalah jalur yang paling banyak terwakili (nilai y tertinggi pada Gambar. 2c), dan metabolit dalam jalur tersebut cenderung berada di jalur komunikasi (nilai x yang lebih tinggi pada Gambar. 2c) dan mengatur arus informasi. Di antara banyak metabolit dalam metabolisme AA, kami memilih AA itu sendiri sebagai biomarker; sebagai awal masuk ke jalur, AA sendiri dapat menjadi perwakilan dari metabolit terganggu lainnya.
Sensor magneto-elektrokimia kompetitif (cMES) untuk deteksi AA dalam plasma
Kami selanjutnya berangkat untuk memajukan sistem pengujian di tempat yang cepat untuk deteksi AA. Kami memilih untuk menggunakan teknologi penginderaan magneto-elektrokimia [12-17]. Ini menggabungkan pengayaan dan deteksi target ke dalam satu platform: manik-manik magnetik (MB) digunakan untuk menangkap dan memberi label target molekuler, dan target yang terikat manik dideteksi melalui penginderaan elektrokimia. Pendekatan ini memiliki banyak keuntungan praktis: i) sampel asli (plasma atau darah) dapat langsung digunakan tanpa perlu pemurnian sampel; ii) pengujian mencapai sensitivitas deteksi tinggi melalui pengayaan magnetik dan amplifikasi sinyal enzimatik; iii) berdasarkan skema deteksi listrik, sensor dapat dengan mudah diminiaturisasi sebagai perangkat portabel (Gbr. 3a).
Mendeteksi AA melalui penginderaan magneto-elektrokimia, bagaimanapun, menimbulkan tantangan teknis; karena AA adalah molekul kecil (~304,5 Da), immunoassays menggunakan sepasang AA-antibodi sulit untuk diterapkan. Dengan demikian kami mengeksplorasi format uji kompetitif (cMES; sensor magneto-elektrokimia kompetitif) yang hanya membutuhkan antibodi AA tunggal (Gbr. 3b). Untuk penangkapan target, kami melapisi MB dengan AA-antibodi (MBAb). Kami juga menyiapkan zat pesaing (AA-HRP) dengan mengkonjugasikan AA dengan enzim pengoksidasi (horseradish peroxidase, HRP). Secara khusus, kami menggunakan bentuk hapten; AA terkonjugasi pada bovine serum albumin (BSA), dan selanjutnya mengkonjugasikan HRP ke pembawa BSA (Gbr. S3). Untuk uji cMES, sampel darah dicampur dengan MBAb dan AA-HRP. Jumlah AA-HRP cukup untuk menjenuhkan situs pengikatan AA di MBAb (Metode). Ini akan menyebabkan pemuatan HRP yang berbeda pada MB, tergantung pada jumlah AA endogen dalam sampel. Secara berurutan menambahkan mediator elektron kromogenik (3,3',5,5'-tetramethylbenzidine, TMB) menghasilkan arus listrik yang dibacakan oleh elektroda planar. Waktu reaksi untuk penangkapan AA dan inkubasi TMB dioptimalkan untuk memaksimalkan level sinyal (Gbr. S4).

Gambar 3. Sensor magneto-elektrokimia kompetitif (cMES) untuk pengujian AA. (A) Skema perangkat. Perangkat cMES memiliki footprint kecil dan mampu
operasi di tempat. (B) Kami merancang uji elektrokimia kompetitif untuk deteksi AA. Manik-manik magnetik (MBAb) terkonjugasi dengan antibodi terhadap AA.
Sampel kontrol hanya mengandung AA-HRP dan dicampur dengan manik-manik magnetik. Sampel uji dicampur dengan manik-manik magnetik dan AA-HRP. (C) Arus listrik
diukur oleh pembaca cMES portabel. Dalam uji cMES, besarnya arus menurun dengan meningkatnya konsentrasi AA [AA]. Sinyal dari kontrol
sampel mengatur dasar untuk [AA]=0 ng/mL. Perbedaan arus (∆I) antara kontrol dan sampel plasma yang ditargetkan digunakan sebagai metrik analitik. (D)
Jumlah AA yang diketahui dibubuhi serum dan diukur dengan cMES. Batas deteksi adalah ~ 126 ng/mL. (E) cMES dan ELISA dibandingkan untuk
konkordansi. Hasil dari kedua modalitas menunjukkan kesepakatan yang baik (R2=0.959). Data ditampilkan sebagai mean ± SEM dari pengukuran rangkap tiga.

Gambar 4. Pengukuran AA dalam sampel plasma. (A) Analisis kursus waktu tingkat AA tikus setelah injeksi plasma. Kami menyuntikkan 13{{10}} L plasma (konsentrasi AA=7.2 g/mL) ke dalam tikus (n=6) dan mengumpulkan darah tikus setelah 3, 7 dan 14 hari. Kadar AA darah tikus kemudian dipantau. Tingkat AA meningkat secara signifikan pada hari ke-3 dan kembali ke tingkat normal setelah 7 hari. *p < 0.05;="" **p="">< 0.01;="" ***p="">< 0.001.="" (b)="" sampel="" plasma="" tikus="" diuji.="" pada="" kelompok="" kontrol="" (n="5)," tikus="" muda="" (usia,="" 5="" dan="" 8="" bulan)="" memiliki="" tingkat="" aa="" lebih="" tinggi="" daripada="" tikus="" tua="" yang="" diperlakukan="" palsu="" (usia,="" 20="" dan="" 23="" bulan;="" n="8)." untuk="" kelompok="" yang="" diobati="" dengan="" plasma="" (n="5)," peningkatan="" aa="" yang="" berkelanjutan="" diamati.="" *p="">< 0,05;="" **p="">< 0,01;="" ***p="">< 0,001.="" (c)="" sampel="" plasma="" dari="" kohort="" yang="" sama="" seperti="" pada="" (b)="" dianalisis="" dengan="" spektrometri="" massa.="" tingkat="" aa="" menunjukkan="" tren="" yang="" sama="" yang="" diukur="" dengan="" cmes.="" *p="">< 0,05;="" **p="">< 0,01;="" ***p="">< 0,001.="" data="" ditampilkan="" sebagai="" mean="" ±="">
Sebagai hasil dari uji kompetitif, besarnya arus listrik menurun dengan konsentrasi AA plasma yang lebih tinggi ([AA]). Oleh karena itu kami menyiapkan sampel kontrol dengan menginkubasi MBAb dengan AA-HRP saja. Sampel kontrol digunakan untuk menetapkan baseline atas (yaitu, [AA]=0 ng/mL) untuk menghitung perbedaan sinyal; arus listrik dari kontrol dan sampel plasma diukur, dan perbedaan bersih |∆I |=|Icontrol - Iplasma|diperoleh (Gbr. 3c). Seperti
pengukuran diferensial juga mengkompensasi sinyal latar belakang umum.
Eksperimen titrasi (Gbr. 3d) menggunakan sampel yang dibubuhi dengan jumlah AA yang bervariasi menunjukkan batas deteksi (LOD) sebesar ~125,9 ng/mL. LOD pengujian adalah ~300-kali lipat lebih rendah dari konsentrasi AA khas (38 g/ml) dalam plasma tikus muda (5 bulan, n=2). Berdasarkan hasil ini, kami mengencerkan sampel plasma awal (100-kali lipat) dengan menambahkan larutan buffer (lihat Metode). Sinyal dari pengikatan nonspesifik mendekati tingkat latar belakang intrinsik (~43 nA), berpotensi diuntungkan dari faktor pengenceran tinggi. Kami juga mengkonfirmasi bahwa hasil assay cocok dengan hasil ELISA konvensional (R2=0.961, Gbr. 3e). Uji cMES, bagaimanapun, lebih cepat (1 jam) daripada ELISA (4 jam), sebagian besar karena kinetika pengikatan yang cepat; di cMES, MB menangkap AA di seluruh volume sampel (3-difusi dimensi), sedangkan penangkapan AA bergantung pada 1-difusi dimensi dalam ELISA berbasis pelat.
Pemantauan AA pada tikus yang diobati dengan plasma
Kami menerapkan cMES untuk menganalisis kadar AA pada tikus setelah pengobatan plasma tunggal. Karena AA secara alami ada dalam darah tali pusat manusia, injeksi plasma secara aditif akan meningkatkan kadar AA tikus. Konsentrasi AA rata-rata dari enam plasma darah tali pusat manusia yang berbeda adalah 7,2 ± 0,5 g/mL (rata-rata ± SEM). Kami menyuntikkan 130 L plasma darah tali pusat manusia ke tikus (n=6) dan memantau kadar AA mereka (Gbr. 4a). Injeksi plasma segera meningkatkan kadar AA darah (hari 3; p <0,01, dibandingkan="" dengan="" semua="" titik="" waktu="" lainnya),="" tetapi="" efeknya="" bersifat="" sementara;="" tingkat="" aa="" kembali="" normal="" 7="" hari="" setelah="" pengobatan="" (p="0.34," dibandingkan="" dengan="" titik="" waktu="" sebelum="" injeksi="">
Kami selanjutnya memantau kadar AA plasma setelah jadwal pengobatan penuh (Gbr. S1). Tiga kelompok tikus yang berbeda digunakan: kelompok usia yang diobati dengan plasma (n=8) dan palsu (n=8) (berusia 20-23 bulan), dan kelompok kontrol muda (<8 months="" old,="" n="5)." we="" used="" 0.5="" µl="" of="" mouse="" plasma="" for="" each="" measurement.="" the="" sham="" group="" showed="" lower="" aa="" level="" compared="" to="" the="" young="" group="" (p="0.003," fig.="" 4b).="" the="" plasma="" treated="" group,="" however,="" showed="" increased="" aa="" levels="" even="" after="" 1="" month="" after="" the="" treatment.="" the="" effect="" was="" sustained="" up="" to="" 4="" months="" post="" treatment;="" the="" plasma-treated="" group="" had="" higher="" aa="" level="" than="" the="" sham="" group="" (p="0.0003)." we="" also="" analyzed="" aliquots="" of="" samples="" via="" lc/ms="" (fig.="" 4c).="" the="" results="" from="" both="" assays="" were="" concordant,="" corroborating="" aa's="" value="" as="" a="">
Perawatan plasma yang mengarah pada peningkatan kognitif dan perilaku pada tikus tua
Kami selanjutnya menilai fenotipe perilaku kohort hewan, terutama mengevaluasi pembelajaran motorik dan fungsi memori mereka. Kami melakukan {{0}}tes uji rotarod pada 1 dan 4 bulan setelah pengobatan plasma atau palsu (Gbr. 5a); latensi (waktu berjalan) tikus sebelum jatuh pada batang yang berputar digunakan untuk menilai kinerja motorik hewan. Pada 1 bulan setelah pengobatan (20-bulan), latensi dari kelompok palsu dan yang diobati dengan plasma secara signifikan lebih rendah (p <0,0001) dibandingkan="" dengan="" yang="" muda="" (5-bulan="" )="" kelompok="" (gbr.="" 5b).="" kelompok="" yang="" diobati="" dengan="" plasma,="" bagaimanapun,="" menunjukkan="" peningkatan="" bertahap="" dalam="" pembelajaran="" motorik="" dan="" memori,="" sedangkan="" fakultas="" yang="" sama="" menurun="" pada="" kelompok="" palsu.="" perubahan="" tingkat="" aa="" melanjutkan="" perubahan="" perilaku,="" yang="" dapat="" berfungsi="" sebagai="" indikator="" awal="">anti penuaanefek pengobatan (Gbr. 5c).
Analisis jaringan otak (Gbr. 5d, 5e) menunjukkan bahwa tikus tua (kelompok palsu) memiliki area sel DCX-positif yang lebih kecil di zona sub-ventrikular dibandingkan tikus muda. Sebaliknya, area sel DCX-positif meningkat pada hewan yang diobati dengan plasma dan tetap tidak berubah (p=0.04) menunjukkan bahwa plasma darah tali pusat yang disuntikkan merangsang neurogenesis otak tua. Hasilnya menunjukkan manfaat potensial dari pengobatan plasma pada neurogenesis berkelanjutan yang menghasilkan peningkatan fungsi motorik pada kelompok yang diobati.
Diskusi
Kemajuan dalam terapi peremajaan secara bersamaan meningkatkan kebutuhan akan ukuran objektif dan kuantitatif untuk membaca kemanjuran pengobatan. Dengan demikian kami merancang penelitian kami untuk mengidentifikasi biomarker molekuler yang dapat menjelaskan fitur fenotipik penuaan dananti penuaanperlakuan. Eksperimen hewan kami menghasilkan pengamatan berikut: i) profil metabolit dari kelompok tikus muda dan dewasa jelas berbeda; dan ii) menyuntikkan plasma tali pusat manusia ke tikus tua mengubah pola metabolit mereka lebih dekat dengan tikus muda. Menariknya, kami menemukan asam arakidonat (AA) sebagai biomarker pengganti yang paling efektif untukanti penuaanperlakuan; Metabolisme AA sangat tidak diatur baik pada tikus muda dan tikus yang diobati dengan plasma, dan ditemukan memainkan peran kunci dalam berinteraksi dengan jalur metabolisme lain seperti metabolisme asam linoleat [10, 18].
Kami selanjutnya mengembangkan sistem sensor portabel yang cepat (cMES) untuk memfasilitasi deteksi AA dalam penelitian rutin dan pengaturan klinis. Kami secara khusus mengintegrasikan skema uji kompetitif dengan pengayaan imunomagnetik dalam upaya untuk mendeteksi target molekul kecil (yaitu, metabolit) langsung dari sampel plasma. Kombinasi ini membawa keuntungan berikut. (i) Uji manfaat dari kinetika pengikatan cepat, karena manik-manik magnetik menangkap AA di seluruh volume sampel (3-difusi dimensi). (ii) Proses pengujian (misalnya, langkah pencucian) disederhanakan dengan magnet eksternal yang digunakan untuk pengumpulan manik-manik. (iii) Dengan mengkonsentrasikan manik-manik terikat AA secara magnetis di dekat elektroda deteksi, sinyal analitik keseluruhan dapat ditingkatkan (~72 persen) [12]. Memang, kami menunjukkan bahwa uji cMES menggunakan<1 µl="" of="" plasma="" with="" the="" total="" assay="" time="" within="" 1.5="" hour.="" both="" cmes="" and="" mass="" spectrometry="" consistently="" showed="" that="" plasma="" aa="" levels="" decrease="" with="" aging,="" but="" that="" they="" reversely="" increase="" with="" cord-plasma="" treatment.="" importantly,="" increases="" in="" aa="" levels="" could="" be="" an="" early="" indicator="" of="" improved="" cognitive="" functions="" in="" treated="" animals.="" these="" results="" highlight="" the="" utility="" of="" aa-cmes;="" with="" minimally="" invasive="" blood="" draw,="" individual="" patients="" can="" be="" monitored="" in="" a="" serial="" fashion="" to="" better="" assess="" treatment="">
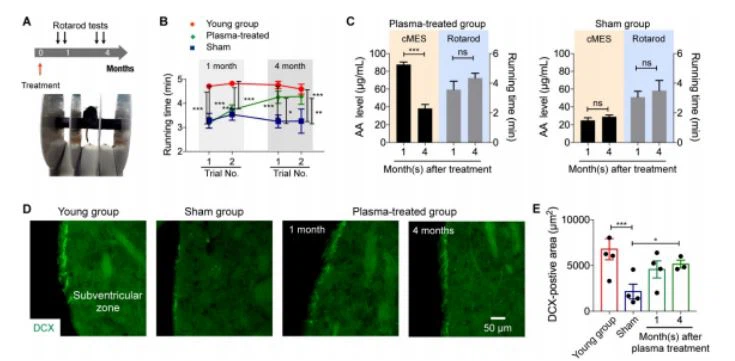
Gambar 5. Uji perilaku dan molekuler. (A) 2-uji coba Rotarod dilakukan pada 1 dan 4 bulan setelah injeksi plasma. (B) Kelompok yang diobati dengan plasma
menunjukkan peningkatan progresif dalam koordinasi motorik; kinerjanya mendekati kelompok muda pada akhirnya (percobaan kedua pada 3 bulan). Waktu berjalan dari kelompok palsu menurun dengan penuaan. *p < 0.05;="" **p="">< 0.01.="" (c)="" untuk="" kelompok="" perlakuan="" plasma,="" peningkatan="" kadar="" aa="" mendahului="" perbaikan="" fungsi="" motorik.="" *p="">< 0.05;="" **p="">< 0,01;="" ***p="">< 0,001.="" (d)="" sel-sel="" otak="" di="" zona="" subventrikular="" diimunisasi="" untuk="" penanda="" neurogenesis,="" doublecortin="">
Bilah skala adalah 50 m. Perhatikan bahwa kelompok palsu memiliki area sel DCX-positif yang lebih kecil secara signifikan di zona sub-ventrikular daripada tikus muda, sedangkan area meningkat pada hewan yang diobati dengan plasma dan tetap tidak berubah. (E) Area sel DCX-positif dalam gambar (D) diukur. *p < 0.05;="" ***p=""><>
AA telah terbukti meningkatkan pertumbuhan otot dan perkembangan otak [19, 20]. Laporan lain juga menyoroti potensi manfaat AA dalamanti penuaan[21, 22]. Studi saat ini sejalan dengan temuan ini, tetapi ruang lingkupnya terbatas untuk membangun hubungan korelatif antara tingkat AA dananti penuaanfenotipe. Pemantauan AA serial, bagaimanapun, menunjukkan bahwa peningkatan AA pada tikus yang diobati dengan plasma kemungkinan berasal dari sumber endogen, bukan dari plasma yang ditransfusikan. Apalagi, berkelanjutananti penuaanefek diamati pada tikus penerima bahkan 4 bulan setelah akhir pengobatan plasma. Pembelajaran motorik dan fungsi memori meningkat; dan jumlah sel prekursor saraf meningkat di otak. Pengamatan ini sangat menyarankan perubahan fisiologis pada tikus yang diobati dengan plasma; mekanisme yang tepat belum dapat dijelaskan.
Beberapa keterbatasan lain dari penelitian ini harus diatasi dalam penelitian masa depan. Pertama, uji cMES perlu disempurnakan untuk akurasi yang lebih tinggi. Secara khusus, dengan kurangnya sampel negatif yang sebenarnya (yaitu, sampel darah tanpa AA endogen), sulit untuk menjelaskan sinyal dari pengikatan non-spesifik. Dapat dibayangkan, pengaruh matriks darah dapat diabaikan karena kami mengencerkan sampel sebanyak 100-kali lipat. Asumsi seperti itu, bagaimanapun, harus divalidasi dengan menggunakan sampel plasma yang dihapus AA yang dapat dibuat dari model tikus yang kekurangan AA [23] atau melalui imunodeplesi AA. Kedua, kami fokus pada pendeteksian metabolit tunggal dalam metabolisme AA untuk kesederhanaan, tetapi pendekatan ini mungkin mengabaikan konteks biologis seperti interaksi antara metabolit dalam jalur tertentu. Memasukkan panel metabolit akan lebih baik menangkap gangguan metabolisme dan juga meningkatkan akurasi diagnostik. cMES dapat dengan mudah diskalakan untuk mendeteksi beragam penanda sambil mengonsumsi sampel dalam jumlah kecil. Ketiga, menginterpolasi temuan saat ini kepada manusia akan menjadi tantangan. Meskipun tikus dan manusia memiliki jalur metabolisme yang sama, tikus memiliki tingkat metabolisme 7-kali lipat lebih tinggi daripada manusia [24]. Percobaan pada manusia diperlukan untuk menentukan dosis plasma yang optimal untuk infus dan untuk menetapkan dasar untuk biomarker; diinformasikan oleh penelitian pada hewan, kami merencanakan penelitian pada manusia seperti itu. Upaya ini akan mempercepat pengembangananti penuaanterapi, meningkatkan kualitas hidup individu serta mengurangi beban masyarakat.

Metode
Desain eksperimental
Plasma dipisahkan dari darah tali pusat manusia yang dikumpulkan saat melahirkan. Plasma darah tali pusat diberikan melalui infus intravena pada tikus tua (18-bulan), dan kontrol palsu (18-bulan) dan tikus muda (3-bulan sebagai positif kontrol) disuntik dengan saline. Pada 1 dan 4 bulan setelah transplantasi, 2-tes uji rotarod dilakukan untuk menilai koordinasi motorik dan memori jangka panjang (Gbr. S1). Profil metabolit yang tidak ditargetkan dilakukan pada darah dari tiga kelompok dan analisis bioinformatika menentukananti penuaanjalur yang relevan (metabolisme asam arakidonat). Biosensor dikembangkan untuk mendeteksi asam arakidonat yang bersirkulasi darah dengan mudah dan efisien.
Persiapan sampel darah tali pusat
Darah tali pusat manusia dikumpulkan di bawah Institutional Review Board Rumah Sakit Umum CHA (Seoul, Korea, IRB No. CHAMC-2015- 08-130-009). Darah tali pusat disumbangkan dari 4 donor dan diobati dengan antikoagulan sitrat-fasfat-dekstrosa dengan adenin (CPDA-1). Plasma darah tali pusat diisolasi dengan sentrifugasi pada 2,000 g selama 15 menit pada suhu kamar. Sampel plasma terisolasi disimpan pada -80 derajat dan digunakan dengan siklus beku-cair tunggal pada suhu kamar.
Eksperimen hewan
Protokol hewan telah disetujui oleh CHA University Institutional Animal Care and Use Committee (IACUC). Kami menggunakan tikus C57BL/6 betina berusia 18-bulan untuk mengevaluasi gangguan metabolisme dan fenotipe perilaku yang berkorelasi dengan penuaan dananti penuaan. Kontrol positif adalah tikus C57BL/6 betina berumur 3-bulan. Semua tikus dibiakkan pada suhu kamar dalam siklus terang-gelap standar 12 jam. Untuk tikus dewasa, plasma darah tali pusat atau saline (130 L) disuntikkan secara intravena 12 kali selama 4 minggu. Plasma darah tali pusat manusia yang diisolasi tidak dikumpulkan, dan hewan yang diberikan menerima plasma darah tali pusat dari donor yang sama. Jumlah hewan yang digunakan dalam setiap percobaan dijelaskan di bagian metode yang sesuai. Plasma dikumpulkan melalui sentrifugasi (3,000 g, 15 menit pada suhu kamar).
Akuisisi metabolit dan analisis data
Untuk pembuatan profil metabolit yang terbawa darah, darah dikumpulkan dari tikus dengan tusukan jantung pada titik waktu yang ditentukan: kelompok muda (3-bulan, n=10), kelompok palsu ({{ 4}}bulan, n=10; 23-bulan, n=12), kelompok yang diberi plasma (20-bulan, n {{13 }}; 23-bulan, n=5). Sampel darah dianalisis menggunakan sistem kromatografi cair-spektrometri massa (LC-MS) (Agilent). Kami mengonversi file LC/MS ke dalam format mzXML standar (ProteoWizard) [25] dan kemudian memprosesnya menggunakan MAIT (toolkit identifikasi otomatis metabolit) [26] untuk deteksi fitur, analisis statistik, dan identifikasi metabolit. Fitur yang signifikan secara statistik (yaitu, metabolit terionisasi dan/atau terfragmentasi) diidentifikasi melalui analisis varians (ANOVA). Fitur-fitur ini dicocokkan dengan semua kemungkinan metabolit dalam database metabolome [9] berdasarkan rasio massa/muatan ion spektral massa (toleransi m/z 0.005). Kami mengkarakterisasi perubahan metabolit global melalui analisis pengelompokan hierarkis dan struktur bawaan data metabolomik melalui analisis komponen utama (PCA). Dua atau tiga ulangan teknis (memastikan bahwa variasi teknis jauh lebih kecil daripada variasi biologis) per tikus dimasukkan dalam pembelajaran tanpa pengawasan seperti PCA dan pengelompokan hierarkis. Pengelompokan hierarkis pada komponen utama (HCPC) dilakukan oleh FactoMineR, sebuah paket R [27]. Untuk analisis fungsional, jalur metabolisme yang paling mungkin terganggu oleh penuaan dan pengobatan plasma ditentukan melalui analisis jalur KEGG (MetaboAnalyst 3.0) [28]. Distribusi hipergeometrik digunakan untuk mengukur representasi berlebihan dari metabolit yang cocok dalam jalur KEGG tertentu.
Persiapan manik-manik imunomagnetik
Manik-manik magnetik (5 mg) yang dilapisi dengan gugus epoksi (Dynabeads M-270 Epoxy, Invitrogen) disuspensikan dalam 100 L larutan natrium fosfat 0,1 M. Seratus mikrogram antibodi terhadap asam arakidonat (Biomatik) ditambahkan dan dicampur secara menyeluruh. Seratus mikroliter larutan amonium sulfat 3 M ditambahkan, dan campuran diinkubasi pada suhu kamar selama 2 jam dan kemudian diinkubasi lebih lanjut pada suhu 4 derajat selama semalam dengan rotasi kemiringan lambat. Reaksi konjugasi dilakukan pada pH=7.4. Proses-proses ini menginduksi pembentukan ikatan kovalen antara kelompok epoksi (manik) dan amina (antibodi), yang sebelumnya telah kami konfirmasikan dengan menundukkan konjugat manik antibodi pada tantangan pH [29]. Rata-rata 2,4 × 104 antibodi diimobilisasi per manik. Manik-manik magnetik terkonjugasi antibodi dipisahkan dengan magnet permanen, dicuci dua kali dengan larutan PBS, dan disuspensikan kembali dalam 200 L PBS dengan 1 persen BSA. Manik-manik disimpan dalam 4 derajat hingga satu bulan.
Konjugasi HRP menjadi asam arakidonat
HRP kemudian dikonjugasikan ke BSA melalui kimia aminasi reduktif. Secara khusus, 100 g AA terkonjugasi BSA (RPU51089, Biomatik) dilarutkan dalam 0,5 mL buffer karbonat-biokarbonat 0,2 M (pH 9,4), ditambahkan ke satu miligram EZ-link terliofilisasi Plus Activated Peroxidase (Thermo Scientific), dan diinkubasi selama 1 jam pada suhu kamar. Selanjutnya, 10 L natrium cyanoborohydride (Thermo Scientific) ditambahkan dan campuran diinkubasi selama 15 menit pada suhu kamar. Akhirnya, 20 L buffer Quenching (Thermo Scientific) ditambahkan, diikuti dengan inkubasi 15 menit pada suhu kamar. Elektroforesis gel dan analisis pita protein mengkonfirmasi konjugasi HPR ke BSA-AA (Gbr. S3a). AA terkonjugasi HRP dikumpulkan dan dipekatkan dengan filter sentrifugal Amicon Ultra 100K (Millipore). Peroksidase dan BSA-AA yang tersisa dicuci dengan PBS selama empat kali.
Deteksi elektrokimia AA dalam sampel plasma
Untuk deteksi elektrokimia AA, darah dikumpulkan dari kelompok muda (n {{{0}}), palsu (n=8), dan plasma (n=5 selama 1 bulan dan n=5 selama 3 bulan). Sampel plasma tikus (0.5 L) diencerkan dalam 50 L BSA 1 persen dalam PBS (×100-kali lipat pengenceran) dan dicampur dengan larutan manik imunomagnetik (50 L) dan larutan AA terkonjugasi HRP (50 L). Jumlah AA-HRP cukup besar untuk menjenuhkan situs pengikatan dalam manik-manik magnetik. Kami menggunakan sekitar 8,4 × 107 manik-manik per pengujian, yang menyediakan situs pengikatan AA 2.0 × 1012. Jumlah AA-HRP adalah ~1,7×1013; rasio antara AA-HRP dan situs pengikatan adalah ~8:1. Campuran diinkubasi pada suhu kamar selama 1 jam dengan putaran miring lambat. Manik kontrol dibuat dengan mencampurkan 1 persen BSA dalam PBS (50 L) dengan larutan manik imunomagnetik (50 L) dan larutan AA terkonjugasi HRP (50 L). Semua manik-manik yang bereaksi dipisahkan dengan magnet permanen dan dicuci dua kali dengan 80 L PBS (1 persen BSA). Akhirnya, manik-manik disuspensikan kembali dalam 7 L PBS. Larutan manik-manik yang telah disiapkan dan 20 L larutan TMB (Biomatik) dimuat di atas elektroda. Setelah 6 menit, pengukuran kronoamperometri dimulai. Kami menggunakan sensor elektrokimia mini (sistem prototipe yang dikembangkan oleh AcurreHealth Inc.). Level saat ini dalam kisaran 40-45 d dirata-ratakan. Kami menggunakan faktor konversi (×100) untuk melaporkan perkiraan konsentrasi AA asli dalam plasma.
Uji imunosorben terkait enzim (ELISA)
Eksperimen ELISA dilakukan dengan menggunakan kit ELISA asam arakidonat (AA) tikus (Biomatik) sesuai dengan pedoman pembuatan. AA yang diencerkan secara serial ditambahkan ke setiap sumur, dan diinkubasi dengan AA terkonjugasi HRP pada 37 derajat selama 40 menit. Setelah dicuci dengan washing buffer sebanyak empat kali, ditambahkan larutan TMB dan diinkubasi selama 20 menit. Pengembangan warna dihentikan dengan menambahkan stop solution. Absorbansi dibaca pada 450 nm menggunakan microplate reader (Tecan).
Tes Rotarod
Kami memodifikasi uji Rotarod dari Kong et al. [30] untuk menilai koordinasi alat gerak. Rotarod dengan batang berdiameter 3-cm dimulai pada 4 rpm dan dipercepat sebesar 4 rpm per 30 detik selama 5 menit. Tikus ditempatkan pada batang, dan waktu yang dibutuhkan tikus untuk jatuh dari batang diukur. Setiap tikus diberi 3 percobaan sehari, dan waktu berjalan setiap hari dihitung sebagai rata-rata waktu pelatihan. Tes rotarod pertama dilakukan pada 1-bulan pasca pengobatan plasma: kelompok muda (n=29), kelompok palsu (n=17), kelompok yang diobati dengan plasma (n {{ 11}}). Sesi pelatihan ulang dimulai pada 4-bulan setelah pengobatan plasma. Untuk menghindari over training, dilakukan retraining selama 2 hari. Prosedur lainnya sama dengan sesi pertama.
Pencitraan jaringan otak
Pada 1 bulan (n=4) dan 4 bulan (n=3) setelah injeksi plasma darah tali pusat atau injeksi salin, hewan di-eutanasia dan kemudian diperfusi dengan 4 persen paraformaldehyde (PFA) dan PBS melalui ventrikel kiri. Kelompok muda (n=5) dan kelompok palsu (n=4) digunakan sebagai kontrol. Otak mereka adalah
diekstraksi dan dikrioproteksi. Setiap otak dipotong pada cryotome dengan ketebalan 30 m. Ke
melakukan imunohistokimia, pengikatan non-spesifik diblokir dengan 5 persen serum kambing normal dalam 0.3 persen Triton X-100 selama 40 menit. Antibodi primer terhadap Doublecortin (DCX; 1:400, Cell Signaling, #4604S) diaplikasikan semalaman pada 4 derajat, dan kemudian PBS digunakan untuk mencuci [31]. Antibodi sekunder Alexa Fluor 488 (1:2000, Invitrogen, #A11008) digunakan untuk mendeteksi DCX. Gambar diambil menggunakan mikroskop fluoresensi (Nikon Eclipse 80i) dan dianalisis menggunakan Gambar J [32].
Analisis statistik
Analisis statistik dilakukan menggunakan fungsi dasar R dan lme4, paket R untuk Linear
Model Efek Campuran atau Model Linier Umum
(GLM) diikuti dengan tes post-hoc LSD [33]. Data disajikan sebagai mean ± standard error dan nilai p < 0.05="" dianggap="">
Materi tambahan
Angka tambahan.
http://www.thno.org/v09p0001s1.pdf
Ucapan Terima Kasih
Kami berterima kasih kepada AccureHealth Inc. karena menyediakan sensor elektrokimia mini. Studi ini didukung sebagian oleh hibah Institute for Information and Communications Technology Promotion (IITP) yang didanai oleh Pemerintah Korea (MSIT) (2017M3A9B4025699).
Kepentingan Bersaing
Para penulis telah menyatakan bahwa tidak ada kepentingan yang bersaing.
